Proteomics of Tea Plant in Response to Infestation by Empoasca vitis
-
摘要:目的
探明都匀毛尖本地种茶树响应茶小绿叶蝉为害相关的蛋白质。
方法以被茶小绿叶蝉侵染0、12、24、36、48 h的都匀毛尖本地种茶树叶片为材料,利用串联质谱标签(tandem mass tag, TMT)结合液相色谱-串联质谱(LC-MS/MS)技术对茶小绿叶蝉侵染茶树叶片后的蛋白质进行定性定量分析。
结果共鉴定出2 893个蛋白质,0 h与12 h、24 h、36 h、48 h之间分别有0、1、848、849个差异蛋白质,共有2 622个蛋白质被注释,其中2 360个蛋白注释到GO数据库,1 232个注释到KEGG数据库。GO和KEGG分析表明茶小绿叶蝉侵染茶树时可能通过差异蛋白质4-二磷酸胞基-2-c-甲基-d-赤藓糖醇激酶、法尼基二磷酸合成酶、香叶基二磷酸合成酶、香叶基香叶基二磷酸合成酶、过氧化物酶、果胶酯酶、丙二烯氧化环化酶、倍半萜类、三萜类、单萜类、二萜类化合物以及倍半萜和三萜生物合成途径、萜类骨架生物合成途径和单萜生物合成途径来抵御害虫的侵染。
结论筛选出4个差异蛋白质(4-二磷酸胞基-2-c-甲基-d-赤藓糖醇激酶、法尼基二磷酸合成酶、香叶基二磷酸合成酶和香叶基香叶基二磷酸合成酶)和萜类化合物可能在应答防御小绿叶蝉侵害时具有重要的作用。研究结果可为揭示茶树应答茶小绿叶蝉为害的分子机制提供理论依据。
Abstract:ObjectiveProteins related to the response of Duyun Maojian native tea plant infested by Empoasca vitis were studied.
MethodLeaves of Duyun Maojian native tea plant were artificially infested by E. vitis Göthe for 0, 12, 24, 36, and 48 h. Tandem mass tag combined with liquid chromatography-tandem mass spectrometry was applied to detect the proteins generated in the leaves by the infestation.
ResultsThe chemical analysis identified 2 893 proteins that included 0, 1, 848, and 849 differential expression proteins (DEPs) in the leaf specimens sampled at the time periods that lasted from 0 h to 12 h, 24 h, 36 h, and 48 h, respectively. Of the 2 622 annotated proteins, 2 360 were explained to the GO database and 1 232 to the KEGG database. The GO and KEGG analyses indicated that the tea plants might be resistant to E. vitis infestation through the enzymes, such as CMK, FPPS, GPPS, GGPPS, peroxidase, pectinesterase, and allene-oxide cyclase, the biosynthesis of sesquiterpenoid, triterpeoid, monoterpenoid, and diterpenoid, and/or the biosynthesis pathways of sesquiterpenoid, triterpenoid, terpenoid backbone, and monoterpenoid.
ConclusionFour DEPs, i.e., CMK, FPPS, GPPS, and GGPPS, and terpenoids might play important roles in the response and defense of the tea plant against E. vitis Göthe.
-
Keywords:
- tea plant /
- Empoasca vitis Gothe /
- proteomics /
- tandem mass tag /
- differential expression protein
-
0. 引言
【研究意义】茶树起源于中国西南地区[1],贵州省都匀毛尖茶享誉世界,曾获巴拿马茶叶赛会优质奖[2]。都匀毛尖本地种茶树在生长过程中常受到茶小绿叶蝉的为害,茶小绿叶蝉喜好刺吸芽下第二叶,一般不大喜爱芽下五、六叶和更老的叶片[3],使茶叶产量和质量受到影响[4]。目前,茶树对茶小绿叶蝉的应答研究已经延伸到分子生物学水平。探索茶树被茶小绿叶蝉为害的研究对于探索都匀毛尖本地种茶树的响应害虫侵染的分子机制和品质提高具有重要意义。【前人研究进展】潘杰[5]应用分子生物学技术探讨了两种茶树抗性蛋白对茶小绿叶蝉的毒性作用,结果表明核糖体失活蛋白对茶小绿叶蝉具有明显的毒性作用。杨会敏[6]研究发现了21个基因主要编码植物防卫蛋白。王梦馨[7]研究表明丙二烯氧化物环化酶在茶树应对小绿叶蝉侵染时具有重要的作用。任倩倩[8]研究表明萜类化合物合成酶在抵御小绿叶蝉侵染时具有重要作用。小绿叶蝉取食为害还可以诱导茶树体内芳樟醇合成酶基因的上调表达[9]。小绿叶蝉为害显著诱导了茶树体内调控茉莉酸(Jasmonic acid, JA)和水杨酸(Salicylic acid, SA)通路的相关转录因子上调,这些转录因子可作为调控茶树对茶小绿叶蝉抗性的潜在因子[10]。蛋白质组是研究一个生物体、组织或细胞内的所有蛋白质,其核心内容是探索蛋白质的动态变化规律[11],因此研究蛋白质组学可以对生物体的生长发育、代谢过程甚至是疾病的发生等方面有着全面的认识,从而更加全面地掌握生命现象和本质,了解生命活动的规律[12]。应用蛋白质组学技术在茶树中的研究目前主要体现在茶树抗寒、抗旱、抗虫、差异蛋白质组、亚细胞水平等方面[13]。庄重光[14]利用蛋白质组学技术研究铁观音茶树叶片在不同水分处理条件下参与光合作用的蛋白质表达情况。郭春芳[15]利用蛋白质组学方法分析茶树对干旱胁迫的应答机制,为揭示茶树响应干旱胁迫的分子机理提供了理论依据。Li等[16]对茶花粉进行蛋白质组研究,表明冷冻是保持茶花粉质量的最佳储存方式。Chien等[17]利用蛋白质组学技术分别对遭受不同程度茶小绿叶蝉为害的乌龙茶鲜叶进行蛋白质组学分析。邹瑶等[18]探讨蛋白质组学关键技术在茶树研究中的应用,从而为认识茶树的生命本质指明方向。周琼琼等[19]研究茶树总蛋白质的提取方法,为开展茶树蛋白质组学研究奠定了基础。Hu等[20]应用MALDI-TOF-MS技术研究发现茶树冻害组和正常组的差异蛋白主要是参与碳代谢的酶等。Xu等[21]利用iTRAQ蛋白质组技术研究茶树对铝胁迫的响应机制。吴致君[22]通过iTRAQ技术,研究茶叶在3种萎凋处理中蛋白质组的变化。任燕[23]以蛋白质组学的方法对茶树自交和杂交授粉后24、48、72 h的雌蕊蛋白质进行差异表达分析,探讨茶树的自交不亲和性。蛋白质组学技术串联质谱标记(tandem mass tag, TMT)与液相色谱质谱联用(liquid chromatography tandem mass spectrometry, LC-MS/MS)相结合是一种基于标记定量的新技术,可以对多个样品进行蛋白质和多肽的定量分析[24]。TMT是定量蛋白质组学中最常用的同位素标记方法,提高了蛋白质的相对表达量的准确性和可重复性,该方法可对鉴定的蛋白质进行相互验证[25,26]。【本研究切入点】茶树应答茶小绿叶蝉为害的分子机制尚不清楚,因此,通过TMT蛋白质组学技术研究茶树被茶小绿叶蝉侵染后蛋白质的表达量变化亟需进行。【拟解决的关键问题】以茶小绿叶蝉吸食0、12、24、36、48 h的都匀毛尖本地种茶树叶片为试验材料,运用TMT蛋白质组学技术,研究茶鲜叶被茶小绿叶蝉取食后蛋白质表达量的变化,为揭示茶树响应茶小绿叶蝉为害的分子机制提供理论依据,为选育茶树抗虫良种奠定理论基础。
1. 材料与方法
1.1 材料与仪器
2019年底从都匀市红敏茶园选取1株长势优良的茶树[Camellia sinensis (L.) O. Kuntze]作为母株,剪取茎叶进行扦插培养。2022年7月选取15株长势情况一致并且健康的茶苗分为5组进行茶小绿叶蝉的侵染试验。将5组茶苗分别放入5个大小一致的纱网笼中,分别标记为0、12、24、36、48 h。除了0 h的纱网笼中不放入小绿叶蝉,其余4个纱网笼中分别放入100头茶小绿叶蝉,在侵染0 h时从第一组第一株中取5片健康叶作为侵染0 h第一个生物学重复,第一组第二株取5片健康叶作为侵染0 h第二个生物学重复,第一组第三株取5片健康叶作为侵染0 h的第三个生物学重复;12 h时在第二组第一株中选取5片叶作为侵染12 h的第一个生物学重复,以此类推,总共15个样本,全部放入液氮中进行固定,然后放入−80 ℃冰箱中进行存储。
主要试剂包括:碳酸氢铵(Sigma-Aldrich, A6141-500 G)、TEAB(Sigma-Aldrich, T7408-100 mL)、尿素(Amresco, M123-1 KG)、蛋白定量染液(Huaxingbio, HXJ5137)、牛血清白蛋白(Thermo Scientific, 23209)、二硫苏糖醇DTT(Amresco, M109-5G)、碘代乙酰胺IAM(Amresco, M216-30 G)、胰蛋白酶(Promega, V5280/100 μg)、乙腈(J.T.Baker, 34851 MSDS)、甲酸(Sigma-Aldrich, T79708)、进样瓶(Thermo, 11190533)、瓶盖(Thermo, 11150635)。
主要仪器包括:高效液相色谱系统(北京普源精电科技有限公司,型号:RIGOL L-3000)、涡旋振荡器(SCILOGEX,型号:MX-S)、真空离心浓缩仪(北京吉艾母科技有限公司,型号:CV100-DNA)、电热恒温水浴锅(北京市光明医疗仪器有限公司,型号:XMTD-7000)、高通量组织研磨器(上海贺帆仪器有限公司,型号:HF-48)、超声破碎仪(上海沪析实业有限公司,型号:JY96-IIN)。
1.2 蛋白质提取、酶解脱盐和样本标记
将冷冻的样本研磨成粉末,加入裂解液超声1 s,停2 s,累计120 s。14 000×g、4 ℃离心20 min,收取上清液进行蛋白定量,SDS-PAGE进行质控。
取100 μg蛋白,加入终浓度为10 mmol·L−1二硫苏糖醇,37 ℃反应 1 h,然后恢复室温。加入终浓度40 mmol·L−1的碘代乙酰胺,避光室温45 min。使用碳酸氢铵稀释样本,并按照蛋白和胰酶质量比50∶1加入胰酶,37 ℃过夜。次日,加入50 μL 0.1%的甲酸进行终止反应。使用C18脱盐柱对样本进行脱盐,最后使用70%乙腈洗脱,收集流穿液,冻干。
取出TMT试剂于室温解冻后开盖,加入41 μL乙腈。振荡5 min,离心。将TMT试剂加入100 μg酶切好的样本中,室温反应1 h,然后加入氨水终止反应。混合标记后的样品,进行真空冷冻离心干燥。
1.3 LC-MS/MS质谱分析
流动相:A相(100%水, 0.1%甲酸),B相(80%乙腈,0.1%甲酸)。使用10 μL A液溶解冻干粉末,4 ℃下14 000×g离心20 min,取上清1 μg样品进样,进行液质检测。液相色谱洗脱条件为:0 min(7% B),7 min(15% B),34 min(25% B),49 min(40% B),50 min(100% B),60 min(100% B),流速为600 nL·min−1。分离后的肽段使用Orbitrap ExplorisTM 480质谱仪进行分析,补偿电压CV在−45和−65之间每1 s切换1次,一级质谱分辨率设为
60000 ,扫描范围m/z 350~1500 ,二级质谱检测采用“Top Speed”模式,生成质谱检测原始数据。1.4 数据处理
利用Proteome Discoverer2.4软件对原始数据进行Uniprot_Camellia sinensis数据库检索,获得蛋白质和肽段定性和定量的结果。
2. 结果与分析
2.1 质谱鉴定结果评估
质谱鉴定到的肽段长度范围主要为15~30 aa,过长的肽段(>40 aa)由于分子量太高难以被质谱鉴定到,<7 aa的肽段大部分被过滤掉。同时肽段长度大部分在24 aa以内,在16~19 aa达到峰值,展示了1个符合理论肽段长度的分布情况(图1A)。鉴定到蛋白质的肽段分布中含有1个肽段的蛋白质最多,其次是含有两个肽段的蛋白质,说明肽段的蛋白质鉴定效率高,蛋白质的数量相对集中在1~20个肽段的范围内(图1B)。蛋白质的相对分子质量主要集中在10~150 kDa,在20~50 kDa达到峰值,相对分子质量越大,鉴定到的蛋白质数量越少(图1C)。1个蛋白质往往只有少数几个肽段被鉴定,蛋白质的覆盖率能显示蛋白质被鉴定的情况,覆盖率越高,对于解释蛋白异构体等越有利。鉴定到的蛋白质数量的覆盖率在3%~5%达到峰值,覆盖率在70%以上的蛋白质数量几乎为0(图1D)。
2.2 主成分分析
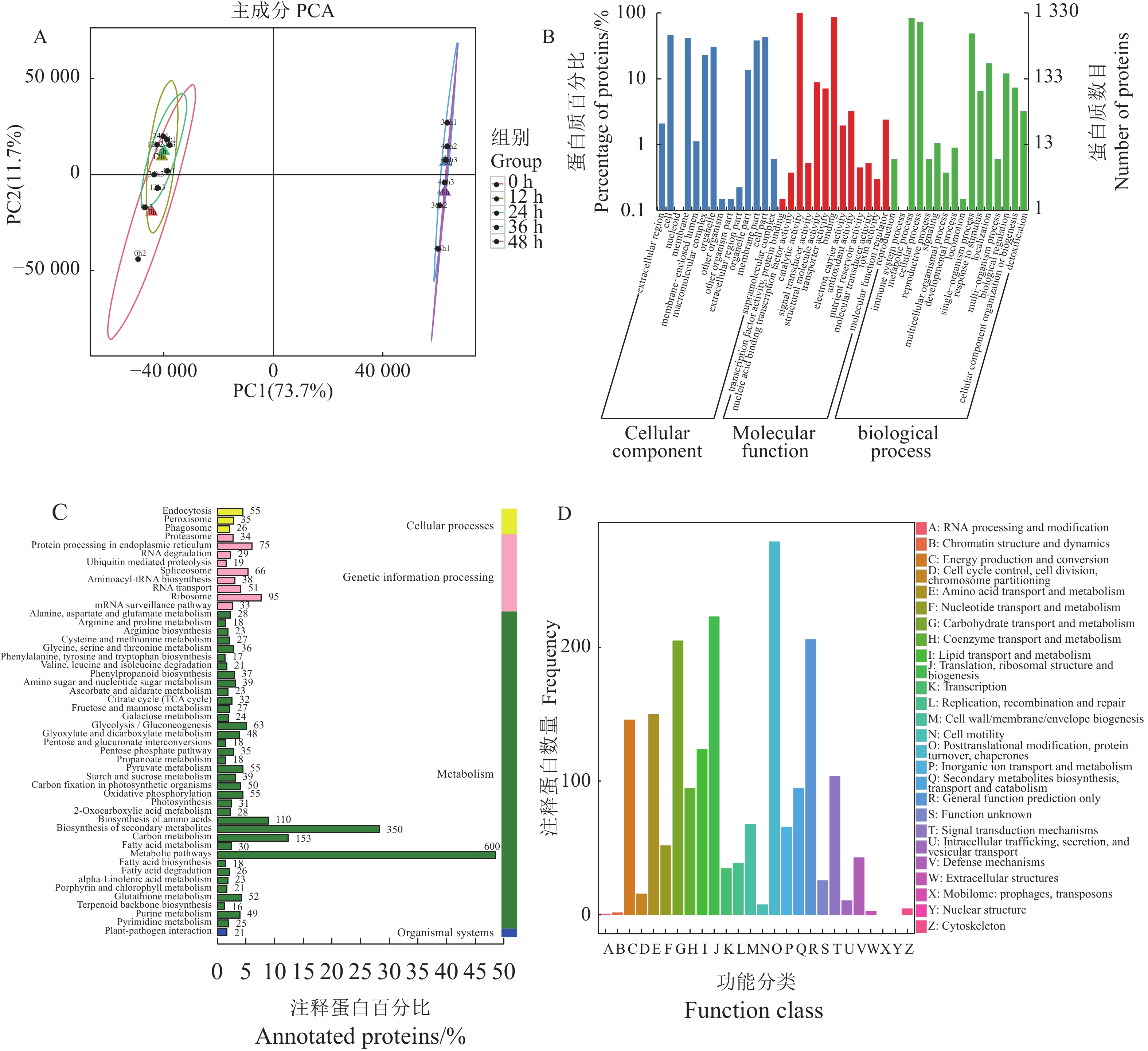
对茶小绿叶蝉侵染0、12、24、36、48 h的15个样本的蛋白组进行主成分分析,0、12、24、36、48 h的蛋白质基本上可以区分(图2A),表明在试验过程中数据的重现性较好。主成分1和2的贡献值分别为73.7%和11.7%,样品累积贡献值为85.4%,说明这两个主成分解释了85.4%的原始变量信息,代表性较好。
2.3 蛋白质注释
都匀毛尖本地种茶树被茶小绿叶蝉侵染0、12、24、36、48 h后共鉴定出2 893个蛋白质,共有2 622个蛋白质被注释,其中2 360个蛋白质注释到GO数据库,1 232个注释到KEGG数据库,1 813个注释到COG数据库。在GO注释中,注释最多的分类中,有1 330个蛋白质注释到催化活性,1 153个蛋白质注释到结合性,1 122个蛋白质注释到代谢过程,966个蛋白质注释到细胞过程,653个蛋白质注释到单生物过程,619个蛋白质注释到细胞,577个蛋白质注释到细胞部分,550个蛋白质注释到膜,509个蛋白质注释到膜部分,410个蛋白质注释到细胞器,309个蛋白质注释到大分子复合物,230个蛋白质注释到定位,182个蛋白质注释到细胞器部分,161个蛋白质注释到生物调节,118个蛋白质注释到结构分子活性(图2B)。对茶小绿叶蝉侵染茶树后鉴定出的所有蛋白质进行KEGG分析,能确定蛋白质参与的最主要的生物化学代谢通路。所有鉴定出的蛋白质共注释到118条代谢通路中,注释到的蛋白质最多的通路分别是600个蛋白质注释到代谢通路中,350个蛋白质注释到次级代谢物的生物合成,153个蛋白质注释到碳代谢,110个蛋白质注释到氨基酸的生物合成,95个蛋白质注释到核糖体,75个蛋白质注释到内质网上的蛋白质加工,66个蛋白质注释到剪接体,63个蛋白质注释到糖酵解/糖质新生(图2C)。对鉴定到的蛋白质进行COG注释,其中279个蛋白质参与翻译后修饰、蛋白质周转和伴侣蛋白;223个蛋白质参与翻译、核糖体结构和生物发生过程;43个蛋白质参与防御机制的过程(图2D)。
2.4 差异蛋白质分析
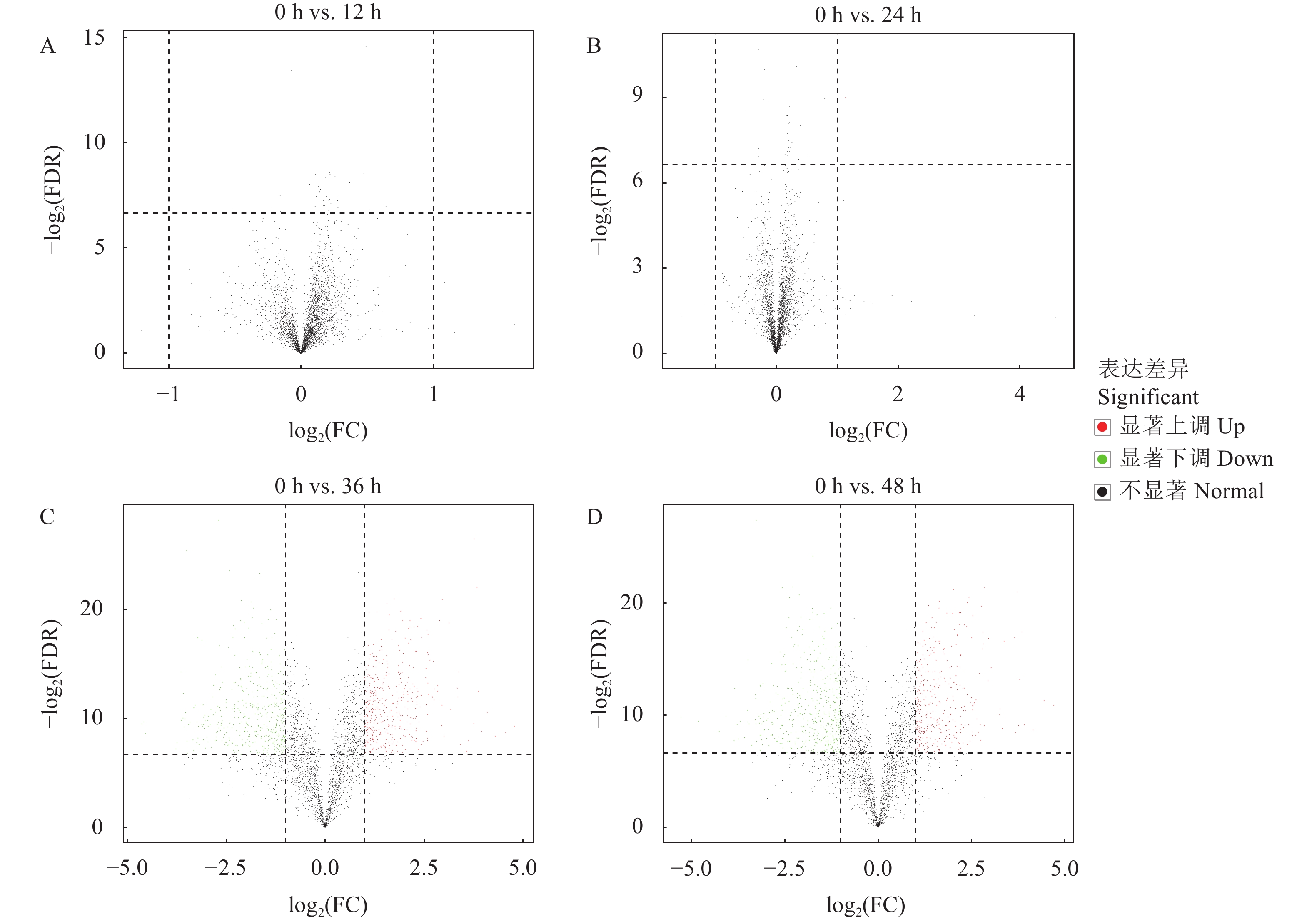
蛋白质在茶小绿叶蝉侵染0、12、24、36、48 h表达量不同,将差异倍数(Fold change)≥2且指错误发现率(False Discovery Rate, FDR)<0.01作为筛选差异蛋白质的标准,得到茶小绿叶蝉侵染0 h与12 h、0 h与24 h、0 h与36 h、0 h与48 h之间的差异蛋白质(表1)。0 h与12 h间没有差异蛋白质,可能由于蛋白质的数量太少。0 h与24 h之间有1个差异蛋白,并且在侵染24 h时上调。0 h与36 h之间有848个差异蛋白,其中385个上调,463个下调。0 h与48 h之间有849个差异蛋白,374个上调,475个下调。以log2(Fold change)为横坐标,以t检验显著性P值的负对数−log2(FDR)为纵坐标,绘制茶小绿叶蝉侵染都匀毛尖本地种茶树5个时间点的火山图,可以形象地反映出5个时间点蛋白质表达水平的差异(图3)。
表 1 差异表达蛋白质Table 1. Differential expression proteins差异蛋白
Differential expression protein差异蛋白数
The number of DEPs上调
Up-regulated下调
Down-regulated0 h vs. 12 h 0 0 0 0 h vs. 24 h 1 1 0 0 h vs. 36 h 848 385 463 0 h vs. 48 h 849 374 475 2.5 差异蛋白质GO功能注释
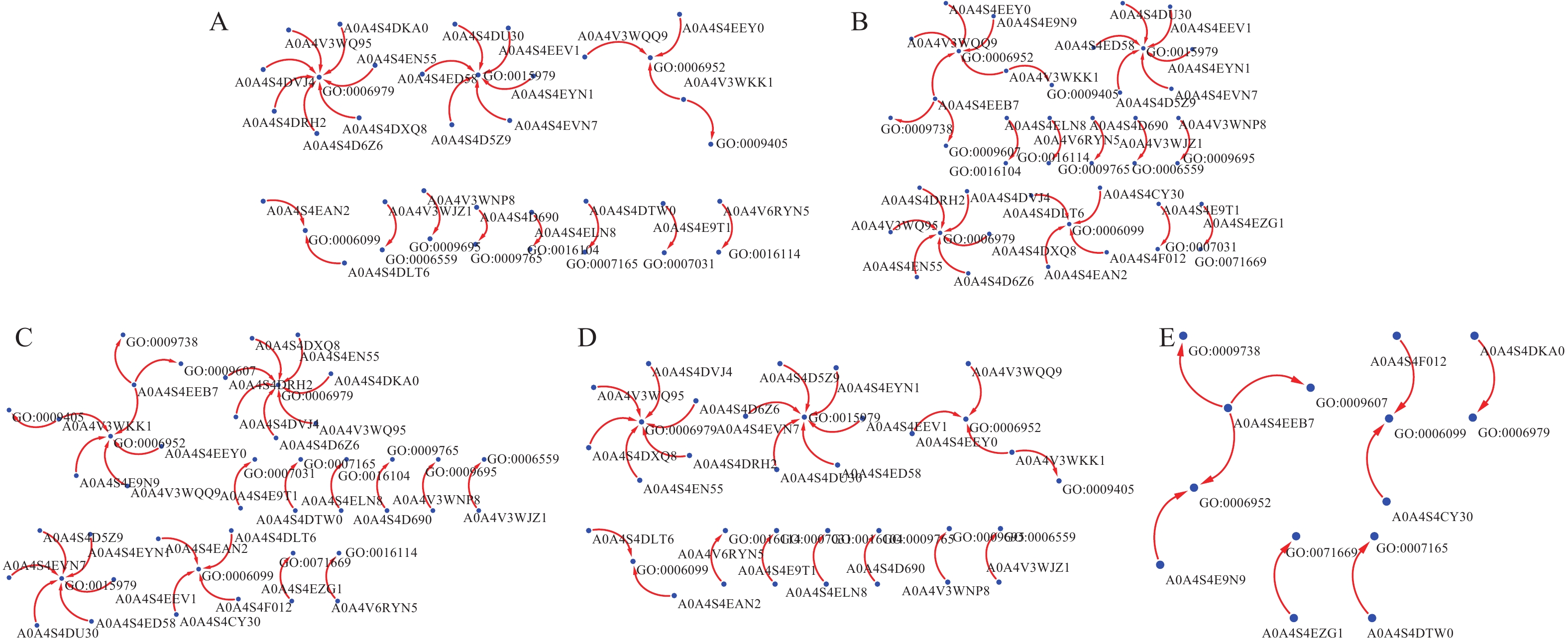
0 h与24 h有1个差异蛋白质A0A4S4E1L9 (含有延伸蛋白结构域的蛋白质)注释到细胞壁的结构组成和植物型细胞壁组织。0 h与36 h、0 h与48 h分别有708和693个差异蛋白质注释到GO数据库。0 h与36 h的差异蛋白质中,A0A4S4DU30(PSI反应中心亚基II,叶绿体)、A0A4S4EYN1(PSI亚基V)、A0A4S4ED58(NADPH-原叶绿素氧化还原酶)、A0A4S4EEV1(PSII产氧系统23kda亚基)、A0A4S4D5Z9(香叶基二磷酸还原酶)在光合作用中富集;A0A4V3WKK1(核糖体失活蛋白)、A0A4V3WQQ9(包含Bet v I/主要乳胶蛋白结构域蛋白)、A0A4S4EEY0(包含Bet v I/主要乳胶蛋白结构域蛋白)在防御反应中富集;A0A4V6RYN5[4-(胞苷5'-二磷酸)-2- c -甲基-d -赤藓糖醇激酶]在萜类化合物生物合成途径中富集;A0A4S4E9T1(包含wd重复区结构域的蛋白)在过氧化物酶体组织中富集;A0A4S4ELN8(萜烯环化酶/突变酶家族成员)在三萜生物合成途径中富集;A0A4S4D690(叶绿素a-b结合蛋白,叶绿体)在光合作用、光收集中富集;A0A4V3WNP8(丙二烯氧化环化酶)在茉莉酸生物合成途径中富集;A0A4V3WKK1(核糖体失活蛋白)在发病机理中富集(图4A)。0 h与48 h的差异蛋白质中,A0A4S4DU30(PSI反应中心亚基II,叶绿体)、A0A4S4ED58(NADPH-原叶绿素氧化还原酶)、A0A4S4D5Z9(香叶基二磷酸还原酶)在光合作用中富集;A0A4V3WKK1(核糖体失活蛋白)、A0A4V3WQQ9(包含Bet v I/主要乳胶蛋白结构域蛋白)、A0A4S4EEB7(包含Bet v I/主要乳胶蛋白结构域蛋白)、A0A4S4E9N9(包含Bet v I/主要乳胶蛋白结构域蛋白)、A0A4S4EEY0(包含Bet v I/主要乳胶蛋白结构域蛋白)在防御反应中富集;A0A4V3WNP8(丙二烯氧化环化酶)在茉莉酸生物合成过程中富集;A0A4S4D690(叶绿素a-b结合蛋白,叶绿体)富集在光合作用、光收集中;A0A4V6RYN5[4-(胞苷5'-二磷酸)-2- c -甲基-d -赤藓糖醇激酶]在萜类化合物生物合成途径中富集;A0A4S4EEB7(包含Bet v I/主要乳胶蛋白结构域蛋白)在脱落酸激活信号通路中富集;A0A4V3WKK1(核糖体失活蛋白)在发病机理中富集;A0A4S4ELN8(萜烯环化酶/突变酶家族成员)在三萜生物合成途径中富集;A0A4S4E9T1(包含wd重复区结构域的蛋白)在过氧化物酶体组织中富集(图4B)。并且合并了0 h与12 h、0 h与36 h、0 h与48 h的富集网络(图4C)。同时,还发现了0 h与36 h和0 h与48 h差异蛋白质富集网络的共性和差异(图4D、图5E)。
![]() 图 4 差异蛋白质的GO富集网络A:0 h与36 h差异蛋白质的GO富集网络;B:0 h与48 h差异蛋白质的GO富集网络;C:差异蛋白质GO富集网络;D:0 h与36 h和0 h与48 h共同的差异蛋白质GO富集网络;E:0 h与36 h和0 h与48 h不同的差异蛋白质GO富集网络。Figure 4. GO enrichment networks of DEPsA: GO enrichment network between 0 h and 36 h; B: GO enrichment network between 0 h and 48 h; C: merged GO enrichment network of DEPs; D: GO enrichment network of shared DEPs between 0–36 h and 0–48 h; E: GO enrichment network of distinct DEPs between 0–36 h and 0–48 h.
图 4 差异蛋白质的GO富集网络A:0 h与36 h差异蛋白质的GO富集网络;B:0 h与48 h差异蛋白质的GO富集网络;C:差异蛋白质GO富集网络;D:0 h与36 h和0 h与48 h共同的差异蛋白质GO富集网络;E:0 h与36 h和0 h与48 h不同的差异蛋白质GO富集网络。Figure 4. GO enrichment networks of DEPsA: GO enrichment network between 0 h and 36 h; B: GO enrichment network between 0 h and 48 h; C: merged GO enrichment network of DEPs; D: GO enrichment network of shared DEPs between 0–36 h and 0–48 h; E: GO enrichment network of distinct DEPs between 0–36 h and 0–48 h.2.6 差异蛋白质KEGG功能注释
对差异蛋白质进行KEGG分类,0 h与36 h之间有343个差异蛋白质注释到KEGG中,0 h与48 h之间有340个蛋白质注释到KEGG,大多数差异蛋白质参与代谢途径、次级代谢生物合成、碳代谢、核糖体和氨基酸的生物合成。1个差异蛋白质参与泛酸和辅酶A的生物合成,C5支链二氢酸代谢、类胡萝卜素的生物合成、RNA聚合酶和脂肪酸延伸等生物过程(图5)。
![]() 图 5 差异蛋白质KEGG功能分类A:0 h vs.36 h;B:0 h vs. 48 h 。1:内吞作用;2:过氧化物酶体;3:吞噬体;4:蛋白酶体;5:蛋白质输出;6:内质网蛋白加工;7:RNA降解;8:泛素介导的蛋白水解;9:核苷酸切除修复;10:剪接体;11:氨酰tRNA生物合成;12:RNA转运;13:核糖体;14:真核生物中核糖体生物发生;15:mRNA监测途径;16:丙氨酸、天冬氨酸和谷氨酸代谢;17:精氨酸和脯氨酸代谢;18:半胱氨酸和蛋氨酸代谢;19:甘氨酸、丝氨酸和苏氨酸的代谢;20:苯丙氨酸代谢;21:苯丙氨酸、酪氨酸和色氨酸:生物合成;22:酪氨酸代谢;23:苯丙素:生物合成;24:氨基糖和核苷酸糖代谢;25:柠檬酸循环;26:果糖和甘露糖代谢;27:糖酵解:糖质新生;28:乙醛酸盐和二羧酸盐代谢;29:戊糖磷酸途径;30:丙酸代谢;31:丙酮酸代谢;32:淀粉和蔗糖代谢;33:光合生物中:碳固定;34:氧化磷酸化;35:光合作用;36:氨基酸生物合成;37:次级代谢生物合成;38:碳代谢;39:脂肪酸代谢;40:代谢途径;41:脂肪酸生物合成;42:脂肪酸降解;43:α-亚麻酸代谢;44:碳池;45:卟啉和叶绿素代谢;46:维生素B6代谢;47:谷胱甘肽代谢;48:嘌呤代谢;49:嘧啶代谢;50:植物-病原互作;51:精氨酸生物合成;52:烟酸和烟酰胺代谢;53:萜类骨架生物合成。Figure 5. KEGG classifications of DEPsA: 0 h vs. 36 h; B: 0 h vs. 48 h. 1: Endocytosis; 2: peroxisome; 3: phagosome; 4: proteasome; 5: protein export; 6: protein processing in endoplasmic reticulum; 7: RNA degradation; 8: ubiquitin mediated proteolysis; 9: nucleotide excision repair; 10: spliceosome; 11: aminoacyl-tRNA biosynthesis; 12: RNA transport; 13: ribosome; 14: ribosome biogenesis in eukaryotes; 15: mRNA surveillance pathway; 16: alanine, aspartate, and glutamate metabolism; 17: arginine and proline metabolism; 18: cysteine and methionine metabolism; 19: glycine, serine, and threonine metabolism; 20: phenylalanine metabolism; 21: phenylalanine, tyrosine, and tryptophan biosynthesis; 22: tyrosine metabolism; 23: phenylpropanoid biosynthesis; 24: amino sugar and nucleotide sugar metabolism; 25: citrate cycle (TCA cycle); 26: fructose and mannose metabolism; 27: glycolysis/gluconeogenesis; 28: glyoxylate and dicarboxylate metabolism; 29: pentose phosphate pathway; 30: propanoate metabolism; 31: pyruvate metabolism; 32: starch and sucrose metabolism; 33: carbon fixation in photosynthetic organisms; 34: oxidative phosphorylation; 35: photosynthesis; 36: biosynthesis of amino acids; 37: biosynthesis of secondary metabolites; 38: carbon metabolism; 39: fatty acid metabolism; 40: metabolic pathways; 41: fatty acid biosynthesis; 42: fatty acid degradation; 43: alpha-linolenic acid metabolism; 44: one carbon pool by folate; 45: porphyrin and chlorophyll metabolism; 46: vitamin B6 metabolism; 47: glutathione metabolism; 48: purine metabolism; 49: pyrimidine metabolism; 50: plant-pathogen interaction; 51: arginine biosynthesis; 52: nicotinate and nicotinamide metabolism; 53: terpenoid backbone biosynthesis.
图 5 差异蛋白质KEGG功能分类A:0 h vs.36 h;B:0 h vs. 48 h 。1:内吞作用;2:过氧化物酶体;3:吞噬体;4:蛋白酶体;5:蛋白质输出;6:内质网蛋白加工;7:RNA降解;8:泛素介导的蛋白水解;9:核苷酸切除修复;10:剪接体;11:氨酰tRNA生物合成;12:RNA转运;13:核糖体;14:真核生物中核糖体生物发生;15:mRNA监测途径;16:丙氨酸、天冬氨酸和谷氨酸代谢;17:精氨酸和脯氨酸代谢;18:半胱氨酸和蛋氨酸代谢;19:甘氨酸、丝氨酸和苏氨酸的代谢;20:苯丙氨酸代谢;21:苯丙氨酸、酪氨酸和色氨酸:生物合成;22:酪氨酸代谢;23:苯丙素:生物合成;24:氨基糖和核苷酸糖代谢;25:柠檬酸循环;26:果糖和甘露糖代谢;27:糖酵解:糖质新生;28:乙醛酸盐和二羧酸盐代谢;29:戊糖磷酸途径;30:丙酸代谢;31:丙酮酸代谢;32:淀粉和蔗糖代谢;33:光合生物中:碳固定;34:氧化磷酸化;35:光合作用;36:氨基酸生物合成;37:次级代谢生物合成;38:碳代谢;39:脂肪酸代谢;40:代谢途径;41:脂肪酸生物合成;42:脂肪酸降解;43:α-亚麻酸代谢;44:碳池;45:卟啉和叶绿素代谢;46:维生素B6代谢;47:谷胱甘肽代谢;48:嘌呤代谢;49:嘧啶代谢;50:植物-病原互作;51:精氨酸生物合成;52:烟酸和烟酰胺代谢;53:萜类骨架生物合成。Figure 5. KEGG classifications of DEPsA: 0 h vs. 36 h; B: 0 h vs. 48 h. 1: Endocytosis; 2: peroxisome; 3: phagosome; 4: proteasome; 5: protein export; 6: protein processing in endoplasmic reticulum; 7: RNA degradation; 8: ubiquitin mediated proteolysis; 9: nucleotide excision repair; 10: spliceosome; 11: aminoacyl-tRNA biosynthesis; 12: RNA transport; 13: ribosome; 14: ribosome biogenesis in eukaryotes; 15: mRNA surveillance pathway; 16: alanine, aspartate, and glutamate metabolism; 17: arginine and proline metabolism; 18: cysteine and methionine metabolism; 19: glycine, serine, and threonine metabolism; 20: phenylalanine metabolism; 21: phenylalanine, tyrosine, and tryptophan biosynthesis; 22: tyrosine metabolism; 23: phenylpropanoid biosynthesis; 24: amino sugar and nucleotide sugar metabolism; 25: citrate cycle (TCA cycle); 26: fructose and mannose metabolism; 27: glycolysis/gluconeogenesis; 28: glyoxylate and dicarboxylate metabolism; 29: pentose phosphate pathway; 30: propanoate metabolism; 31: pyruvate metabolism; 32: starch and sucrose metabolism; 33: carbon fixation in photosynthetic organisms; 34: oxidative phosphorylation; 35: photosynthesis; 36: biosynthesis of amino acids; 37: biosynthesis of secondary metabolites; 38: carbon metabolism; 39: fatty acid metabolism; 40: metabolic pathways; 41: fatty acid biosynthesis; 42: fatty acid degradation; 43: alpha-linolenic acid metabolism; 44: one carbon pool by folate; 45: porphyrin and chlorophyll metabolism; 46: vitamin B6 metabolism; 47: glutathione metabolism; 48: purine metabolism; 49: pyrimidine metabolism; 50: plant-pathogen interaction; 51: arginine biosynthesis; 52: nicotinate and nicotinamide metabolism; 53: terpenoid backbone biosynthesis.3. 讨论与结论
蛋白质组学是从整体角度分析细胞内动态变化的蛋白质组成、表达水平与修饰状态,揭示蛋白质功能与细胞生命活动规律新的研究领域。本研究采用时间梯度法[27,28],以茶小绿叶蝉取食0、12、24、36、48 h的都匀毛尖本地种茶树叶片为试验材料,运用TMT蛋白质组学技术,研究茶鲜叶被茶小取食后蛋白质表达的变化,结果共鉴定出2 893个蛋白质,通过对多肽长度、数量、分子质量和覆盖率分布进行评估,与梅瑜等[29]和袁清华[30]的结果一致,说明结果较好。被鉴定出的蛋白质中有2 360个蛋白质注释到GO数据库,1 232个注释到KEGG数据库,1 813个注释到COG数据库。0 h与12 h、0 h与24 h、0 h与36 h、0 h与48 h间分别有0、1、848、849个差异蛋白质。
通过对差异蛋白质进行GO注释分析,茶小绿叶蝉侵染都匀毛尖茶树0、12、24、36、48 h的差异蛋白质通过参与各种生物反应来应对害虫的侵染。A0A4S4EEB7(包含Bet v I/主要乳胶蛋白结构域蛋白)参与脱落酸激活信号通路,A0A4V3WKK1(核糖体失活蛋白)、A0A4V3WQQ9(包含Bet v I/主要乳胶蛋白结构域蛋白)、A0A4S4EEY0(包含Bet v I/主要乳胶蛋白结构域蛋白)参与防御反应,A0A4S4F1Y0(果胶酯酶)和A0A4S4DYM7(果胶酯酶)参与细胞壁的修饰过程,A0A4S4D0Z6(过氧化物酶)、A0A4S4DRH2(谷胱甘肽过氧化物酶)、A0A4S4DXQ8(过氧化氢酶)、A0A4S4D6Z6(过氧化物酶)、A0A4V3WQ95(过氧化物酶)、A0A4S4DVJ4(谷胱甘肽过氧化物酶)、A0A4S4EN55(过氧化物酶)参与氧化应激反应,A0A4V3WNP8(丙二烯氧化环化酶)参与茉莉酸生物合成。A0A4V3WKK1(核糖体失活蛋白)参与发病机理,A0A4S4EEB7(包含Bet v I/主要乳胶蛋白结构域蛋白)参与对生物刺激的反应来达到对茶小绿叶蝉侵染的响应。因此,当都匀毛尖茶树被茶小绿叶蝉侵害时,推测茶树通过防御反应、脱落酸激活信号通路、茉莉酸生物合成等过程对茶小绿叶蝉进行防御应答,与前人的研究结果一致[31,32]。此外,A0A4S4DU30(PSI反应中心亚基II,叶绿体)、A0A4S4EYN1(PSI亚基V)、A0A4S4ED58(NADPH-原叶绿素氧化还原酶)、A0A4S4EEV1(PSII产氧系统23kda亚基)、A0A4S4D5Z9(香叶基二磷酸还原酶)可能通过参与光合作用来对茶小绿叶蝉进行应答,推测光合作用可为茶树防御茶小绿叶蝉的侵害提供能量。
在KEGG注释中,差异蛋白质A0A4S4ELN8(萜烯环化酶/突变酶家族成员)富集在倍半萜类和三萜类生物合成途径中,A0A4S4D5Z9(香叶基二磷酸还原酶)、A0A4S4EZ09(含丙烯酰半胱氨酸裂解酶结构域的蛋白)、A0A4V6RYN5(4-(胞苷5'-二磷酸)-2- c -甲基-d -赤藓糖醇激酶)富集在萜类骨架生物合成途径中,A0A4S4F1K4(短链脱氢酶/还原酶)富集在单萜生物合成途径中,A0A4S4ECG9(4-香豆酸辅酶A连接酶)富集在泛醌和其他萜类醌的生物合成途径中。萜类化合物能刺激植物产生天然的杀虫和保护物质,是植物代谢产物中种类最多的化合物,在茶树对害虫的直接和间接防御反应中起着重要作用。
在茶小绿叶蝉侵染都匀毛尖本地种茶树时,甲戊酸激酶途径的中乙酰辅酶A(Acetyl-CoA)通过乙酰乙酰辅酶A巯基酶(ATOT)转化为乙酰乙酰辅酶A(Acetoacetyl-CoA),再通过羟甲基戊二酰辅酶A合成酶(HMGS)转化为3-羟基-3-甲基戊二酰辅酶A(HMG-CoA)。HMG-CoA随后在NADPH和羟甲基戊二酰辅酶A还原酶(HMGR)的作用下转化为甲羟戊酸(MVA)。甲羟戊酸激酶催化MVA生成5-磷酸甲羟戊酸(MVAP)。然后,MVAP通过磷酸戊酸激酶和甲戊酸焦磷酸脱羧酶的催化转化为焦磷酸异戊烯(IPP)。在1-脱氧-d-木酮糖5-磷酸途径中,丙酮酸和甘油醛-3-磷酸通过1-脱氧-d-木酮糖5-磷酸合成酶(DXS)转化为1-脱氧-d-木酮糖5-磷酸(DXP),然后通过1-脱氧-d-木酮糖5-磷酸还原异构酶(DXR)转化为2-c-甲基-d-赤藓糖醇4-磷酸(MEP)。MEP随后通过4-二磷酸胞基-2- c -甲基-d -赤藓糖醇合成酶(CMS)和上调的4-二磷酸胞基-2- c -甲基-d -赤藓糖醇激酶(CMK)转化为4-二磷酸胞基-2- c -甲基-d -赤藓糖醇2-磷酸(CDP-ME2P),在2- c -甲基-d -赤藓糖醇2,4-环二磷酸合成酶(MCS)、1-羟基-2-甲基-2-(E)-丁烯基4-二磷酸合成酶(HDS)和异戊烯基单磷酸激酶(IPK)的催化下,将CDP-ME2P转化为焦磷酸异戊烯(IPP)。IPP在上调的法尼基二磷酸合成酶(FPPS)的催化下转化为法尼基焦磷酸(FPP)。IPP通过上调的香叶基二磷酸合成酶(GPPS)转化为香叶基二磷酸(GPP)。IPP通过上调的香叶基香叶基二磷酸合成酶(GGPPS)转化为香叶基二磷酸(GGPP)。FPP、GPP和GGPP通过不同的萜烯合成酶等催化分别转化为倍半萜类、三萜类、单萜类和二萜类化合物以响应茶小绿叶蝉对都匀毛尖茶树的侵染。因此,本文得出都匀毛尖本地种茶树中的倍半萜类、三萜类、单萜类、二萜类化合物在响应茶小绿叶蝉侵染时具有重要的作用,与前人的研究结果的一致[33,34]。研究结果可能为揭示茶树防御应答茶小绿叶蝉为害的分子机制提供理论依据。
-
图 4 差异蛋白质的GO富集网络
A:0 h与36 h差异蛋白质的GO富集网络;B:0 h与48 h差异蛋白质的GO富集网络;C:差异蛋白质GO富集网络;D:0 h与36 h和0 h与48 h共同的差异蛋白质GO富集网络;E:0 h与36 h和0 h与48 h不同的差异蛋白质GO富集网络。
Figure 4. GO enrichment networks of DEPs
A: GO enrichment network between 0 h and 36 h; B: GO enrichment network between 0 h and 48 h; C: merged GO enrichment network of DEPs; D: GO enrichment network of shared DEPs between 0–36 h and 0–48 h; E: GO enrichment network of distinct DEPs between 0–36 h and 0–48 h.
图 5 差异蛋白质KEGG功能分类
A:0 h vs.36 h;B:0 h vs. 48 h 。1:内吞作用;2:过氧化物酶体;3:吞噬体;4:蛋白酶体;5:蛋白质输出;6:内质网蛋白加工;7:RNA降解;8:泛素介导的蛋白水解;9:核苷酸切除修复;10:剪接体;11:氨酰tRNA生物合成;12:RNA转运;13:核糖体;14:真核生物中核糖体生物发生;15:mRNA监测途径;16:丙氨酸、天冬氨酸和谷氨酸代谢;17:精氨酸和脯氨酸代谢;18:半胱氨酸和蛋氨酸代谢;19:甘氨酸、丝氨酸和苏氨酸的代谢;20:苯丙氨酸代谢;21:苯丙氨酸、酪氨酸和色氨酸:生物合成;22:酪氨酸代谢;23:苯丙素:生物合成;24:氨基糖和核苷酸糖代谢;25:柠檬酸循环;26:果糖和甘露糖代谢;27:糖酵解:糖质新生;28:乙醛酸盐和二羧酸盐代谢;29:戊糖磷酸途径;30:丙酸代谢;31:丙酮酸代谢;32:淀粉和蔗糖代谢;33:光合生物中:碳固定;34:氧化磷酸化;35:光合作用;36:氨基酸生物合成;37:次级代谢生物合成;38:碳代谢;39:脂肪酸代谢;40:代谢途径;41:脂肪酸生物合成;42:脂肪酸降解;43:α-亚麻酸代谢;44:碳池;45:卟啉和叶绿素代谢;46:维生素B6代谢;47:谷胱甘肽代谢;48:嘌呤代谢;49:嘧啶代谢;50:植物-病原互作;51:精氨酸生物合成;52:烟酸和烟酰胺代谢;53:萜类骨架生物合成。
Figure 5. KEGG classifications of DEPs
A: 0 h vs. 36 h; B: 0 h vs. 48 h. 1: Endocytosis; 2: peroxisome; 3: phagosome; 4: proteasome; 5: protein export; 6: protein processing in endoplasmic reticulum; 7: RNA degradation; 8: ubiquitin mediated proteolysis; 9: nucleotide excision repair; 10: spliceosome; 11: aminoacyl-tRNA biosynthesis; 12: RNA transport; 13: ribosome; 14: ribosome biogenesis in eukaryotes; 15: mRNA surveillance pathway; 16: alanine, aspartate, and glutamate metabolism; 17: arginine and proline metabolism; 18: cysteine and methionine metabolism; 19: glycine, serine, and threonine metabolism; 20: phenylalanine metabolism; 21: phenylalanine, tyrosine, and tryptophan biosynthesis; 22: tyrosine metabolism; 23: phenylpropanoid biosynthesis; 24: amino sugar and nucleotide sugar metabolism; 25: citrate cycle (TCA cycle); 26: fructose and mannose metabolism; 27: glycolysis/gluconeogenesis; 28: glyoxylate and dicarboxylate metabolism; 29: pentose phosphate pathway; 30: propanoate metabolism; 31: pyruvate metabolism; 32: starch and sucrose metabolism; 33: carbon fixation in photosynthetic organisms; 34: oxidative phosphorylation; 35: photosynthesis; 36: biosynthesis of amino acids; 37: biosynthesis of secondary metabolites; 38: carbon metabolism; 39: fatty acid metabolism; 40: metabolic pathways; 41: fatty acid biosynthesis; 42: fatty acid degradation; 43: alpha-linolenic acid metabolism; 44: one carbon pool by folate; 45: porphyrin and chlorophyll metabolism; 46: vitamin B6 metabolism; 47: glutathione metabolism; 48: purine metabolism; 49: pyrimidine metabolism; 50: plant-pathogen interaction; 51: arginine biosynthesis; 52: nicotinate and nicotinamide metabolism; 53: terpenoid backbone biosynthesis.
表 1 差异表达蛋白质
Table 1 Differential expression proteins
差异蛋白
Differential expression protein差异蛋白数
The number of DEPs上调
Up-regulated下调
Down-regulated0 h vs. 12 h 0 0 0 0 h vs. 24 h 1 1 0 0 h vs. 36 h 848 385 463 0 h vs. 48 h 849 374 475 -
[1] 黄瑞, 夏华富, 代洪苇, 等. 茶树开花相关基因家族的克隆及CsMFT基因的可变剪切分析 [J]. 西北植物学报, 2021, 41(12):2002−2013. DOI: 10.7606/j.issn.1000-4025.2021.12.2002 HUANG R, XIA H F, DAI H W, et al. Cloning of flowering-related genes and alternative splicing analysis of CsMFT in tea plant [J]. Acta Botanica Boreali-Occidentalia Sinica, 2021, 41(12): 2002−2013. (in Chinese) DOI: 10.7606/j.issn.1000-4025.2021.12.2002
[2] 杨家干. 都匀毛尖成分及其部分生理功能研究[D]. 广州: 华南农业大学, 2016. YANG J G. Study on constituent and part of physiological function from DuyunMaojian [D]. Guangzhou: South China Agricultural University, 2016. (in Chinese)
[3] 邬子惠, 王梦馨, 潘铖, 等. 茶小绿叶蝉发生规律与绿色防控研究进展 [J]. 茶叶通讯, 2021, 48(2):200−206,252. DOI: 10.3969/j.issn.1009-525X.2021.02.002 WU Z H, WANG M X, PAN C, et al. Research progress and prospect of occurrence regularity and green control of tea green leafhopper [J]. Journal of Tea Communication, 2021, 48(2): 200−206,252. (in Chinese) DOI: 10.3969/j.issn.1009-525X.2021.02.002
[4] 李金玉, 王庆森, 李良德, 等. 茶小绿叶蝉种名变更及其种群发生与生物生态环境关系的研究进展 [J]. 福建农业学报, 2022, 37(1):123−130. LI J Y, WANG Q S, LI L D, et al. Research progress on the dominant species identification of tea green leafhopper and the relationship between its population and the biological and ecological environment [J]. Fujian Journal of Agricultural Sciences, 2022, 37(1): 123−130. (in Chinese)
[5] 潘杰. 茶树抗性相关蛋白(Cs-cystatin, Cs-Rip)对假眼小绿叶蝉消化道组织的影响[D]. 厦门: 厦门大学, 2014. PAN J. Toxic effects of resistance associated proteins (Cs-cystatin, Cs-Rip) of tea on empoasca vitis [D]. Xiamen: Xiamen University, 2014. (in Chinese)
[6] 杨会敏. 茶树抗假眼小绿叶蝉相关基因的克隆及表达研究[D]. 信阳: 信阳师范学院, 2010. YANG H M. Cloning and expression of anti-Empoasca vitis-related genes in tea [D]. Xinyang: Xinyang Normal University, 2010. (in Chinese)
[7] 王梦馨. 叶蝉诱导的茶树重要防御相关基因的功能解析和互利素鉴定应用[D]. 南京: 南京农业大学, 2012. WANG M X. Function analysis of defence-related genes of tea plant (Camellia Sinensis) and identification and application of its synomones induced by tea green leafhopper [D]. Nanjing: Nanjing Agricultural University, 2012. (in Chinese)
[8] 任倩倩. 抗、感茶树品种对茶小绿叶蝉取食诱导的防御反应[D]. 福州: 福建农林大学, 2020. REN Q Q. The defense strategies of resistant and susceptible tea cultivars in response to Empoasca onukii feeding [D]. Fuzhou: Fujian Agriculture and Forestry University, 2020. (in Chinese)
[9] MEI X, LIU X Y, ZHOU Y, et al. Formation and emission of linalool in tea (Camellia sinensis) leaves infested by tea green leafhopper (Empoasca (Matsumurasca) onukii Matsuda) [J]. Food Chemistry, 2017, 237: 356−363. DOI: 10.1016/j.foodchem.2017.05.124
[10] ZHAO X M, CHEN S, WANG S S, et al. Defensive responses of tea plants (Camellia sinensis) against tea green leafhopper attack: A multi-omics study [J]. Frontiers in Plant Science, 2019, 10: 1705.
[11] WASINGER V C, CORDWELL S J, CERPA-POLJAK A, et al. Progress with gene-product mapping of the Mollicutes: Mycoplasma genitalium [J]. Electrophoresis, 1995, 16(7): 1090−1094.
[12] 陈玲玲. 敖汉苜蓿小花与种子响应硼胁迫的蛋白质组学与代谢组学分析[D]. 北京: 中国农业大学, 2017. CHEN L L. Proteomic and metabolomics analysis of flowers and seeds of Medicago sativa L. cv. “Aohan” response to boron stress [D]. Beijing: China Agricultural University, 2017. (in Chinese)
[13] 程晓梅, 黄建安, 刘仲华, 等. 茶树蛋白质组学研究进展 [J]. 湖南农业科学, 2014(23):28−31. CHENG X M, HUANG J A, LIU Z H, et al. Research progress in tea proteomics [J]. Hunan Agricultural Sciences, 2014(23): 28−31. (in Chinese)
[14] 庄重光. 不同水分处理下铁观音茶树的生理机制及其差异蛋白质组学研究[D]. 福州: 福建农林大学, 2008. ZHUANG C G. A study on physiological mechanism and differential proteomics of tea (Camelllia sinensis (L. ) O. Kuntze) under different watering regimes [D]. Fuzhou: Fujian Agriculture and Forestry University, 2008. (in Chinese)
[15] 郭春芳. 水分胁迫下茶树的生理响应及其分子基础[D]. 福州: 福建农林大学, 2008. GUO C F. Physiological response and molecular basis of tea plant (Camellia sinensis) exposed to water stress [D]. Fuzhou: Fujian Agriculture and Forestry University, 2008. (in Chinese)
[16] LI J K, CHEN J, ZHANG Z H, et al. Proteome analysis of tea pollen (Camellia sinensis) under different storage conditions [J]. Journal of Agricultural and Food Chemistry, 2008, 56(16): 7535−7544. DOI: 10.1021/jf800885z
[17] CHIEN H J, YANG M M, WANG W C, et al. Proteomic analysis of “Oriental Beauty” oolong tea leaves with different degrees of leafhopper infestation [J]. Rapid Communications in Mass Spectrometry, 2020, 34(15): e8825. DOI: 10.1002/rcm.8825
[18] 邹瑶, 齐桂年, 陈盛相, 等. 蛋白质组学关键技术及其在茶树研究中的应用 [J]. 生物技术通报, 2012, 28(7):60−64. ZOU Y, QI G N, CHEN S X, et al. Key technology of proteomics and its application in tea plant [J]. Biotechnology Bulletin, 2012, 28(7): 60−64. (in Chinese)
[19] 周琼琼, 孙威江. 茶树总蛋白质提取方法及双向电泳体系的建立 [J]. 热带作物学报, 2014, 35(8):1517−1522. DOI: 10.3969/j.issn.1000-2561.2014.08.012 ZHOU Q Q, SUN W J. Establishment of extraction methods and two-dimensional electrophoresis conditions for proteomic analysis of Camellia sinensis [J]. Chinese Journal of Tropical Crops, 2014, 35(8): 1517−1522. (in Chinese) DOI: 10.3969/j.issn.1000-2561.2014.08.012
[20] HU Y G, LU Y Z, LU J. Comparative proteomics analysis of tea leaves exposed to subzero temperature: Molecular mechanism of freeze injury [J]. International Journal of Agricultural & Biological Engineering, 2013, 6(4): 27−34.
[21] XU Q S, WANG Y, DING Z T, et al. Aluminum induced physiological and proteomic responses in tea (Camellia sinensis) roots and leaves [J]. Plant Physiology and Biochemistry, 2017, 115: 141−151. DOI: 10.1016/j.plaphy.2017.03.017
[22] 吴致君. 茶树叶发育相关miRNA和转录因子挖掘及采后不同萎凋蛋白质组差异分析[D]. 南京: 南京农业大学, 2017. WU Z J. Discovery of leaf development-related miRNAs and transcription factors and analysis of the proteome differences of postharvest leaves under different treatments in tea plant (Camellia sinensis) [D]. Nanjing: Nanjing Agricultural University, 2017. (in Chinese)
[23] 任燕. 茶树雌蕊自交和杂交的差异蛋白质组学初步研究[D]. 南京: 南京农业大学, 2013. REN Y. Primary differential proteome analysis of self-and cross-pollinated pistils in tea plant (Camellia sinensis) [D]. Nanjing: Nanjing Agricultural University, 2013. (in Chinese)
[24] BAI B, TAN H, PAGALA V R, et al. Chapter twenty deep profiling of proteome and phosphoproteome by isobaric labeling, extensive liquid chromatography, and mass spectrometry [J]. Methods in Enzymology, 2017, 585: 377−395.
[25] TYERS M, MANN M. From genomics to proteomics [J]. Nature, 2003, 422(6928): 193−197. DOI: 10.1038/nature01510
[26] LI Z, ADAMS R M, CHOUREY K, et al. Systematic comparison of label-free, metabolic labeling, and isobaric chemical labeling for quantitative proteomics on LTQ Orbitrap Velos [J]. Journal of Proteome Research, 2012, 11(3): 1582−1590. DOI: 10.1021/pr200748h
[27] JIN S, REN Q Q, LIAN L L, et al. Comparative transcriptomic analysis of resistant and susceptible tea cultivars in response to Empoasca onukii (Matsuda) damage [J]. Planta, 2020, 252(1): 10. DOI: 10.1007/s00425-020-03407-0
[28] 陈升龙. 诱导茶树抗茶小绿叶蝉挥发物筛选体系的建立及反式: 橙花叔醇诱抗机制初探[D]. 北京: 中国农业科学院, 2020 CHEN S L. Establishment of screening system for volatiles that induces tea plant defense against tea green leafhopper and preliminary study on (E)-nerolidol induction mechanism [D]. Beijing: Chinese Academy of Agricultural Sciences, 2020. (in Chinese)
[29] 梅瑜, 王继华, 蔡时可, 等. 金线莲应答高温胁迫的蛋白质组学分析 [J]. 江苏农业学报, 2020, 36(6):1389−1397. DOI: 10.3969/j.issn.1000-4440.2020.06.006 MEI Y, WANG J H, CAI S K, et al. Proteomics analysis on Anoectochilus roxburghii in response to high temperature stress [J]. Jiangsu Journal of Agricultural Sciences, 2020, 36(6): 1389−1397. (in Chinese) DOI: 10.3969/j.issn.1000-4440.2020.06.006
[30] 袁清华. 茶树“信阳10号”生态休眠不同阶段的蛋白质组学研究[D]. 信阳: 信阳师范学院, 2020. YUAN Q H. Proteomics research of ecodormancy of tea plant variety ‘Xinyang 10’ [D]. Xinyang: Xinyang Normal University, 2020. (in Chinese)
[31] YANG Y X, AHAMMED G J, WU C J, et al. Crosstalk among jasmonate, salicylate and ethylene signaling pathways in plant disease and immune responses [J]. Current Protein & Peptide Science, 2015, 16(5): 450−461.
[32] 李新岗, 刘惠霞, 黄建. 虫害诱导植物防御的分子机理研究进展 [J]. 应用生态学报, 2008, 19(4):893−900. LI X G, LIU H X, HUANG J. Molecular mechanisms of insect pests-induced plant defense [J]. Chinese Journal of Applied Ecology, 2008, 19(4): 893−900. (in Chinese)
[33] BLOCK A K, VAUGHAN M M, SCHMELZ E A, et al. Biosynthesis and function of terpenoid defense compounds in maize (Zea mays) [J]. Planta, 2019, 249(1): 21−30. DOI: 10.1007/s00425-018-2999-2
[34] NINKUU V, ZHANG L, YAN J P, et al. Biochemistry of terpenes and recent advances in plant protection [J]. International Journal of Molecular Sciences, 2021, 22(11): 5710. DOI: 10.3390/ijms22115710





 下载:
下载: