Metabolomics of Mulberry Fruits at Developmental Stages
-
摘要:目的
研究桑葚果实发育过程中的代谢组分变化规律。
方法以桑葚品种粤椹大十绿果期、转色期和成熟期的果实为样本材料,进行广泛靶向代谢组学分析,并基于差异富集代谢物(Differentially accumulated metabolites, DAMs)进行KEGG代谢途径富集分析。
结果从粤椹大十3个时期果实样本中检测到
1146 种代谢组分,以P<0.05且VIP>1.0为标准,其中483种代谢物被鉴定为DAMs,包括51种积累水平在整个果实发育过程中均显著差异的DAMs。2种类黄酮和1种花色苷在桑葚发育过程中显著提高。基于DAMs进行KEGG分析表明,α-亚麻酸代谢和亚油酸代谢在绿果期发育到转色期过程中显著富集,抗坏血酸和藻酸盐代谢在转色期发育到成熟期过程中显著富集,而亚油酸代谢和角质/木栓和蜡生物合成在整个果实发育过程中显著富集。进一步分析发现,尽管粤椹大十桑葚果实发育过程中包含6种上调积累和1种下调积累的亚油酸代谢组分,但从整体上看亚油酸积累水平呈下降趋势。结论51种DAMs可能持续参与桑葚果实整个发育过程,其中花色苷与类黄酮显著提高,亚油酸代谢途径中的7种关键代谢组分可能影响其品质风味形成。研究结果有助于更好地了解桑葚成熟过程中营养成分的动态变化规律,为揭示桑葚果实品质风味形成机制和选育优质桑葚种质奠定基础,同时也为桑葚采摘期的判定提供科学依据。
Abstract:ObjectiveChanges in metabolic substances at various developmental stages of mulberry fruits were studied.
MethodsA widely targeted metabolomic analysis was conducted on Morus alba cv. yueshen dashi fruits sampled at the stages of green fruit, color transition, and maturation. KEGG metabolic pathway enrichment was analyzed based on the differentially accumulated metabolites (DAMs).
ResultsA total of 1 146 metabolic substances were identified from the specimens at the fruit developmental stages. At P<0.05 and VIP>1.0, 483 metabolites were identified as DAMs, 51 DAMs showed significant differences in the accumulation throughout the whole fruit development process. The contents of two flavonoids and one anthocyanin increased significantly during the developmental stages. The DAMs based on the KEGG metabolic pathway analysis indicated α-linolenic acid and linoleic acid metabolisms to be significantly enriched from the green to the colored stage, while ascorbate and aldarate metabolisms significantly enhanced from the color transition period to maturity, whereas linoleic acid metabolism as well as cutin, suberine, and wax biosynthesis significantly augmented throughout the entire development process. Although there were 6 up-accumulated and one down-accumulated linoleic acid, overall, the accumulation was on a downward trend as the fruits developed.
ConclusionsThere were 51 DAMs that might involve in the mulberry fruit development. It was found that anthocyanins and flavonoids rose significantly and 7 key metabolic components in the linoleic acid metabolism pathway might affect the quality and flavor of the fruits as well. The research results contributed a better understanding of the dynamic change in the nutritional composition of ripening mulberries, laying the foundation for revealing the mechanism of quality and flavor formation and breeding high-quality germplasm. At the same time, it also provided a scientific basis for determining the optimal fruit picking time.
-
Keywords:
- Mulberry /
- fruit development /
- metabolomics /
- KEGG metabolic pathway /
- linoleic acid
-
0. 引言
【研究意义】桑葚(Morus alba)为桑科桑属植物,原产于我国,其栽培历史悠久,分布区域广泛。桑葚具有很高的营养价值和药用价值,富含类黄酮、花青素、生物碱、白藜芦醇、多糖等多种功能活性成分,具有增强免疫力、抗衰老、降血糖、促进造血细胞生长等药理作用[1]。此外,桑葚籽中富含油酸、亚油酸、亚麻酸等不饱和脂肪酸,尤其是亚油酸含量高达69.55%,是最主要的脂肪酸之一[2]。据《本草纲目》记载,桑葚具有解酒毒、消肿、滋阴补血等功效。1993年,桑葚被国家卫生部列入首批“药食两用资源”名录。目前,粤椹大十、长果桑、白玉王等一批桑葚品种的成功选育,为桑葚的推广和栽培奠定了良好的基础,其中粤椹大十是我国第一个通过审定的桑葚品种,也是我国种植面积最大的桑葚品种之一[3]。而桑葚果实的发育好坏对品质风味的形成具有重要影响,对桑葚果实成熟过程中营养成分动态变化的研究可为其品质形成提供研究基础。【前人研究进展】张若彤等[4]发现中性转化酶(Neutral invertase, NINV)、己糖激酶(Hexokinase, HK)、柠檬酸合酶(Citrate synthase, CS)、乌头酸水合酶(Aconitate hydratase, ACO)、苹果酸脱氢酶(Malate dehydrogenase, MDH)和异柠檬酸脱氢酶(Isocitrate dehydrogenase, ICDH)基因在桑葚成熟过程中通过调控可溶性糖和有机酸的合成和代谢,潜在影响桑葚口感变化。孙志超等[5]研究了桑葚果实发育过程中硬度、可溶性固形物、可滴定酸、总黄酮、总酚含量以及糖代谢相关基因的变化。而代谢组学具有高通量、广覆盖、高精度等优点,是研究生物样本内源性代谢物质变化的有效工具,已被广泛应用于果实发育过程相关研究。基于代谢组学技术,刘淑桢等[6]检测了温州蜜柑果实绿熟期、转色期和完熟期的极性代谢物,并找到了评价果实成熟度的指标代谢物,而糖类和有机酸类物质在果实成熟过程中剧烈变化并表现出很强的组织特异性。Wang等[7]发现纽荷尔脐橙果实发育过程中,角质层积累与果实膨大同步,蜡质合成与果实成熟同步,而脱落酸能够调控蜡质的生物合成。王乐飞等[8]阐明了枣果实发育过程中果皮颜色和类黄酮的内在关系。郭荣琨等[9]揭示了花青素和类胡萝卜素的差异性积累是造成不同类型山楂果皮颜色差异的关键因素。可见,代谢组学对于揭示果实发育过程的物质变化具有重要意义。目前,刘晴晴等[10]利用代谢组学分析紫色桑葚和白色桑葚的代谢图谱差异,发现了类黄酮、花色苷、酚酸、氨基酸、核苷酸、糖类、脂类等在内的136种差异代谢物。【本研究切入点】桑葚果实发育过程中的相关研究均集中在糖和酸的合成和代谢,其中代谢物质的整体动态变化尚不明确,目前代谢组学在桑葚中的相关研究较少。【拟解决的关键问题】为进一步研究桑葚果实发育过程中的代谢物质的富集规律,本研究以福建省主栽的紫果桑葚品种粤椹大十果实为材料,采用代谢组学检测了果实发育早、中、后期的绿果期、转色期和成熟期的代谢组分差异,以期为揭示桑葚果实发育和品质风味形成机制奠定科学基础。
1. 材料与方法
1.1 试验材料
供试粤椹大十品种桑葚果实取自福建省农业科学院果树研究所试验基地(119°19′57′′E、26°7′46′′N)。于2024年4月分别采集桑葚绿果期、转色期、成熟期样品(图1),即桑葚果实不同发育期每株树随机取20个果实,重复取样3株树。果实带回实验室后,用蒸馏水洗净,滤纸擦干后采用液氮速冻,置于−80 ℃超低温冰箱中保存备用。
1.2 试验方法
1.2.1 样品制备
称取桑葚果肉样本0.2 g于离心管中,加入0.6 mL 4 mg·L−1的2-氯苯丙氨酸,涡旋振荡30 s。随后,加入100 mg玻璃珠,放入组织研磨器(SCIENTZ-48,宁波新芝,中国)中,60 Hz研磨90 s,置于室温条件下超声15 min。
12000 r·min−1、4 ℃离心10 min,取300 μL上清液过0.22 μm膜过滤,滤液加入到检测瓶中备用。每个待测样本各取20 μL混合成质控(Quality control, QC)样本。将待测样本和QC样本进行液相色谱串联质谱(Liquid chromatography-mass spectrometry, LC-MS)检测。1.2.2 LC-MS检测
参照Lai等[11]设置的质谱和色谱条件参数进行桑葚果实LC-MS检测。采用Proteowizard v3.0.8789中的MSConvert模块将原始质谱下机文件转换为mzXML文件格式,采用R XCMS v3.12.0进行峰检测、峰过滤、峰对齐处理,得到代谢物定量列表。采用公共数据库HMDB[12]、MassBank[13]、Knapsack、ReSpect、LipidMaps[14]、KEGG[15]及诺米代谢标准品(PANOMIX,Suzhou,CHN)等物质库,基于一级分子量、保留时间、谱图与数据库进行代谢物定性。
1.2.3 数据分析
采用Ropls进行主成分分析、偏最小二乘判别分析、正交偏最小二乘判别分析(Orthogonal partial least squares discriminant analysis, OPLS-DA)降维分析。采用统计检验计算P值,同时通过OPLS-DA降维方法计算变量投影重要度(Variable importance in projection, VIP),差异倍数(Fold change, FC)计算组间差异倍数,以P< 0.05和VIP> 1.0为标准筛选样本间的差异富集代谢物(Differentially accumulated metabolites, DAMs)。采用MetaboAnalyst对差异代谢物进行京都基因与基因组百科全书(Kyoto encyclopedia of genes and genomes, KEGG)代谢通路富集分析。
2. 结果与分析
2.1 质量控制
桑葚果实不同发育时期的基峰色谱图结果如图2A和图2B所示,在正、负离子模式下,同一样品的峰信号类似,保留时间和峰响应强度波动很小,表明仪器在整个样品检测过程中状态良好、信号稳定。进一步进行样本PCA分析,发现同一发育阶段的生物学重复样品均较好地聚集在一起,表明每组样品的数据重复性良好,可用于后续分析。
2.2 整体代谢物质检测
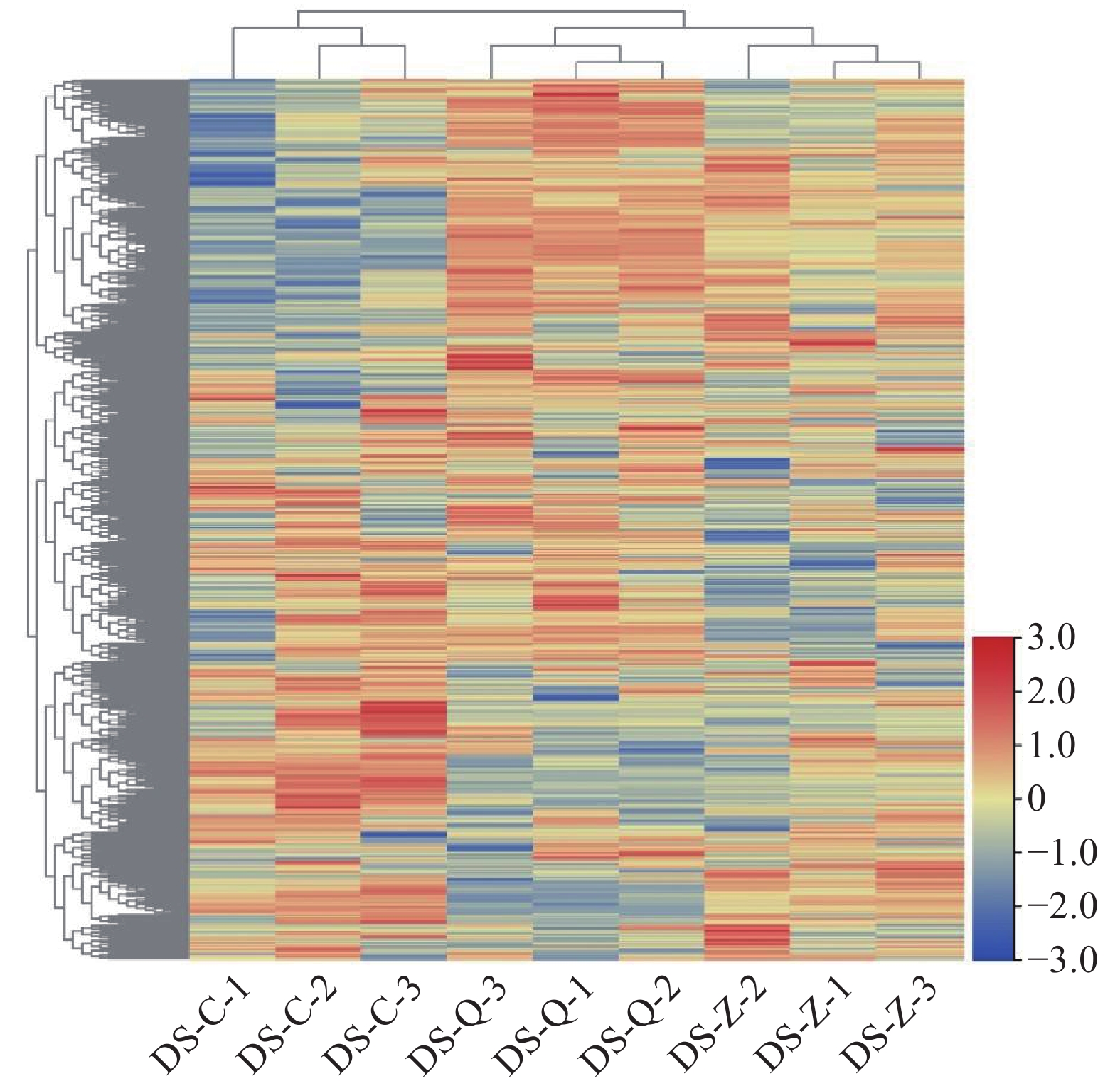
基于代谢组学从桑葚3个发育时期样本中共检测到
1146 种代谢组分(图3),不同发育阶段的生物学重复样本之间的代谢组分组成较为一致。与成熟期相比,绿果期与转色期的相似度更高,结果与实际相符合。根据这些代谢组分在桑葚不同发育时期的积累水平,可以分为3类,第一类主要在绿果期富集,其次是转色期,随着果实的发育,其积累水平逐渐降低;第二类主要在绿果期和成熟期富集,在转色期中的积累水平较低;第三类在绿果期中的积累水平最低,随着果实发育逐渐上升,并在成熟期大量富集。这些代谢组分在不同阶段差异性富集,可能与桑葚果实发育调控密切相关。2.3 差异富集代谢物鉴定
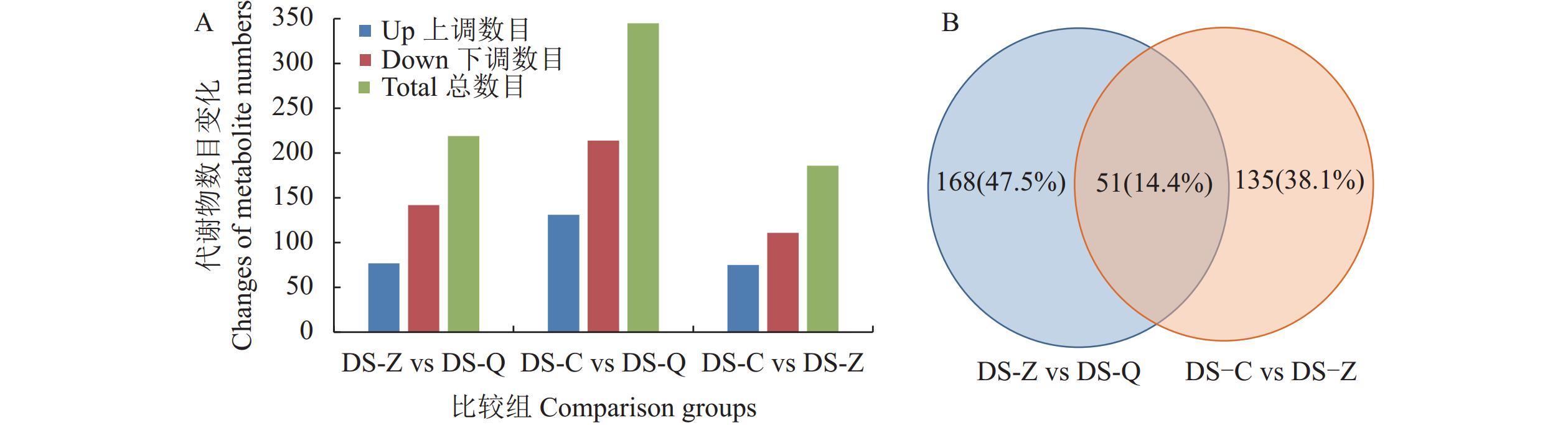
以P<0.05且VIP>1.0为标准,共鉴定获得桑葚果实发育过程中483种DAMs,包括脂肪酸、类黄酮、酚酸、萜类、氨基酸、有机酸、糖类、生物碱等多个类别,可见这些类别代谢物可能是桑葚营养价值与风味形成的来源物质。对不同发育时期代谢组分进行比较,结果如图4所示。与绿果期样本相比,转色期和成熟期样本分别鉴定到219种和345种DAMs,其中上调的DAMs分别为77种和131种,下调的DAMs分别为142种和214种;与转色期样本相比,成熟期样本分别有75种上调和111种下调的DAMs。从结果上看,随着桑葚果实的发育,积累水平下调的代谢组分明显多于上调的代谢组分(图4A)。从韦恩图上看,168种代谢组分在桑葚果实从绿果期发育到转色期过程中特异性变化,135种代谢物在转色期发育到成熟期过程中显著变化(图4B)。值得注意的是,51种代谢组分在这2个阶段均同时显著变化,说明这些代谢物质可能持续参与桑葚果实发育过程。此外,值得注意的是,与绿果期样本相比,转色期样本中检测到2种重要代谢组分显著上调了100倍以上,即矢车菊素-3-槐糖苷(201.98倍)、3-O-β-(6-反式咖啡酰基)-吡喃半乳糖基槲皮素(113.08倍);成熟期样本中检测到3种重要代谢组分显著提高了800倍以上,即3-O-β-(6-反式咖啡酰基)-吡喃半乳糖基槲皮素(
1306.57 倍)、矢车菊素-3-槐糖苷(983.72倍)、3,4,5,7-四羟基黄酮(898.99倍);与转色期样本相比,成熟期样本中检测到1种关键代谢组分显著提高了200倍以上,即SCHEMBL12391563(209.46倍)。可见,桑葚果实成熟过程中,花青素和类黄酮组分显著变化。2.4 基于DAMs的KEGG代谢途径富集分析
在桑葚果实发育早期,与绿果期样本相比,转色期样本DAMs共富集到59条KEGG代谢途径,根据P值大小排序,前 20条KEGG代谢途径包括α-亚麻酸代谢,亚油酸代谢,苯丙氨酸代谢,谷胱甘肽代谢,缬氨酸、亮氨酸和异亮氨酸生物合成,精氨酸生物合成,肌醇磷酸代谢,氨酰基tRNA生物合成,泛酸和辅酶A生物合成,花生四烯酸代谢,赖氨酸降解,苯丙素生物合成,戊糖和葡萄糖醛酸相互转化,C5支链二元酸代谢,ABC转运蛋白、D-氨基酸代谢,精氨和脯氨酸代谢,缬氨酸/亮氨酸和异亮氨酸降解,莨菪烷、哌啶和吡啶生物碱生物合成,胞吐作用(图5A)。其中,α-亚麻酸代谢(P=3.61
× 10−3)和亚油酸代谢(P=1.46×10−2)在这一过程中显著富集(P<0.05),可能与桑葚果实早期发育过程密切相关。在桑葚果实发育后期,与转色期样本相比,成熟期样本的DAMs共富集到63条KEGG代谢途径,以P值为排序依据,富集的前20条代谢途径包括抗坏血酸和藻酸盐代谢,精氨酸和脯氨酸代谢,光合生物中的固碳,苯丙氨酸代谢,黄酮和黄酮醇生物合成,角质/木栓和蜡生物合成,泛酸和辅酶A生物合成,糖酵解/糖异生,乙醛酸酸和二羧酸代谢,C5支链二元酸代谢,戊糖磷酸途径,植物激素信号转导,黄酮生物合成,脂肪酸代谢,α-亚麻酸代谢,萜类骨架生物合成,甘氨酸、丝氨酸和苏氨酸代谢,氧化磷酸化,果糖和甘露糖代谢,柠檬酸循环(图5B)。值得注意的是,抗坏血酸和藻酸盐代谢(P=4.39×10−2)在这一过程中显著富集(P<0.05),说明抗坏血酸可能在桑葚果实发育后期发生明显变化。
在整个果实发育过程中,与绿果期样本相比,成熟期样本的DAMs共富集到71条KEGG代谢途径,以P值为排序依据,富集的前20条KEGG代谢途径分别为亚油酸代谢、角质/木栓和蜡生物合成、植物激素信号转导、抗坏血酸和藻酸盐代谢、泛酸和辅酶A生物合成、苯丙氨酸代谢、精氨酸和脯氨酸代谢、柠檬酸循环、光合生物的固碳作用、内酰胺生物合成、缬氨酸/亮氨酸和异亮氨酸生物合成、乙醛酸和二羧酸代谢、嘧啶代谢、萜类骨架生物合成、半乳糖代谢、丙氨酸/天冬氨酸和谷氨酸代谢、组氨酸代谢、糖酵解/糖异生、黄酮和黄酮醇生物合成、氨酰基tRNA生物合成。其中,亚油酸代谢(P=1.98×10−3)和角质/木栓和蜡生物合成(P=4.09×10−2)在果实发育整个过程中显著富集(P<0.05)。
值得注意的是,43条KEGG代谢途径在DS-Z vs DS-Q、DS-C vs DS-Z和DS-C vs DS-Q比较组中均有富集,说明这些代谢途径参与桑葚果实发育整个过程。其中,亚油酸代谢在DS-Z vs DS-Q和DS-C vs DS-Q中均有显著富集,说明亚油酸可能在果实发育过程中显著变化。
2.5 亚油酸代谢途径变化分析
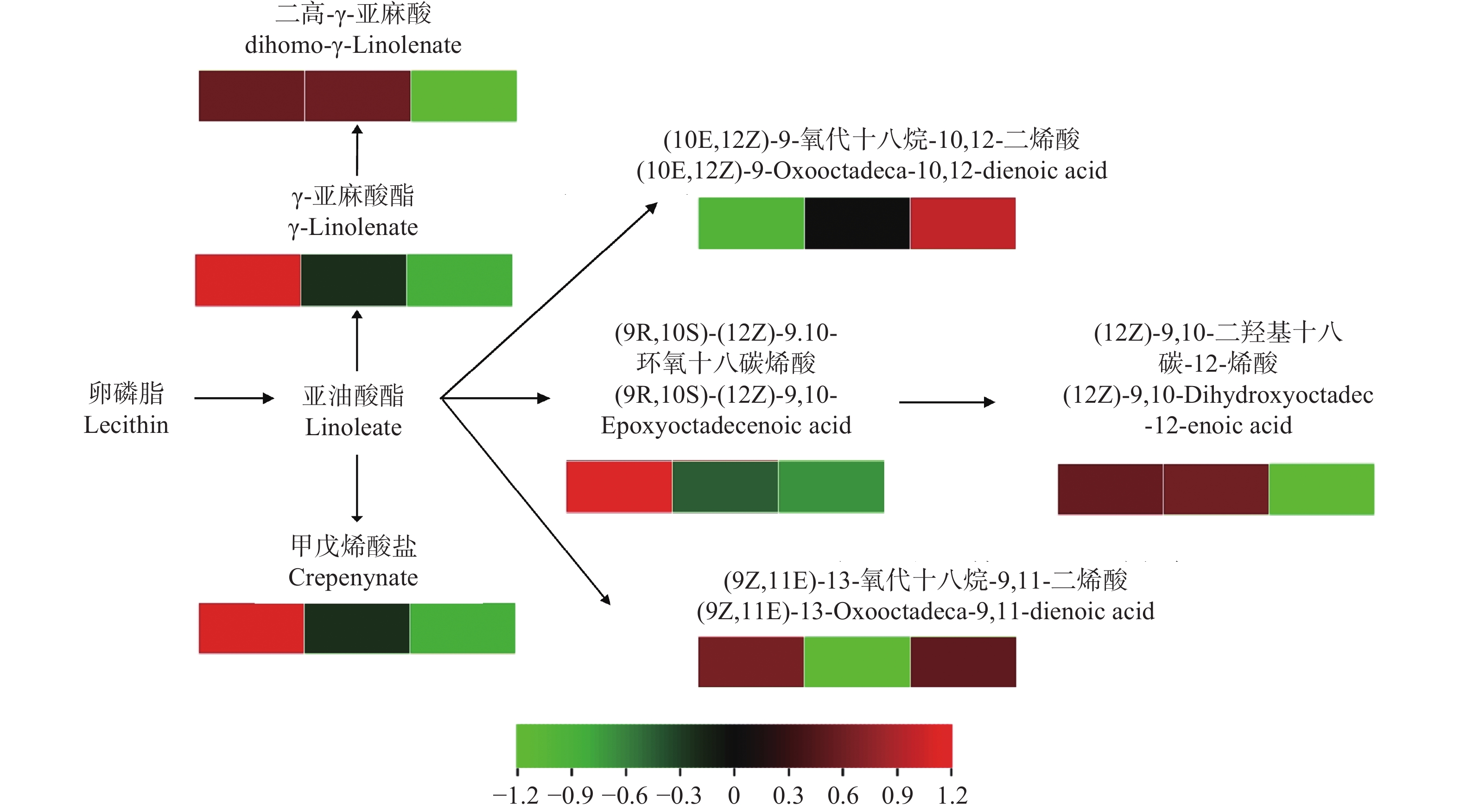
基于桑葚果实不同发育时期代谢组学发现,亚油酸代谢途径在这一过程中显著富集。进一步分析表明在这一代谢途径中,共发现6种下调积累和1种上调积累的代谢组分(图6)。从整体上看,随着桑葚果实的发育,亚油酸的积累水平呈下降趋势。
![]() 图 6 桑葚果实发育过程中亚油酸代谢途径变化红色表示该代谢物在对应样本中上调积累,绿色表示下调积累。从左往右对应的3种样本分别为绿果期、转色期和成熟期的桑葚果实。图例颜色从红到绿,表示log10(FPKM)值从大到小。Figure 6. Changes in linoleic acid metabolism pathway in mulberry fruit developmentRed indicates up-accumulation and green down-accumulation of metabolite in corresponding sample. Three corresponding samples from left to right are of mulberry fruits at green fruit, color transition, and maturation stages.
图 6 桑葚果实发育过程中亚油酸代谢途径变化红色表示该代谢物在对应样本中上调积累,绿色表示下调积累。从左往右对应的3种样本分别为绿果期、转色期和成熟期的桑葚果实。图例颜色从红到绿,表示log10(FPKM)值从大到小。Figure 6. Changes in linoleic acid metabolism pathway in mulberry fruit developmentRed indicates up-accumulation and green down-accumulation of metabolite in corresponding sample. Three corresponding samples from left to right are of mulberry fruits at green fruit, color transition, and maturation stages.3. 讨论与结论
本研究采用代谢组学从不同发育时期的桑葚中总共鉴定到483种差异富集的代谢组分,广泛涉及脂肪酸、类黄酮、酚酸、萜类、氨基酸、有机酸、糖类、生物碱等,说明这些组分在桑葚果实发育过程中发生明显变化,可能影响桑葚果实的品质风味。在已有报道中,代谢组学可为黄芩(Scutellaria baicalensis Georgi)[16]、结香花(Edgeworthia chrysantha Lindl.)[17]、卷柏(Selaginella tamariscina (Beauv.) Spring)[18]等采收评价指标确定提供依据。可见,采用代谢组学可有效鉴定桑葚中的代谢组分,为桑葚果实成熟和采收提供依据,在后续研究中可进一步增加样本群体,开发可有效应用于桑葚果实采摘时期判断的标志物。
基于代谢组学研究表明,许多代谢途径持续参与桑葚果实早期、中期和后期的发育过程,但每个发育阶段涉及的主要生物学过程又有所差异。已有研究表明,桑葚果实发育过程中可溶性糖和有机酸的合成和代谢的变化,潜在影响桑葚口感变化[4]。本研究利用代谢组学也发现了桑葚果实发育过程中15种差异积累的有机酸,以及6种显著变化的糖类,这种糖酸转化最终影响桑葚果实的品质风味。相关研究表明,桑葚果实中类黄酮和花青素含量整体上与果实成熟度具有正相关性[19−20],同时桑葚的抗氧化活性与其总黄酮的含量呈正相关[10,21]。本研究发现桑葚果实由绿果期发育到转色期和成熟期时,矢车菊素-3-槐糖苷、3-O-β-(6-反式咖啡酰基)-吡喃半乳糖基槲皮素、3,4,5,7-四羟基黄酮等花色苷和类黄酮显著提高。结果表明花色苷与类黄酮的显著变化可能与紫果桑葚品种成熟密切相关,并可能是其具有良好抗氧化特性的原因之一。植物类黄酮生物合成是花青素生物合成的上游途径,桑葚果实发育过程中由绿色转变为紫红色最后形成紫黑色,类黄酮组分和花色苷含量上调积累在紫果桑葚色泽形成过程中发挥重要作用。值得注意的是,矢车菊素衍生物在整个发育过程中均显著上调,矢车菊素可能是紫果桑葚的主要色素成分。已有研究表明,桑葚含量最高的是矢车菊素,锦葵色素含量较少,飞叶草素、矮牵牛素和芍药色素含量较低[22],与本研究结果类似,进一步说明矢车菊素是形成桑葚果实色泽的重要成分。
此外,本研究发现α-亚麻酸代谢和亚油酸代谢在果实早期发育到中期过程中显著富集,抗坏血酸和藻酸盐代谢在果实中期到成熟过程中显著富集。值得注意的是,亚油酸代谢在整个果实发育过程中也显著富集,而这一过程中大部分亚油酸组分的积累水平均为下调,预测亚油酸可能主要参与桑葚果实早期发育过程。此外,亚油酸在桑葚果实成熟过程呈负相关,而研究表明亚油酸是桑葚果实中最主要的脂肪酸组分之一[2]。研究结果也为后续高不饱和脂肪酸果实的采摘提供了新思路。
综上所述,桑葚果实发育过程中,脂肪酸、类黄酮、酚酸、萜类、氨基酸、有机酸、糖类、生物碱等代谢组分显著变化,这一过程中糖酸转化潜在影响果实品质风味,类黄酮和花色苷积累影响果实着色,亚油酸可能参与果实早期发育过程。此外,代谢组学可有效检测桑葚果实中代谢物质的变化,为桑葚果实发育调控和采收指标确定提供依据。
-
图 6 桑葚果实发育过程中亚油酸代谢途径变化
红色表示该代谢物在对应样本中上调积累,绿色表示下调积累。从左往右对应的3种样本分别为绿果期、转色期和成熟期的桑葚果实。图例颜色从红到绿,表示log10(FPKM)值从大到小。
Figure 6. Changes in linoleic acid metabolism pathway in mulberry fruit development
Red indicates up-accumulation and green down-accumulation of metabolite in corresponding sample. Three corresponding samples from left to right are of mulberry fruits at green fruit, color transition, and maturation stages.
-
[1] BATIHA G E S, AL-SNAFI A E, THUWAINI M M, et al. Morus alba: A comprehensive phytochemical and pharmacological review [J]. Naunyn-Schmiedeberg’s Archives of Pharmacology, 2023, 396(7): 1399−1413. DOI: 10.1007/s00210-023-02434-4
[2] 刘玮, 陈亮, 吴志明, 等. 3种不同产地桑葚籽油的脂肪酸成分分析 [J]. 食品研究与开发, 2015, 36(20):13−16. DOI: 10.3969/j.issn.1005-6521.2015.20.004 LIU W, CHEN L, WU Z M, et al. Analysis of fatty acid compositions of mulberry seed oil in three different regions [J]. Food Research and Development, 2015, 36(20): 13−16. (in Chinese) DOI: 10.3969/j.issn.1005-6521.2015.20.004
[3] 吴剑安, 唐翠明, 罗国庆, 等. 果桑品种“粤椹大10” 苗木快速高效繁育技术 [J]. 广东蚕业, 2006, 40(2):12−14. WU J A, TANG C M, LUO G Q, et al. Speediness and high efficiency multiplication technique of fruit mulberry variety \ “Yue Shen Da 10\” [J]. Guangdong Sericulture, 2006, 40(2): 12−14. (in Chinese)
[4] 张若彤, 李蒙, 齐一鸣, 等. 转录组和代谢组联合分析桑葚发育过程中可溶性糖和有机酸代谢的变化 [J]. 果树学报, 2024, 41(4):690−702. ZHANG R T, LI M, QI Y M, et al. Transcriptome and metabolome combined analysis metabolism change of soluble sugars and organic acids in mulberry fruit during development stages [J]. Journal of Fruit Science, 2024, 41(4): 690−702. (in Chinese)
[5] 孙志超, 郭新淼, 李蒙, 等. 2个桑树品种果实不同发育时期营养物质的变化 [J]. 果树学报, 2024, 41(4):703−711. SUN Z C, GUO X M, LI M, et al. Nutrientional compound changes in fruits of 2 mulberries(Morus alba)varieties at different development stages [J]. Journal of Fruit Science, 2024, 41(4): 703−711. (in Chinese)
[6] 刘淑桢, 韩静雯, 云泽, 等. 国庆1号温州蜜柑果实成熟过程中极性代谢物的变化 [J]. 中国农业科学, 2012, 45(21):4437−4446. DOI: 10.3864/j.issn.0578-1752.2012.21.012 LIU S Z, HAN J W, YUN Z, et al. Changes of polar metabolites in guoqing No. 1 Satsuma mandarine during fruit ripening [J]. Scientia Agricultura Sinica, 2012, 45(21): 4437−4446. (in Chinese) DOI: 10.3864/j.issn.0578-1752.2012.21.012
[7] WANG J Q, SUN L, XIE L, et al. Regulation of cuticle formation during fruit development and ripening in ‘Newhall’ navel orange (Citrus sinensis Osbeck) revealed by transcriptomic and metabolomic profiling [J]. Plant Science, 2016, 243: 131−144. DOI: 10.1016/j.plantsci.2015.12.010
[8] 王乐飞, 古绍彬, 吴影. 基于UPLC-MS代谢组学技术的枣果皮黄酮类化合物分析 [J]. 食品科学, 2020, 41(24):155−161. DOI: 10.7506/spkx1002-6630-20191018-195 WANG L F, GU S B, WU Y. Analysis of flavonoids in fruit of jujube(Ziziphus jujuba)by UPLC-MS-based metabonomics [J]. Food Science, 2020, 41(24): 155−161. (in Chinese) DOI: 10.7506/spkx1002-6630-20191018-195
[9] 郭荣琨, 董宁光, 农惠兰, 等. 基于靶向代谢组学的山楂黄色和红色果皮呈色物质差异分析 [J]. 中国农业科学, 2024, 57(12):2439−2453. DOI: 10.3864/j.issn.0578-1752.2024.12.013 GUO R K, DONG N G, NONG H L, et al. Targeted metabolomics-based analysis of peel color differences between yellow and red hawthorn [J]. Scientia Agricultura Sinica, 2024, 57(12): 2439−2453. (in Chinese) DOI: 10.3864/j.issn.0578-1752.2024.12.013
[10] 刘晴晴, 李勇, 张明霞, 等. 紫色桑葚和白色桑葚总酚含量、抗氧化能力及代谢指纹图谱差异分析 [J]. 江苏农业学报, 2022, 38(3):813−820. DOI: 10.3969/j.issn.1000-4440.2022.03.029 LIU Q Q, LI Y, ZHANG M X, et al. Differences in total phenol content, antioxidant activity and metabolic fin-gerprint between purple mulberry and white mulberry [J]. Jiangsu Journal of Agricultural Sciences, 2022, 38(3): 813−820. (in Chinese) DOI: 10.3969/j.issn.1000-4440.2022.03.029
[11] LAI R L, SHEN C G, FENG X, et al. Integrated metabolomic and transcriptomic analysis reveals differential flavonoid accumulation and its underlying mechanism in fruits of distinct Canarium album cultivars [J]. Foods, 2022, 11(16): 2527. DOI: 10.3390/foods11162527
[12] WISHART D S, TZUR D, KNOX C, et al. HMDB: The human metabolome database[J]. Nucleic Acids Research, 2007, 35(Database issue): D521-D526.
[13] HORAI H, ARITA M, KANAYA S, et al. MassBank: A public repository for sharing mass spectral data for life sciences [J]. Journal of Mass Spectrometry, 2010, 45(7): 703−714. DOI: 10.1002/jms.1777
[14] SUD M, FAHY E, COTTER D, et al. LMSD: LIPID MAPS structure database[J]. Nucleic Acids Research, 2007, 35(Database issue): D527-D532.
[15] OGATA H, GOTO S, SATO K, et al. KEGG Kyoto encyclopedia of genes and genomes [J]. Nucleic Acids Research, 1999, 27(1): 29−34. DOI: 10.1093/nar/27.1.29
[16] 庞溢媛, 薛立英, 郑艳红, 等. 基于UHPLC-MS/MS代谢组学技术的不同采收期黄芩质量比较研究 [J]. 药学学报, 2017, 52(12):1903−1909. PANG Y Y, XUE L Y, ZHENG Y H, et al. Comparative study on quality of Scutellaria baicalensis Georgi in different harvest periods using UHPLC-MS/MS metabolomics technology [J]. Acta Pharmaceutica Sinica, 2017, 52(12): 1903−1909. (in Chinese)
[17] 秦亚东, 汪荣斌, 李林华, 等. 基于GC-TOF-MS非靶向代谢组学结香花不同花期代谢差异的研究 [J]. 现代中药研究与实践, 2022, 36(3):20−24. QIN Y D, WANG R B, LI L H, et al. Metabolic differences in the flower of Edgeworthia chrysantha lindl. from different flowering periods based on untargeted metabolomics using GC-TOF-MS approach [J]. Research and Practice on Chinese Medicines, 2022, 36(3): 20−24. (in Chinese)
[18] 席彩彩, 谷巍, 周晨, 等. 基于GC-TOF/MS的卷柏不同生长阶段代谢组学研究 [J]. 中成药, 2021, 43(12):3542−3547. DOI: 10.3969/j.issn.1001-1528.2021.12.056 XI C C, GU W, ZHOU C, et al. GC-TOF/MS-based metabolomics study of Selaginella in different growth stages [J]. Chinese Traditional Patent Medicine, 2021, 43(12): 3542−3547. (in Chinese) DOI: 10.3969/j.issn.1001-1528.2021.12.056
[19] 石丽雯, 陆柳印, 王娜, 等. 不同成熟度桑葚的品质分析 [J]. 经济林研究, 2024, 42(2):282−292. SHI L W, LU L Y, WANG N, et al. Quality analysis of mulberries with different maturity levels [J]. Non-wood Forest Research, 2024, 42(2): 282−292. (in Chinese)
[20] BIAN M H, FANG Y L, YUAN T M, et al. Dynamics of microbial community structure and metabolites during mulberry ripening [J]. Agriculture, 2024, 14(7): 1129. DOI: 10.3390/agriculture14071129
[21] 贺诗茹. 新疆桑葚主要植物化学物含量测定及抗氧化活性的研究[D]. 乌鲁木齐: 新疆医科大学, 2023 HE S R. Determination of main phytochemicals in Xinjiang mulberries and study on antioxidant activities[D]. Urumqi: Xinjiang Medical University, 2023. (in Chinese)
[22] 王振江, 肖更生, 刘学铭, 等. 桑椹花青素的研究进展 [J]. 蚕业科学, 2006, 32(1):90−94. DOI: 10.3969/j.issn.0257-4799.2006.01.016 WANG Z J, XIAO G S, LIU X M, et al. Research and application of mulberry anthocyanins [J]. Science of Sericulture, 2006, 32(1): 90−94. (in Chinese) DOI: 10.3969/j.issn.0257-4799.2006.01.016





 下载:
下载: