Distribution and Properties of SSR in Transcriptome of Nymphaea Paul Stetson Flowers
-
摘要:目的 通过解析保罗蓝睡莲花转录组数据的SSR位点特征信息,开发新的与表型相关的SSR标记,为睡莲种质资源评价、新品种选育提供科学依据。方法 以热带睡莲保罗蓝不同花器官部位(雌蕊、雄蕊、花瓣)的转录组数据为背景材料,用MISA软件检索序列的SSR位点,采用Excel对位点特征进行分析作图,Primer 3.0软件设计引物,TP-M13-SSR PCR筛选引物。结果 在花器官转录组的
39079 条Unigenes中共检测到12365 个SSR位点,位点发生频率为31.64%,平均每5.79 kb出现1个SSR位点。SSR位点的重复类型主要为二核苷酸重复碱基,占SSR位点总数的71.85%,优势重复类型为AG/CT,占碱基总数的61.34%;其次为三核苷酸重复碱基,为26.10%,优势重复类型是AAG/CTT,占比8.30%。SSR碱基重复次数在5~20次,序列长度为12~30 bp,平均长度18.38 bp。引物设计获得9212 对引物,从中随机挑选100对进行PCR扩增验证,筛选出9对多态性好的引物,可将12份睡莲种质在遗传相似系数为0.735时聚为3支。结论 热带睡莲保罗蓝花器官转录组中的SSR位点分布频率高、类型丰富,多态性较高,具较大的应用潜力。开发的9对SSR引物可将12份种质有效分开,进一步丰富了睡莲现有SSR标记,可为睡莲属植物的遗传多样性分析和分子辅助育种提供科学参考。Abstract:Objective SSRs in the transcriptome of Nymphaea Paul Stetson flowers were studied to generate new markers for evaluating germplasms and facilitating breeding of tropical waterlilies.Method SSR loci were retrieved from the transcriptomes of floral pistils, stamens, and petals of Nymphaea Paul Stetson using MISA. Characteristics of the loci were analyzed by Excel, and primers designed by Primer 3.0 and screened by TP-M13-SSR PCR.Result There were12365 SSR loci found in the39079 unigenes of the transcriptome at the frequency of 31.64% averaging one SSR locus per 5.79 kb. Most of the SSR loci had dinucleotide repeat motifs comprising 71.85% of total with AG/CT being the dominant unit that made up 61.34% of the motifs. Trinucleotide repeat motifs accounted for 26.10% of the sites with AAG/CTT being dominant at 8.30%. The repeating frequency was 5–20 times with a sequence of 12–30 bp averaging 18.38 bp long. Of the9212 pairs of primers designed, 100 were randomly selected for a validation by PCR amplification to arrive at 9 pairs with high polymorphism being used as the markers. Subsequently, the 12 germplasms were clustered into 3 branches under a genetic similarity coefficient of 0.7375.Conclusion The SSR loci in the Nymphaea Paul Stetson transcriptome were high on distribution frequency, rich in diversity, greatly polymorphic, and desirable for applications. The 9 pairs of SSR primers identified in this study extended the existing marker repertoire facilitating effective germplasm differentiation on waterlilies.-
Keywords:
- tropical waterlily /
- transcriptome /
- SSR /
- sequence analysis
-
0. 引言
【研究意义】热带睡莲是睡莲属(Nymphaea L.)植物的一个生态类型,该类型种/品种花朵的花香、花色和花型等表型性状丰富,观赏价值极高,是湿地园林景观建设常用的大型水生植物[1]。近年来,我国睡莲产业迅速发展,睡莲育种研究工作不断深入,众多新种质投入生产使用,由于原引进品种的管理不规范,导致新种质的遗传背景未能有效辨析,出现了命名混乱、图片与种苗实物不对版等现象[2]。依据花器官等表型性状进行睡莲种质鉴定的传统分类学方法,已无法准确有效地划分新选育种质的进化归属,严重制约了睡莲种质资源的创新利用。DNA分子标记是鉴定物种种质资源的常用技术,从分子层面对睡莲种质资源进行区分和鉴定,可有效弥补传统分类学研究的不足。简单重复序列(SSRs)又称微卫星,广泛存在于动植物基因组的编码和非编码区,具有可重复性、多等位基因、共显性遗传、相对丰富等特点,是常用的高效遗传标记类型[3]。花朵是睡莲种质进行种/品种/品系鉴定分类、品质比较和获取表型性状的主要器官,根据睡莲花器官转录组数据进行SSR位点特征分析和筛选多态性优良的SSR引物,对睡莲的种质资源评价、遗传多样性分析及分子标记辅助育种等具有重要意义。【前人研究进展】目前,关于睡莲的DNA分子标记研究有ISSR[4,5]、SRAP[2]、SSR[6,7]以及DNA条形码[8]技术等,其中已报道的睡莲SSR分子标记开发主要依据睡莲的全基因组和叶片转录组数据,而形态学分类主要依据花器官表型性状,故部分种质的SSR标记聚类分析结果与形态学分类结果存在较大分歧[2,6]。前人依据SSR位点所在位置将其分为基因组SSRs(gSSRs)和表达序列SSRs(EST-SSRs或cDNA-SSRs)[9],与基因组SSRs相比,表达序列SSRs位于基因编码区,更适用于解释不同种群的表型多样性,便于进行功能基因定位和进化分析[10]。根据基因表达序列开发SSRs的方法有两种,一种是通过建立cDNA文库和克隆测序获得,存在着工作量大、步骤复杂、价格昂贵等缺点;另一种方法一般以公共数据库的表达序列标签和转录组测序结果为依据,通过软件来开发[11]。目前,利用转录组测序开发SSR引物已在花卉[12−14]、水果[15]、中草药[11]、蔬菜[16]等作物上广泛应用。【本研究切入点】已报道的睡莲SSR位点均基于睡莲基因组或叶片等营养器官转录组数据筛选而来,本项目则从睡莲花器官的转录组数据中筛选SSR位点,分析其分布规律和序列特征,并进行引物筛选和验证,以有效增强用于睡莲种质资源评价、遗传多样性分析和分子辅助育种研究的SSR标记引物的丰富性。【拟解决的关键问题】本研究利用DNBSEQ测序平台对热带睡莲保罗蓝花进行转录组测序,并对测序结果的SSR分布和序列特征进行分析,研究结果可为EST-SSR引物的大量开发及利用SSR技术对睡莲不同品种进行遗传多样性的进一步分析提供科学参考,为睡莲种质的分类鉴定和资源保护提供分子水平的理论依据。
1. 材料与方法
1.1 试验材料
供试睡莲品种保罗蓝来源于广西壮族自治区亚热带作物研究所睡莲种质资源试验基地(22°53′44″N, 108°20′38″E),为5年生苗。于2021年8月晴朗天气采集睡莲保罗蓝鲜花样品,去除萼片、花梗,清水洗净后,放入液氮速冻并研磨,混合后的样品交由华大基因完成RNA提取、cDNA文库构建及转录组测序,测序平台为DNBSEQ。对测序后的高质量序列进行Trinity组装得到Transcript序列,进一步依据序列的相似性和长度,挑选最长的Unigene用于后续试验。
1.2 试验方法
1.2.1 SSR位点检索及引物设计
获得的Unigenes利用MISA(http://pgrc.ipk-gatersleben.de/misa/)在线软件进行SSR位点检索分析,设置参数为:单核苷酸最低重复次数为20次,其他核苷酸类型最低重复次数均为5次,复合型重复SSR筛选条件为2个SSR间距低于100 bp。分析得到的SSR位点用Primer 3.0进行引物批量设计,参照前人在云南金花茶(Camellia fascicularis)[13]中的参数设置,产物的理论长度为100~500 bp。
1.2.2 基因组 DNA 提取及检测
采用传统CTAB法提取睡莲叶片DNA,采用超微量紫外光度计NanoDrop 2000检测DNA浓度,并逐个稀释至25 ng·μL−1,−20 ℃冰箱保存备用。
1.2.3 SSR-PCR有效性验证
随机挑选100对引物,经华大基因合成后,选取2份睡莲原生种质(蓝星睡莲Nymphaea colorata和小花睡莲Nymphaea micrantha)进行PCR扩增,扩增产物先经过琼脂糖电泳初步检测,挑选扩增条带单一且清晰的引物再进行M13荧光引物合成。最后,利用筛选得到的引物对12份睡莲种质(表1)进行PCR扩增,采用毛细管电泳检测扩增产物。
表 1 12份睡莲种质的样品信息Table 1. Information on 12 waterlily germplasms编号
No.样品名称
Sample name来源
Source属性
Attribute1 喀麦隆 Nymphaea zenkeri 海南海口 原种 2 阅卿 Nymphaea Yue Qing 广西都安 园艺杂交种 3 鲁吉娜 Nymphaea rudgeana 江苏南京 原种 4 蓝星 Nymphaea colorata 海南三亚 原种 5 雪白睡莲 Nymphaea candida 海南三亚 原种 6 增殖睡莲 Nymphaea prolifera 海南三亚 原种 7 卡本 Nymphaea carpentariae 海南三亚 原种 8 小花睡莲 Nymphaea micrantha 海南三亚 原种 9 变色澳洲 Nymphaea atrans 云南大理 原种 10 小白子午莲 Nymphaea tetragona 浙江温州 原种 11 我的心 Nymphaea Wode Xin 海南海口 园艺杂交种 12 印度红 Nymphaea rubra 海南三亚 原种 PCR反应体系为20.0 µL:ddH2O 14.8 μL,dNTP 0.4 μL,Buffer 2 μL,上下游引物各 0.3 μL(20 μmol·L−1),DNA模板2 μL,TaKaRa Ex Taq® 0.2 μL。
PCR扩增程序:94 ℃预变性5 min;94 ℃变性30 s,60 ℃复性45 s,72 ℃延伸50 s,共 35个循环;最终72 ℃延伸5 min。
1.3 数据分析
采用Excel 2019进行数据统计分析。SSR分布平均距离计算方法为总Unigene的长度除以SSR的总数,SSR出现频率计算方法为SSR总数除以Unigene的总序列数量。利用Popgene 1.32 软件进行遗传多样性分析。
2. 结果与分析
2.1 保罗蓝花转录组中SSR位点的数量
保罗蓝花转录组测序共组装获得
39079 条去冗余Unigenes,总长度71547.293 kb,GC含量为49.57%。在保罗蓝花的Unigene序列共检测出12365 个SSR位点,分布于9059 条Unigenes(占总Unigene序列的23.18%),SSR的发生频率为31.64%。2462 条Unigene序列上的SSR位点数量为2个或以上,1376 条Unigene序列上分布有复合型SSR位点,整体平均出现1个SSR位点的距离为5.79 kb。2.2 保罗蓝花转录组中SSR位点的重复碱基类型
1~6 bp的SSR碱基类型在保罗蓝睡莲花转录组数据中均有分布(表2),不同SSR碱基类型的数量差异较大。二、三核苷酸重复碱基类型最多,分别为
8884 个(占比71.85%)和3227 个(占比26.10%)。四、五、六核苷酸和单核苷酸类型占比均较低,四者共计254个位点,占比仅为2.07%。SSR位点数量与碱基重复类型无明显规律。二核苷酸重复类型的SSR分布距离最小,为8.05 kb,五核苷酸重复类型的分布距离最大,约为二核苷酸类型的493.56倍;SSR片段长度平均为18.38 bp,最长为六核苷酸(32.44 bp),其次为单核苷酸(28.19 bp),最短的是三核苷酸(17.96 bp)。表 2 保罗蓝花转录组SSR中重复碱基类型分析Table 2. Type and repeat motifs of SSR loci in transcriptome of N. Paul Stetson flowers重复碱基类型
Repeat base type数量
Number占总SSR比例
Proportion of total SSR/%出现频率
Frequency of occurrence/%分布平均距离
Mean distance/kb平均长度
Average length/bp单碱基重复 Mononucleotide 91 0.73 0.23 786.23 28.19 双碱基重复 Dinucleotide 8884 71.85 22.73 8.05 18.34 三碱基重复 Trinucleotide 3227 26.10 8.26 22.17 17.96 四碱基重复 Tetranucleotide 86 0.70 0.22 831.95 21.21 五碱基重复 Pentanucleotide 18 0.14 0.05 3974.85 27.50 六碱基重复 Hexanucleotide 59 0.48 0.15 1212.67 32.44 总计 Total 12365 100 31.64 5.79 18.38 2.3 保罗蓝花转录组中SSR重复碱基构成
保罗蓝花转录组数据
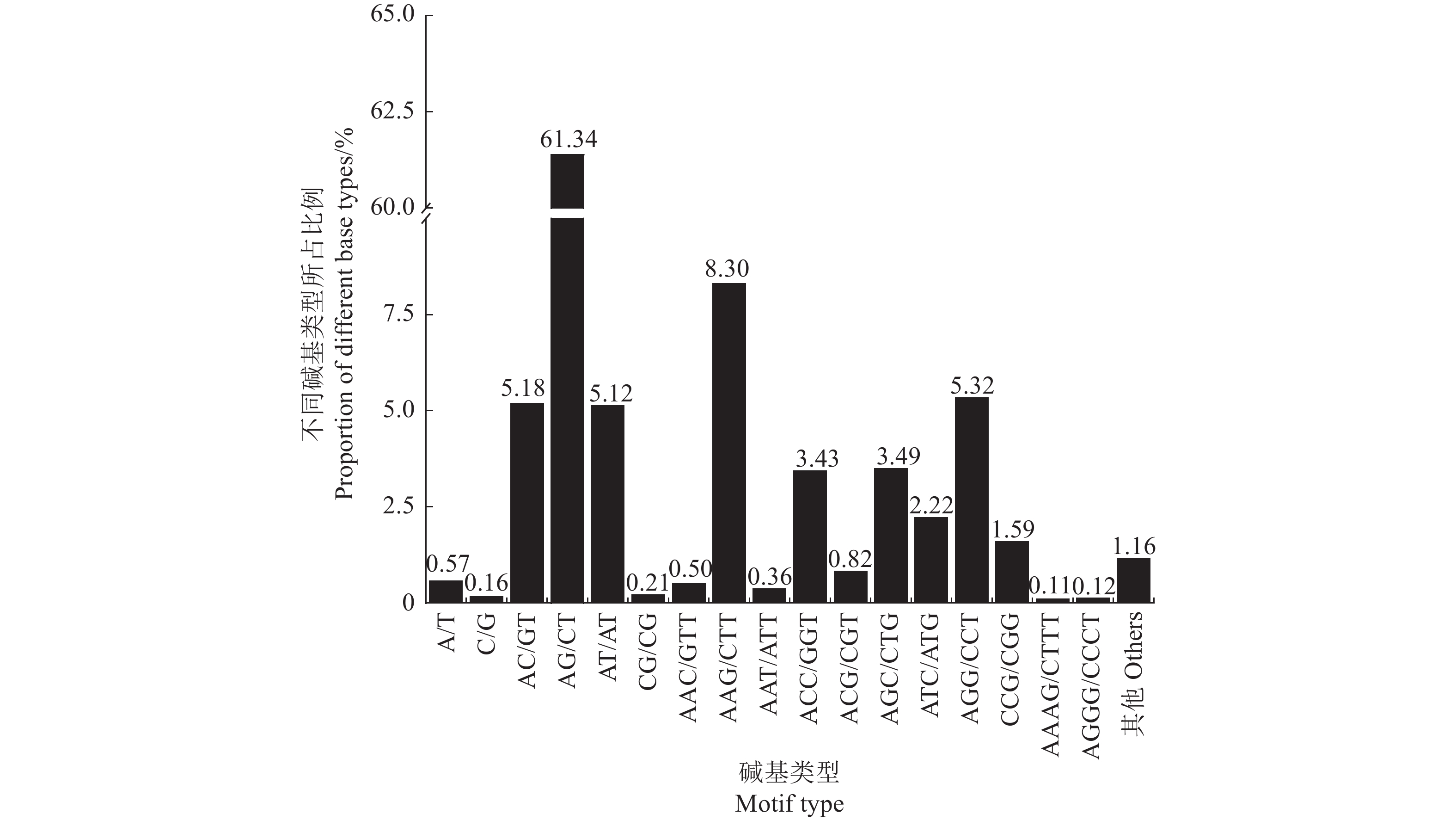
12365 个SSR位点中,共发现了67种重复碱基类型,单核苷酸至六核苷酸重复碱基类型数量分别为2、4、10、15、7、29。在所有核苷酸重复类型中,二核苷酸碱基类型以AG/CT占绝对优势(共计7585 个,占61.34%);其次为三核苷酸重复碱基中的AAG/CTT为优势碱基类型(共计1026 个,占8.30%)。在二核苷酸重复类型中,除AG/CT占绝对优势外,排名依次为AC/GT(共计640个,占5.18%),AT/AT(共计633个,占5.12%),CG/CG(共计26个,占0.21%)。在三核苷酸重复碱基中除AAG/CTT为优势碱基外,排名依次为AGG/CCT(共计658个,占5.32%)、AGC/CTG(共计431个,占3.49%)、ACC/GGT(共计424个,占3.43%)、ATC/ATG(274个,占2.22%)、CCG/CGG(197个,占1.59%)、ACG/CGT(共计102个,占0.82%)、AAC/GTT(共计62个,占0.50%)、AAT/ATT(共计45个,占0.36%)、ACT/AGT(共计8个,占0.06%)(图1)。单、四、五、六核苷酸重复碱基虽然类型丰富,但总体占比较低,仅出现1次的碱基类型有18种。2.4 保罗蓝花转录组SSR多态性潜力分析
2.4.1 保罗蓝花转录组SSR碱基重复次数分布
保罗蓝花转录组SSR位点碱基重复次数总体上与各类型重复碱基的数量和比例呈反比(表3)。除单核苷酸类型外,不同SSR碱基重复次数为5~20,占总SSR的98.27%,单核苷酸主要为20~30次(占单核苷酸类型总数的95.60%,占总SSR的0.70%)。经统计,共计
9902 个(80.08%)SSR的重复次数为5~10次,属低重复次数;分别有1626 个(13.15%)和495个(4.00%)SSR位点重复次数为11~15次和16~20次,属中度重复次数。全部SSR碱基中占比较高的重复次数依次是6次、5次、7次和8次,重复数量分别为3023 、1920、1854、1365 个,分别占SSR总数的15.53%、24.45%、14.99%、11.04%。表 3 保罗蓝花转录组中不同重复次数的SSR数量分析Table 3. Number of SSR with different repetitions in transcriptome of N. Paul Stetson flowers重复类型
Repeat typeSSR数量 Amount/个 总计
Total5次 6次 7次 8次 9次 10次 11次 12次 13次 14次 15次 16次 17次 18次 19次 20次 21~29次 30~41次 单核苷酸
Mononucleotide0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 23 64 4 91 二核苷酸
Dinucleotide0 2273 1518 1204 902 720 566 394 276 240 150 169 107 84 93 42 140 6 8884 三核苷酸
Trinucleotide1798 718 333 157 79 37 35 19 19 11 7 7 4 1 2 0 0 0 3227 四核苷酸
Tetranucleotide66 17 2 0 0 1 0 0 0 0 0 0 0 0 0 0 0 0 86 五核苷酸
Pentanucleotide13 3 0 2 0 0 0 0 0 0 0 0 0 0 0 0 0 0 18 六核苷酸
Hexanucleotide43 12 1 2 1 0 0 0 0 0 0 0 0 0 0 0 0 0 59 总计 Total 1920 3023 1854 1365 982 758 601 413 295 251 157 176 111 85 95 65 204 8 12365 2.4.2 保罗蓝花转录组SSR片段重复长度
前人研究认为理想的SSR标记位点长度在20 bp及以上,这类型的SSR位点通常多态性较高;多态性适中的SSR标记长度为12~20 bp;而长度小于12 bp的SSR标记多态性极低[17]。本研究鉴定到的SSR长度均在12 bp以上,主要分布区域为12~20 bp,共有
9222 个位点长度分布于该区域,占总SSR的74.58%。长度21~30 bp的共计2374 个,占比19.20%;30 bp以上有769个,占比6.22%(图2)。整体上,保罗蓝花转录组中的SSR长度集中在12~20 bp,最长片段重复长度为82 bp,为二核苷酸类型,出现次数为2次。2.5 保罗蓝花转录组SSR引物设计及初步筛选分析
为筛选出可应用于睡莲属种质分类的SSR分子标记,对
12365 个SSR位点采用Primer 3.0进行引物设计,每位点设计1对引物,结果表明共有9212 个SSR符合引物设计要求,占总SSR位点数的74.50%,包括65个单碱基重复,5619 个二碱基重复,2502 个三碱基重复,56个四碱基重复,15个五碱基重复、44个六碱基重复,以及911个复合型重复(表4)。其中共有8944 个位点的引物长度在20 bp以上且符合引物设计要求,将得到的引物序列与蓝星睡莲参考基因组进对比,发现6992 对SSR引物可以锚定到睡莲染色体上,在这些锚定到染色体上的标记中,4023 个标记可以得到100~500 bp的扩增产物。表 4 保罗蓝转录组的SSR引物信息Table 4. Information on SSR primers in transcriptome of N. Paul Stetson flowers重复碱基类型
Repeat base type符合引物设计要求的 SSR
SSRs that meet primer design requirements引物长度
Primer length/bp退火温度
Annealing temperature/℃上、下游引物退火温度差
Difference in annealing temperature
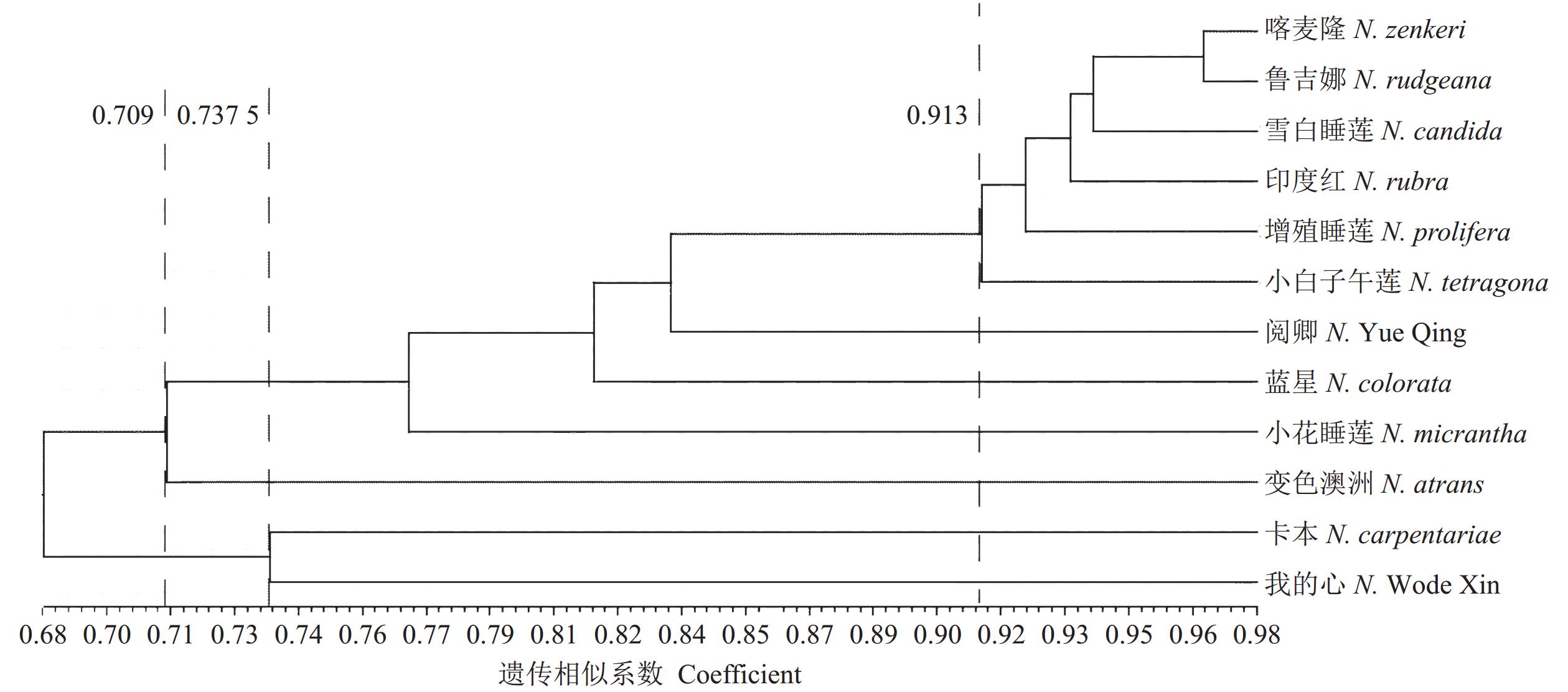
between F and R primers/℃单碱基重复 Mononucleotide 65 20~21 58.98~60.80 <2 二碱基重复 Dinucleotide 5619 18~27 57.02~62.88 <4 三碱基重复 Trinucleotide 2502 18~27 57.04~62.74 <4 四碱基重复 Tetranucleotide 56 20~24 58.90~60.44 <1 五碱基重复 Pentanucleotide 15 19~20 59.72~60.76 <1 六碱基重复 Hexanucleotide 44 18~21 59.02~62.02 <2 复合型重复 Complex repeat type 911 18~27 57.07~62.79 <4 为进一步验证设计引物的实用性和有效性,本研究剔除本课题前期基于基因组筛选的和其他课题组[5]已发表的27对SSR引物,另随机选取100对引物在2个睡莲样品(蓝星睡莲、小花睡莲)中进行多态性引物筛选,共筛选出9对多态性条高(观测等位基因数Na为3~6,有效等位基因数Ne为1.11~1.31,Nei’s基因多样性指数H为0.09~0.20,Shannon’s 信息指数I为0.20~0.33,多态性信息指数PIC为0.55~0.72,均大于0.5)的引物[18](表5、图3),扩增效率为9.0%。选取12份睡莲种质,以筛选出的多态性引物进行毛细管电泳扩增试验和聚类分析。结果(图4)表明,9对引物组合可将12份种质有效区分。在遗传相似系数0.709左右按照花型聚为两支,其中花型似荷花的澳系睡莲聚为1支;在
0.7375 左右将花期花色变化的变色澳洲单独聚为一支;在0.913左右将夜开型睡莲(喀麦隆、鲁吉娜、印度红、丛生睡莲)和耐寒型睡莲(雪白睡莲、小白子午莲)聚为一支。表 5 筛选出的9对SSR引物序列信息Table 5. Information on 9 selected pairs of SSR primers引物编号
Primer number重复单元
Repeating motif引物序列(5′-3′)
Primer sequence等位
基因数
Na有效等位
基因数
NeNei’s基因
多样性指数
HShannon’s
信息指数
I多态性
信息指数
PIC位点所在
染色体编号
Chromosome
number of
the siteP1 (AG)6 F: CAAAGGCTTACAAGGTTTAACG
R: CGCTTGGTTCTATTCGGAAA3 1.13 0.11 0.22 0.55 1 P20 (GAA)11 F:TTTGCGGAATTTTATAGCCG
R:AGGACATTCGCGTACTGCTT6 1.13 0.11 0.22 0.72 3 P25 (TCA)6 F:TTCTCTGCGAGAGTGCAAGA
R:CAAGCAAGCCTCTGGGTTAG4 1.20 0.16 0.28 0.65 4 P26 (CA)6(GA)11 F:ACATGCATGATGTTCGTGCT
R:TTTTGCTGTCAATCTGCGAC4 1.11 0.10 0.21 0.60 4 P33 (GA)12 F:TGAACGCCACCAGATGTTTA
R:CATGAAGCGAAGCAATCTCA3 1.11 0.10 0.20 0.55 5 P35 (GCA)5 F:ACCAAGGTGATGGTCCAGAG
R:ACCCAACGGGGAGTTAAAAG4 1.31 0.20 0.33 0.69 5 P51 (TC)10 F:TGATCGAGAAAAATGGGGAG
R:CACATGCAAGTGTCACACGA5 1.11 0.09 0.20 0.62 7 P63 (GCA)5 F:TTGGACGCTGCAGAATTTTT
R:TCCTTCCACCCATCTCTTTG4 1.14 0.12 0.23 0.62 9 P77 (TC)11 F:CACCCTATACACGTCCCACC
R:GCAGAACCCATGTTCCTGTT5 1.12 0.11 0.21 0.64 11 平均值 Average 4.22 1.15 0.12 0.23 0.63 3. 讨论与结论
随着高通量转录组测序的高速发展,研究基因表达水平、定位功能基因并开发分子标记变得更加快速、便利[19]。本研究对保罗蓝花器官转录组数据的SSR序列特征进行分析,共获得了
12365 个SSR位点,分布于9059 条Unigenes上,SSR发生频率为31.64%,位点平均出现距离5.79 kb,低于小花睡莲和蓝星睡莲叶片转录组的SSR发生频率(33.98%)和位点平均出现距离(11.94 kb),且3种睡莲转录组数据的SSR位点平均出现距离均高于蓝星睡莲基因组的SSR平均出现距离(1.69 kb)[20],表明同属不同物种具有不同的SSR分布特征规律,且不同测序方法获得SSR分布特征存在较大差异。前人研究结果显示万寿菊(Tagetes erecta)[21]、三色堇(Viola × wittrockiana)[22]、云南火焰兰(Renanthera imschootiana R.)[14]、冬瓜(Benicasa hispida)[16]等草本植物的转录组SSR发生频率和位点平均出现距离均低于云南金花茶[13]、美国红枫(Acer rubrum)[23]、油茶(Camellia oleifera)[24]、山桐子(Idesia polycarpa)[25]等木本植物,表明同类型植物的SSR分布特征存在相似性[26]。本研究中保罗蓝花器官转录组SSR发生频率和位点平均出现距离高于上述草本植物,但低于木本植物,表明保罗蓝花器官转录组SSR位点数量较丰富,可满足用于睡莲分类的SSR标记引物开发需求。植物编码基因集中频繁出现AG/CT重复单元,反映出植物mRNA序列中广泛存在UCU和CUC密码子,这些密码子翻译的丙氨酸(Ala)和亮氨酸(Leu)在蛋白质序列中出现的频率高于其他种类氨基酸[27]。本研究结果显示在保罗蓝花器官转录组SSR重复类型以二、三核苷酸重复碱基为主,分别占71.85%和26.10%。其中二核苷酸碱基类型AG/CT占比达61.34%,推测在保罗蓝花器官转录组筛选的unigenes编码蛋白序列中氨基酸Ala和Leu含量可能较高。三核苷酸重复碱基AAG/CTT在云锦杜鹃(Rhododendron fortunei)[28]、油梨(Persea americana)[29]、苦楝(Melia azedarach)[30]、冬瓜[16]等双子叶植物中普遍存在。保罗蓝花器官转录组SSR的三核苷酸重复碱基亦存在AAG/CTT类型(共计
1026 个,占8.30%),符合双子叶植物SSR分布特征规律,且占比高于蓝星睡莲和小花睡莲叶片转录组和蓝星睡莲基因组AAG/CTT类型SSR位点数量[19],进一步表明同属不同物种的SSR分布特征存在差异性。此外,本研究在保罗蓝花器官转录组SSR位点中搜索到197个上述双子叶植物中不常见的CCG/CGG重复碱基,有研究表明CCG/CGG重复碱基可能参与植物的信号传导、代谢调控和抗逆性等生理功能的进化演变[31]。早期研究显示物种的简单重复序列越丰富,则该物种的进化演变时间越长,反之则进化时间越短或变异频率越低[32]。本研究基于睡莲花器官SSR位点发生频率较高且具有CCG/CGG重复碱基等独特的SSR位点重复单元,表明睡莲植物进化演变历史长,印证了植物分类学上将睡莲与无油樟目(Amborellales)、木兰藤目(Austrobaileyales)植物均归类为被子植物基部群的观点[33]。SSR位点的碱基长度和重复次数是影响SSR序列多态性的主要因素。本研究通过对保罗蓝花器官转录组SSR位点重复次数进行分析发现,保罗蓝花器官转录组SSR位点重复次数与油梨(Persea americana)[28]、灰毡毛忍冬(Lonicera macranthoides)[34]等植物研究结果一致,均表现为重复次数多集中于5~20,重复类型总体与重复次数呈反比,四、五、六核苷酸重复碱基的多态性普遍低于单、二、三核苷酸重复类型,二核苷酸重复碱基的重复次数跨度最大且重复次数相对较多,这一类型的SSR位点通常表现出较高的多态性。美国红枫(11.27%)[22]、云南金花茶(7.71%)[13]、云南火焰兰(22.51%)[14]等植物中当SSR序列长度≥20 bp时,SSR序列均表现出较高的多态性。本研究筛选的保罗蓝花器官SSR序列长度>20 bp的位点占25.42%,推测含有上述碱基长度和重复次数特征的SSR位点具有较高多态性和应用价值,可作为睡莲属植物SSR分子标记开发的重点关注位点。此外,本研究从保罗蓝花器官转录组数据中筛选出符合引物设计的SSR位点共有
9212 个,占保罗蓝花转录组SSR位点总数的74.50%,从中随机挑选合成的100对引物经PCR验证,鉴定出9对多态性高的引物,可将供试的12份睡莲种质有效区分,进一步表明借助转录组数据筛选的SSR位点,可作为SSR分子标记引物开发的重要参考。 -
表 1 12份睡莲种质的样品信息
Table 1 Information on 12 waterlily germplasms
编号
No.样品名称
Sample name来源
Source属性
Attribute1 喀麦隆 Nymphaea zenkeri 海南海口 原种 2 阅卿 Nymphaea Yue Qing 广西都安 园艺杂交种 3 鲁吉娜 Nymphaea rudgeana 江苏南京 原种 4 蓝星 Nymphaea colorata 海南三亚 原种 5 雪白睡莲 Nymphaea candida 海南三亚 原种 6 增殖睡莲 Nymphaea prolifera 海南三亚 原种 7 卡本 Nymphaea carpentariae 海南三亚 原种 8 小花睡莲 Nymphaea micrantha 海南三亚 原种 9 变色澳洲 Nymphaea atrans 云南大理 原种 10 小白子午莲 Nymphaea tetragona 浙江温州 原种 11 我的心 Nymphaea Wode Xin 海南海口 园艺杂交种 12 印度红 Nymphaea rubra 海南三亚 原种 表 2 保罗蓝花转录组SSR中重复碱基类型分析
Table 2 Type and repeat motifs of SSR loci in transcriptome of N. Paul Stetson flowers
重复碱基类型
Repeat base type数量
Number占总SSR比例
Proportion of total SSR/%出现频率
Frequency of occurrence/%分布平均距离
Mean distance/kb平均长度
Average length/bp单碱基重复 Mononucleotide 91 0.73 0.23 786.23 28.19 双碱基重复 Dinucleotide 8884 71.85 22.73 8.05 18.34 三碱基重复 Trinucleotide 3227 26.10 8.26 22.17 17.96 四碱基重复 Tetranucleotide 86 0.70 0.22 831.95 21.21 五碱基重复 Pentanucleotide 18 0.14 0.05 3974.85 27.50 六碱基重复 Hexanucleotide 59 0.48 0.15 1212.67 32.44 总计 Total 12365 100 31.64 5.79 18.38 表 3 保罗蓝花转录组中不同重复次数的SSR数量分析
Table 3 Number of SSR with different repetitions in transcriptome of N. Paul Stetson flowers
重复类型
Repeat typeSSR数量 Amount/个 总计
Total5次 6次 7次 8次 9次 10次 11次 12次 13次 14次 15次 16次 17次 18次 19次 20次 21~29次 30~41次 单核苷酸
Mononucleotide0 0 0 0 0 0 0 0 0 0 0 0 0 0 0 23 64 4 91 二核苷酸
Dinucleotide0 2273 1518 1204 902 720 566 394 276 240 150 169 107 84 93 42 140 6 8884 三核苷酸
Trinucleotide1798 718 333 157 79 37 35 19 19 11 7 7 4 1 2 0 0 0 3227 四核苷酸
Tetranucleotide66 17 2 0 0 1 0 0 0 0 0 0 0 0 0 0 0 0 86 五核苷酸
Pentanucleotide13 3 0 2 0 0 0 0 0 0 0 0 0 0 0 0 0 0 18 六核苷酸
Hexanucleotide43 12 1 2 1 0 0 0 0 0 0 0 0 0 0 0 0 0 59 总计 Total 1920 3023 1854 1365 982 758 601 413 295 251 157 176 111 85 95 65 204 8 12365 表 4 保罗蓝转录组的SSR引物信息
Table 4 Information on SSR primers in transcriptome of N. Paul Stetson flowers
重复碱基类型
Repeat base type符合引物设计要求的 SSR
SSRs that meet primer design requirements引物长度
Primer length/bp退火温度
Annealing temperature/℃上、下游引物退火温度差
Difference in annealing temperature
between F and R primers/℃单碱基重复 Mononucleotide 65 20~21 58.98~60.80 <2 二碱基重复 Dinucleotide 5619 18~27 57.02~62.88 <4 三碱基重复 Trinucleotide 2502 18~27 57.04~62.74 <4 四碱基重复 Tetranucleotide 56 20~24 58.90~60.44 <1 五碱基重复 Pentanucleotide 15 19~20 59.72~60.76 <1 六碱基重复 Hexanucleotide 44 18~21 59.02~62.02 <2 复合型重复 Complex repeat type 911 18~27 57.07~62.79 <4 表 5 筛选出的9对SSR引物序列信息
Table 5 Information on 9 selected pairs of SSR primers
引物编号
Primer number重复单元
Repeating motif引物序列(5′-3′)
Primer sequence等位
基因数
Na有效等位
基因数
NeNei’s基因
多样性指数
HShannon’s
信息指数
I多态性
信息指数
PIC位点所在
染色体编号
Chromosome
number of
the siteP1 (AG)6 F: CAAAGGCTTACAAGGTTTAACG
R: CGCTTGGTTCTATTCGGAAA3 1.13 0.11 0.22 0.55 1 P20 (GAA)11 F:TTTGCGGAATTTTATAGCCG
R:AGGACATTCGCGTACTGCTT6 1.13 0.11 0.22 0.72 3 P25 (TCA)6 F:TTCTCTGCGAGAGTGCAAGA
R:CAAGCAAGCCTCTGGGTTAG4 1.20 0.16 0.28 0.65 4 P26 (CA)6(GA)11 F:ACATGCATGATGTTCGTGCT
R:TTTTGCTGTCAATCTGCGAC4 1.11 0.10 0.21 0.60 4 P33 (GA)12 F:TGAACGCCACCAGATGTTTA
R:CATGAAGCGAAGCAATCTCA3 1.11 0.10 0.20 0.55 5 P35 (GCA)5 F:ACCAAGGTGATGGTCCAGAG
R:ACCCAACGGGGAGTTAAAAG4 1.31 0.20 0.33 0.69 5 P51 (TC)10 F:TGATCGAGAAAAATGGGGAG
R:CACATGCAAGTGTCACACGA5 1.11 0.09 0.20 0.62 7 P63 (GCA)5 F:TTGGACGCTGCAGAATTTTT
R:TCCTTCCACCCATCTCTTTG4 1.14 0.12 0.23 0.62 9 P77 (TC)11 F:CACCCTATACACGTCCCACC
R:GCAGAACCCATGTTCCTGTT5 1.12 0.11 0.21 0.64 11 平均值 Average 4.22 1.15 0.12 0.23 0.63 -
[1] 李淑娟, 尉倩, 陈尘, 等. 中国睡莲属植物育种研究进展 [J]. 植物遗传资源学报, 2019, 20(4):829−835. LI S J, YU Q, CHEN C, et al. Breeding progress of waterlilies in China [J]. Journal of Plant Genetic Resources, 2019, 20(4): 829−835. (in Chinese)
[2] 毛立彦, 龙凌云, 黄秋伟, 等. 基于SRAP分子标记的147份睡莲属植物遗传多样性分析 [J]. 南方农业学报, 2023, 54(2):454−466. MAO L Y, LONG L Y, HUANG Q W, et al. Genetic diversity analysis of 147 Nymphaea Linn. plants based on SRAP molecular marker [J]. Journal of Southern Agriculture, 2023, 54(2): 454−466. (in Chinese)
[3] KALIA R K, RAI M K, KALIA S, et al. Microsatellite markers: An overview of the recent progress in plants [J]. Euphytica, 2011, 177(3): 309−334. DOI: 10.1007/s10681-010-0286-9
[4] 苏群, 杨亚涵, 田敏, 等. 睡莲种质资源遗传多样性分析及DNA指纹图谱构建 [J]. 热带作物学报, 2020, 41(2):258−266. SU Q, YANG Y H, TIAN M, et al. Genetic diversity analysis and DNA fingerprinting construction of waterlily germplasm resources [J]. Chinese Journal of Tropical Crops, 2020, 41(2): 258−266. (in Chinese)
[5] POCZAI P, MÁTYÁS K K, SZABÓ I, et al. Genetic variability of thermal Nymphaea (Nymphaeaceae) populations based on ISSR markers: Implications on relationships, hybridization, and conservation [J]. Plant Molecular Biology Reporter, 2011, 29(4): 906−918. DOI: 10.1007/s11105-011-0302-9
[6] 苏群, 王虹妍, 卢家仕, 等. 睡莲的SSR引物对及合成方法和应用: CN113832254A[P]. 2021-12-24. [7] PARVEEN S, SINGH N, ADIT A, et al. Contrasting reproductive strategies of two Nymphaea species affect existing natural genetic diversity as assessed by microsatellite markers: Implications for conservation and wetlands restoration [J]. Frontiers in Plant Science, 2022, 13: 773572. DOI: 10.3389/fpls.2022.773572
[8] QIAN Z H, MUNYWOKI J M, WANG Q F, et al. Molecular identification of African Nymphaea species (water lily) based on ITS, trnT-trnF and rpl16 [J]. Plants, 2022, 11(18): 2431. DOI: 10.3390/plants11182431
[9] LIU G, XIE Y J, ZHANG D Q, et al. Analysis of SSR loci and development of SSR primers in Eucalyptus [J]. Journal of Forestry Research, 2018, 29(2): 273−282. DOI: 10.1007/s11676-017-0434-3
[10] OLIVEIRA DE OLIVEIRA L, CARLOS BEISE D, DAMIAN DOS SANTOS D, et al. Molecular markers in Carya illinoinensis (Juglandaceae): From genetic characterization to molecular breeding [J]. The Journal of Horticultural Science and Biotechnology, 2021, 96(5): 560−569. DOI: 10.1080/14620316.2021.1892534
[11] JIANG M, YAN S, REN W C, et al. Genetic diversity of the Chinese medicinal plant Astragali Radix based on transcriptome-derived SSR markers [J]. Electronic Journal of Biotechnology, 2023, 62: 13−20. DOI: 10.1016/j.ejbt.2022.12.001
[12] SHI Z Y, ZHAO W Q, LI Z A, et al. Development and validation of SSR markers related to flower color based on full-length transcriptome sequencing in Chrysanthemum [J]. Scientific Reports, 2022, 12(1): 22310. DOI: 10.1038/s41598-022-26664-3
[13] 叶鹏, 李显煌, 唐军荣, 等. 云南金花茶转录组SSR的分布及其序列特征 [J]. 中南林业科技大学学报, 2019, 39(9):86−91. YE P, LI X H, TANG J R, et al. Distribution and characteristics of SSR in transcriptome of Camellia fascicularis [J]. Journal of Central South University of Forestry & Technology, 2019, 39(9): 86−91. (in Chinese)
[14] 辛静, 辛雅萱, 董章宏, 等. 云南火焰兰转录组SSR分布及其序列特征分析 [J]. 南方农业学报, 2020, 51(7):1634−1641. XIN J, XIN Y X, DONG Z H, et al. Distribution and sequence characteristics of SSR in transcriptome of Renanthera imschootiana Rolfe [J]. Journal of Southern Agriculture, 2020, 51(7): 1634−1641. (in Chinese)
[15] ZHANG L S, YANG X N, QI X N, et al. Characterizing the transcriptome and microsatellite markers for almond (Amygdalus communis L. ) using the Illumina sequencing platform [J]. Hereditas, 2017, 155: 14.
[16] JIANG B, XIE D S, LIU W R, et al. De novo assembly and characterization of the transcriptome, and development of SSR markers in wax gourd (Benicasa hispida) [J]. PLoS One, 2013, 8(8): e71054. DOI: 10.1371/journal.pone.0071054
[17] TEMNYKH S, DECLERCK G, LUKASHOVA A, et al. Computational and experimental analysis of microsatellites in rice (Oryza sativa L. ): Frequency, length variation, transposon associations, and genetic marker potential [J]. Genome Research, 2001, 11(8): 1441−1452. DOI: 10.1101/gr.184001
[18] 梁燕, 韩传明, 孙超, 等. 基于SSR标记的核桃种质资源遗传多样性与遗传结构分析 [J]. 北方园艺, 2022, (9):47−54. LIANG Y, HAN C M, SUN C, et al. Genetic diversity and genetic structure analysis of walnut germplasm resources based on SSR markers [J]. Northern Horticulture, 2022(9): 47−54. (in Chinese)
[19] CRISTANCHO M, ESCOBAR C. Transferability of SSR markers from related Uredinales species to the coffee rust Hemileia vastatrix [J]. Genetics and Molecular Research: GMR, 2008, 7(4): 1186−1192. DOI: 10.4238/vol7-4gmr493
[20] 苏群, 田敏, 刘俊, 等. 基于生物信息学的睡莲SSR位点特征分析 [J]. 西南农业学报, 2021, 34(10):2076−2083. SU Q, TIAN M, LIU J, et al. SSR loci characteristic analysis of water lily based on bio-informatics methodology [J]. Southwest China Journal of Agricultural Sciences, 2021, 34(10): 2076−2083. (in Chinese)
[21] 张华丽, 丛日晨, 王茂良, 等. 基于万寿菊转录组测序的SSR标记开发 [J]. 园艺学报, 2018, 45(1):159−167. ZHANG H L, CONG R C, WANG M L, et al. Development of SSR molecular markers based on transcriptome sequencing of Tagetes erecta [J]. Acta Horticulturae Sinica, 2018, 45(1): 159−167. (in Chinese)
[22] 杜晓华, 杨雅萍, 朱小佩, 等. 三色堇转录组SSR分析及分子标记开发 [J]. 园艺学报, 2019, 46(4):797−806. DU X H, YANG Y P, ZHU X P, et al. Development of genic-SSR markers by transcriptome sequencing in Viola × wittrockiana [J]. Acta Horticulturae Sinica, 2019, 46(4): 797−806. (in Chinese)
[23] 郭聪, 陈燕, 王莹, 等. 美国红枫转录组SSR序列分析 [J]. 中南林业科技大学学报, 2021, 41(7):132−141. GUO C, CHEN Y, WANG Y, et al. Sequence analysis of SSR in transcriptome of American red maple [J]. Journal of Central South University of Forestry & Technology, 2021, 41(7): 132−141. (in Chinese)
[24] 张震, 许彦明, 陈永忠, 等. 油茶转录组测序与SSR特征分析 [J]. 西南林业大学学报, 2018, 38(6):63−68. ZHANG Z, XU Y M, CHEN Y Z, et al. Transcriptome sequencing and analysis of SSR characteristics of Camellia oleifera [J]. Journal of Southwest Forestry University (Natural Sciences), 2018, 38(6): 63−68. (in Chinese)
[25] 李娜, 姚民, 梅兰菊, 等. 基于山桐子转录组序列的SSR分子标记开发 [J]. 应用与环境生物学报, 2017, 23(5):952−958. LI N, YAO M, MEI L J, et al. Development of SSR molecular markers based on transcriptome sequencing of Idesia polycarpa Maxim [J]. Chinese Journal of Applied and Environmental Biology, 2017, 23(5): 952−958. (in Chinese)
[26] VARSHNEY R K, GRANER A, SORRELLS M E. Genic microsatellite markers in plants: Features and applications [J]. Trends in Biotechnology, 2005, 23(1): 48−55. DOI: 10.1016/j.tibtech.2004.11.005
[27] YANG Q W, JIANG Y J, WANG Y P, et al. SSR loci analysis in transcriptome and molecular marker development in Polygonatum sibiricum [J]. BioMed Research International, 2022, 2022: 4237913.
[28] 杨彬, 许蔷薇, 牛明月, 等. 云锦杜鹃转录组SSR分析及其分子标记开发 [J]. 核农学报, 2018, 32(12):2335−2345. YANG B, XU Q W, NIU M Y, et al. Analysis of SSR information in transcriptome and development of SSR molecular markers in Rhododendron fortunei [J]. Journal of Nuclear Agricultural Sciences, 2018, 32(12): 2335−2345. (in Chinese)
[29] 郭俊, 朱婕, 谢尚潜, 等. 油梨转录组SSR分子标记开发与种质资源亲缘关系分析 [J]. 园艺学报, 2020, 47(8):1552−1564. GUO J, ZHU J, XIE S Q, et al. Development of SSR molecular markers based on transcriptome and analysis of genetic relationship of germplasm resources in avocado [J]. Acta Horticulturae Sinica, 2020, 47(8): 1552−1564. (in Chinese)
[30] 蔡金峰, 杨晓明, 郁万文, 等. 基于苦楝转录组测序的SSR分子标记开发 [J]. 林业科学, 2021, 57(6):85−92. CAI J F, YANG X M, YU W W, et al. Development of SSR molecular markers based on transcriptome sequencing of Melia azedarach [J]. Scientia Silvae Sinicae, 2021, 57(6): 85−92. (in Chinese)
[31] 郝广婧, 祁银燕, 张得芳, 等. 基于转录组的黑果枸杞SSR分布特征分析及引物设计 [J]. 分子植物育种, 2019, 17(13):4342−4350. HAO G J, QI Y Y, ZHANG D F, et al. Analysis of SSR distribution characteristics and primer design of Lycium ruthenicum Murr. based on transcriptome [J]. Molecular Plant Breeding, 2019, 17(13): 4342−4350. (in Chinese)
[32] HARR B, SCHLÖTTERER C. Long microsatellite alleles in Drosophila melanogaster have a downward mutation bias and short persistence times, which cause their genome-wide underrepresentation [J]. Genetics, 2000, 155(3): 1213−1220. DOI: 10.1093/genetics/155.3.1213
[33] ZHANG L S, CHEN F, ZHANG X T, et al. The water lily genome and the early evolution of flowering plants [J]. Nature, 2020, 577(7788): 79−84. DOI: 10.1038/s41586-019-1852-5
[34] 刘思思, 乔中全, 曾慧杰, 等. 灰毡毛忍冬转录组SSR位点分析及EST-SSR标记开发 [J]. 分子植物育种, 2021, 19(9):3015−3021. LIU S S, QIAO Z Q, ZENG H J, et al. Analysis on SSR loci in transcriptome and development of EST-SSR molecular markers in Lonicera macranthoides [J]. Molecular Plant Breeding, 2021, 19(9): 3015−3021. (in Chinese)
-
期刊类型引用(1)
1. 曹婧,李风童,孙春青. 睡莲属植物的研究进展. 植物遗传资源学报. 2025(02): 207-217 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载: