A Rapid Real Time Fluorescence Recombinase-aided Amplification Method for Detecting Porcine Pseudorabies Virus
-
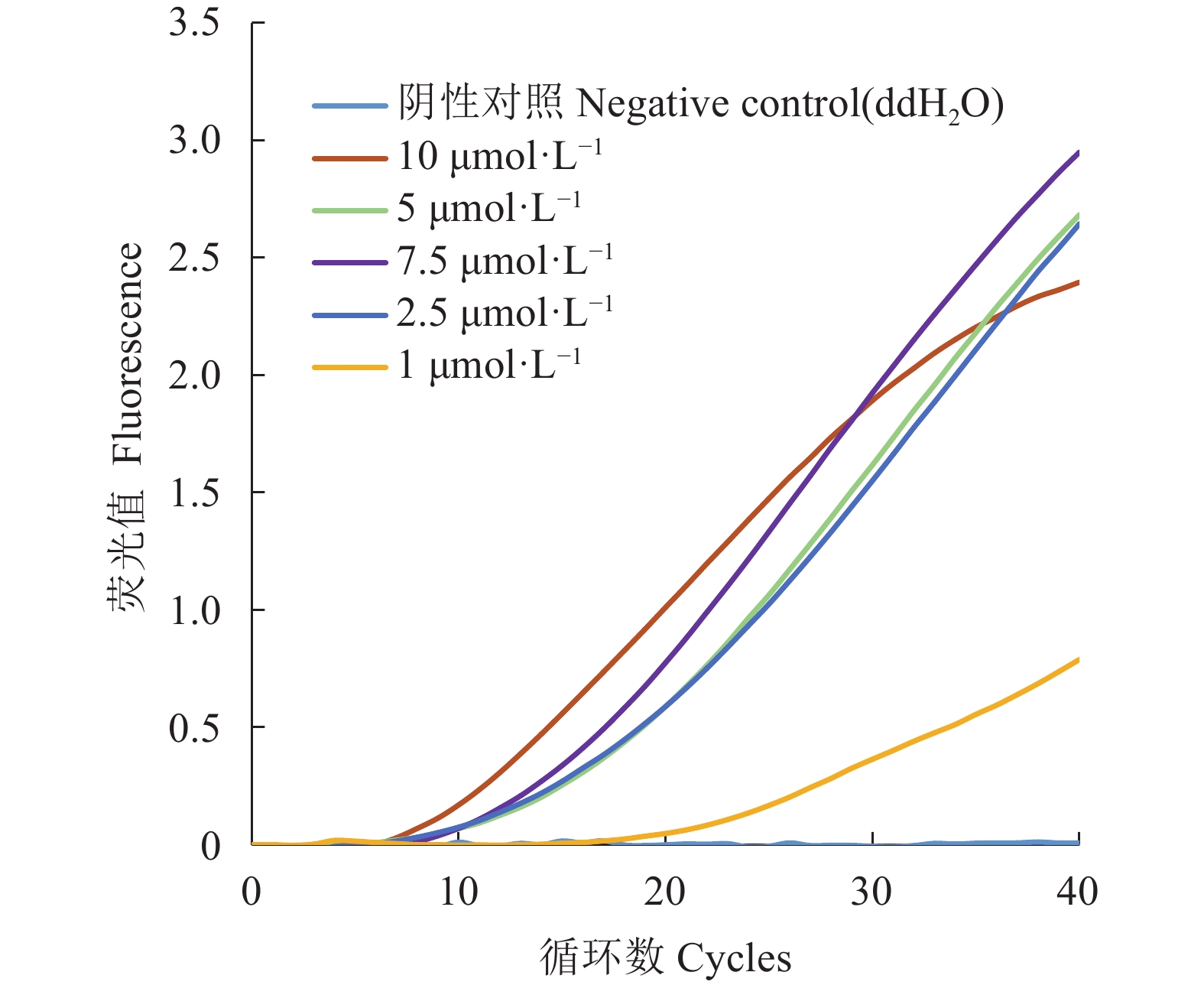
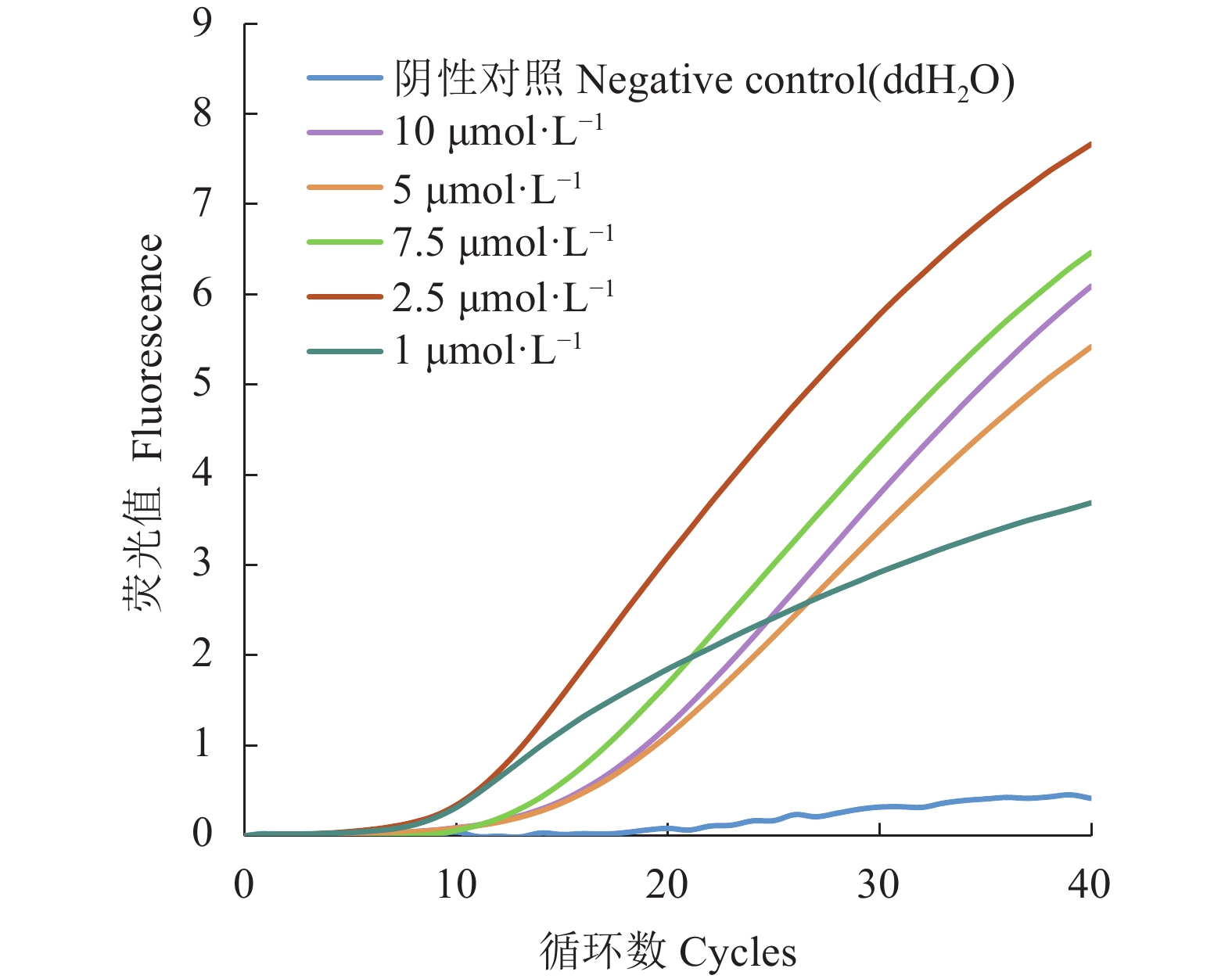
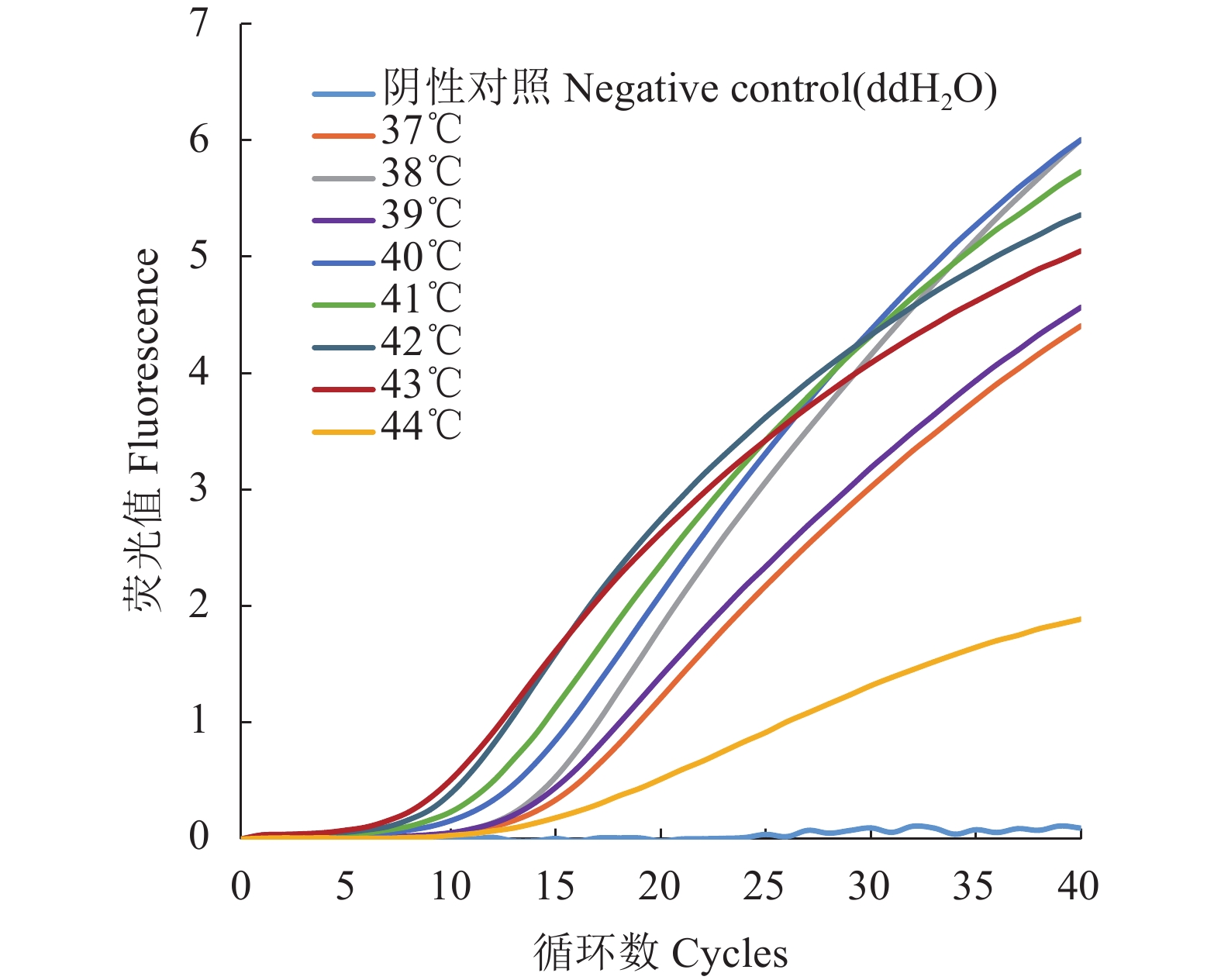
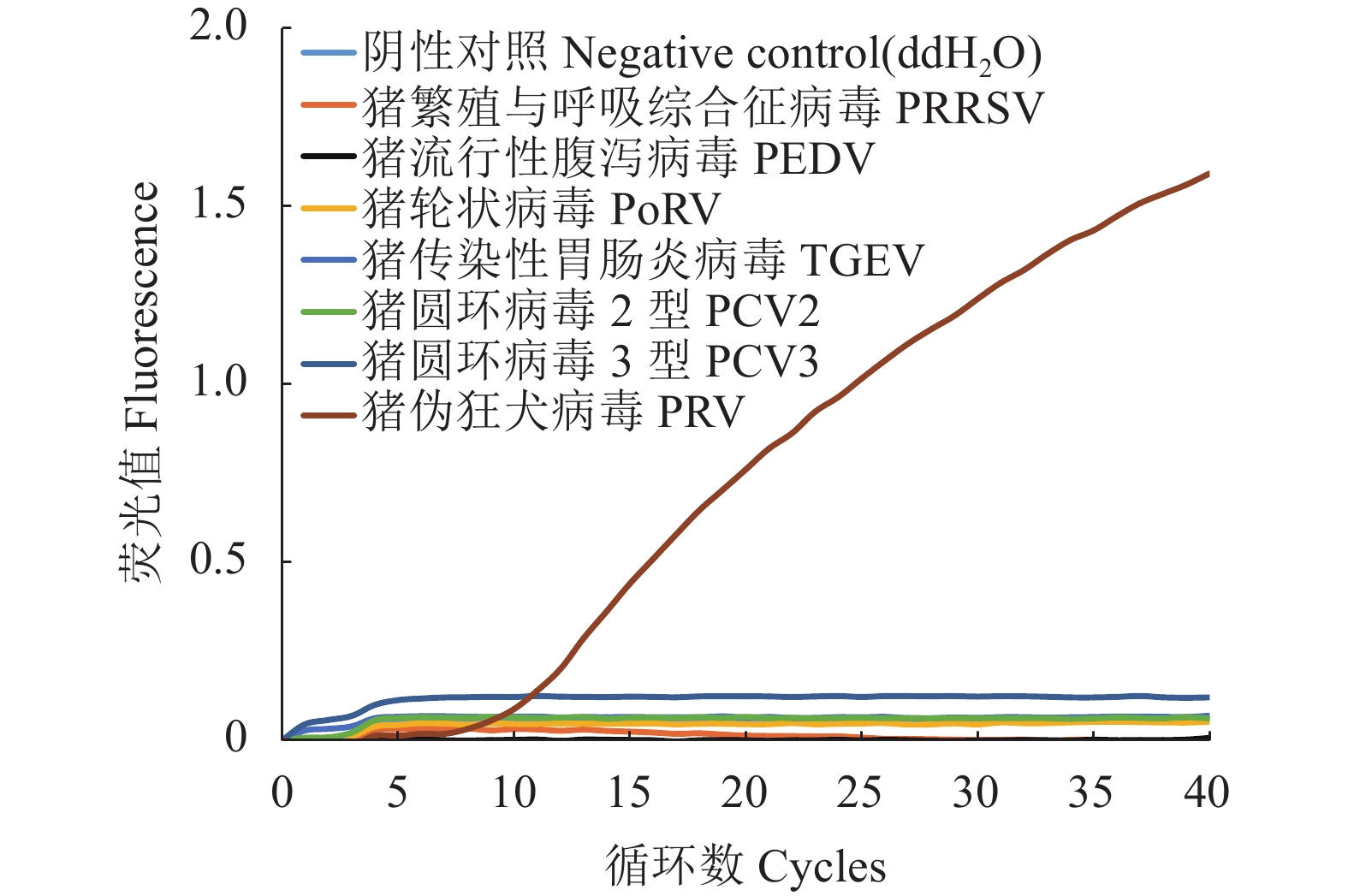
摘要:目的 基于荧光重组酶介导核酸扩增(Recombinase-aided amplification, RAA)技术,建立一种猪伪狂犬病毒(Porcine pseudorabies virus, PRV)快速检测方法。方法 根据PRV gE基因序列,设计特异性引物及探针,优化扩增体系,建立PRV荧光重组酶介导核酸扩增检测方法,检验其特异性、敏感性和重复性,应用该方法对临床样品进行检测。结果 该方法在43 ℃恒温反应23 min即可完成PRV核酸扩增,最低检出限为111 copies·μL−1;与猪繁殖与呼吸综合征病毒(Porcine reproductive and respiratory syndrome virus, PRRSV)、猪流行性腹泻病毒(Porcine epidemic diarrhea virus, PEDV)、猪轮状病毒(Porcine rotavirus, PoRV)、猪传染性胃肠炎病毒(Transmissible gastroenteritis virus, TGEV)、猪圆环病毒2型(Porcine circovirus 2, PCV2)、猪圆环病毒3型(Porcine circovirus 3, PCV3)均无交叉反应。重复性试验显示,组内和组间变异系数均小于5%;40份临床样品检测结果显示PRV阳性率为15%(6/40),检测结果与常规聚合酶链式反应(PCR)一致。结论 成功建立了简便快速、高效准确的PRV实时荧光RAA检测方法,为PRV的快速检测和流行病学调查提供了新的检测手段。
-
关键词:
- 猪伪狂犬病毒 /
- 荧光重组酶介导核酸扩增 /
- 检测方法
Abstract:Objective A rapid method applying the recombinase-aided amplification (RAA) method for detecting porcine pseudorabies virus (PRV) was developed.Methods Based on the sequence of gE gene in PRV, specific primers and probes were designed. Amplification conditions were optimized, and assay specificity, sensitivity, and reproducibility scrutinized by a verification trial on clinical samples.Results The newly developed assay successfully amplified the PRV nucleic acids in merely 23m under the constant temperature of 43 ℃ with a detection limit of 111 copies·μL−1. There were no cross reactions with viruses that produced reproductive and respiratory syndromes, epidemic diarrhea, rotavirus, transmissible gastroenteritis, circovirus 2, or circovirus 3 on pigs. The coefficients of variation within a group and between groups on the repeatability test were less than 5%. And, on 40 clinical samples, the positive detection on PRV of the assay was 15% (6/40), which was comparable to that of the conventional PCR.Conclusion A simple, rapid, efficient, and accurate method of fluorescence RAA detection on PRV was established for laboratory testing and epidemiological investigation of the disease. -
-
图 7 临床样品PRV的PCR和RAA检测
A:临床样品RAA结果。B:临床样品PCR结果;M:DL 2000 Marker;1:阴性对照;2:阳性对照;3~42:临床样品。
Figure 7. PRV detections by conventional PCR and fluorescent RAA on clinical samples
A: results on clinical samples by fluorescent RAA; B: results on clinical samples by conventional PCR; M: DL 2000 marker; 1: negative control ; 2: positive control ; 3–42: clinical samples.
表 1 疑似伪狂犬病料收集的来源信息
Table 1 Tissue collection of suspected diseased pigs
地区
Region样本数(份)/来源猪场(个)
Samples/Farms宁德 Ningde 4/2 泉州 Quanzhou 5/3 漳州 Zhangzhou 10/4 南平 Nanping 12/5 龙岩 Longyan 9/4 合计 Total 40/18 表 2 PRV荧光RAA引物与探针
Table 2 Primers and probes of PRV for fluorescent RAA
引物/探针
Primer/Probe引物序列(5'-3')
Sequence(5'-3')用途
UsagePRV-F1 CGATCTACGTGGACGGCATCACGACGCCG 识别并结合到PRV-gE DNA片段的特定区域,启动扩增过程。 PRV-R1 TAGTAGTCCTCGTGCGTGGGCAGGCTGGTGTA PRV-F2 CGAGTACGTCACGGTCATCAAGGAGCTGAC PRV-R2 GCTGGTGTACACCGGAGAGAGCATGTGCGT PRV-Probe GCTGTTTGTGCTGGCGCTGGGCTCCTTCG[FAM-dT]
[THF]A[BHQ1-dT]GACGTGCGTCGTC-C3用于检测和量化扩增过程中产生的特定核酸序列 表 3 荧光重复性试验结果
Table 3 Repeatability of fluorescent RAA
质粒浓度
Plasmid
concentration/
(copies·μL−1)组内变异试验
Intra-assay variability组间变异试验
Inter-assay variability循环数
¯X+SD变异系数CV/% 循环数
¯X+SD变异系数CV/% 1.11×104 16.9±0.33 1.98 17.27±0.77 4.52 1.11×105 15.09±0.34 2.31 12.09±0.49 4.09 1.11×106 9.38±0.25 2.76 8.74±0.30 3.45 -
[1] CHEN Q Y, WU X M, CHE Y L, et al. The immune efficacy of inactivated pseudorabies vaccine prepared from FJ-2012ΔgE/gI strain [J]. Microorganisms, 2022, 10(10): 1880. DOI: 10.3390/microorganisms10101880
[2] HANSON R P. The history of pseudorabies in the United States [J]. Journal of the American Veterinary Medical Association, 1954, 124(925): 259−261.
[3] HU D F, LV L, ZHANG Z D, et al. Seroprevalence and associated risk factors of pseudorabies in Shandong Province of China [J]. Journal of Veterinary Science, 2016, 17(3): 361−368. DOI: 10.4142/jvs.2016.17.3.361
[4] POMERANZ L E, REYNOLDS A E, HENGARTNER C J. Molecular biology of pseudorabies virus: Impact on neurovirology and veterinary medicine [J]. Microbiology and Molecular Biology Reviews: MMBR, 2005, 69(3): 462−500. DOI: 10.1128/MMBR.69.3.462-500.2005
[5] 周仁峰. 猪伪狂犬病病毒特点及分离鉴定 [J]. 畜牧兽医科学(电子版), 2022, (7):72−74. ZHOU R F. Characteristics and isolation and identification of porcine pseudotumor rabies [J]. Graziery Veterinary Sciences: Electronic Version, 2022(7): 72−74. (in Chinese)
[6] ZHANG C L, GUO L H, JIA X R, et al. Construction of a triple gene-deleted Chinese Pseudorabies virus variant and its efficacy study as a vaccine candidate on suckling piglets [J]. Vaccine, 2015, 33(21): 2432−2437. DOI: 10.1016/j.vaccine.2015.03.094
[7] 王刚, 范伟兴, 刘坤, 等. 布鲁氏菌病血清学检测方法优缺点对比 [J]. 中国动物检疫, 2021, 38(5):72−75. WANG G, FAN W X, LIU K, et al. Comparison on the serological detection methods for brucellosis [J]. China Animal Health Inspection, 2021, 38(5): 72−75. (in Chinese)
[8] 王恩惠. 基于RAA-CRISPR/Cas13a的猪伪狂犬病毒检测方法的建立及初步应用[D]. 泰安: 山东农业大学, 2023. WANG E H. Establishment and preliminary application of detection method of porcine pseudorabies virus based on raa-crispr/cas13a[D]. Taian: Shandong Agricultural University, 2023. (in Chinese)
[9] 张众, 王新茹, 殷健, 等. 猪伪狂犬病毒快速检测方法研究进展 [J]. 现代畜牧兽医, 2023, (9):92−96. ZHANG Z, WANG X R, YIN J, et al. Advances in rapid detection methods for porcine pseudorabies virus [J]. Modern Journal of Animal Husbandry and Veterinary Medicine, 2023(9): 92−96. (in Chinese)
[10] SMITH C J, OSBORN A M. Advantages and limitations of quantitative PCR (Q-PCR)-based approaches in microbial ecology [J]. FEMS Microbiology Ecology, 2009, 67(1): 6−20. DOI: 10.1111/j.1574-6941.2008.00629.x
[11] 苏金辉, 邓云贵, 夏冰. 猪伪狂犬病病毒经典毒株与变异毒株双重实时荧光定量PCR方法的建立及应用 [J]. 黑龙江畜牧兽医, 2023, (21):84−89. SU J H, DENG Y G, XIA B. Establishment and application of dual real-time quantitative PCR method for classical and variant strains of porcine pseudorabies virus [J]. Heilongjiang Animal Husbandry and Veterinary Medicine, 2023(21): 84−89. (in Chinese)
[12] FAN X X, LI L, ZHAO Y G, et al. Clinical validation of two recombinase-based isothermal amplification assays (RPA/RAA) for the rapid detection of African swine fever virus [J]. Frontiers in Microbiology, 2020, 11: 1696. DOI: 10.3389/fmicb.2020.01696
[13] ZHANG J, LIU J, AN D, et al. A novel recombinase polymerase amplification assay for rapid detection of epidemic fowl adenovirus [J]. Poultry Science, 2020, 99(12): 6446−6453. DOI: 10.1016/j.psj.2020.08.021
[14] TU F, ZHANG Y N, XU S K, et al. Detection of pseudorabies virus with a real-time recombinase-aided amplification assay [J]. Transboundary and Emerging Diseases, 2022, 69(4): 2266−2274. DOI: 10.1111/tbed.14241
[15] SUN Y, LIANG W, LIU Q Y, et al. Epidemiological and genetic characteristics of swine pseudorabies virus in mainland China between 2012 and 2017 [J]. PeerJ, 2018, 6: e5785. DOI: 10.7717/peerj.5785
[16] 华涛, 唐波, 黄江, 等. 猪伪狂犬病毒Real-time PCR检测方法的建立和弱毒疫苗病毒含量的检测 [J]. 江西农业学报, 2019, 31(9):73−78. HUA T, TANG B, HUANG J, et al. Establishment of real-time PCR assay of pseudorabies virus and viral load detection of PRV attenuated vaccine [J]. Acta Agriculturae Jiangxi, 2019, 31(9): 73−78. (in Chinese)
[17] 施宁雪, 靳晶豪, 陈孝仁. 重组酶聚合酶扩增技术及其在生命科学领域的应用 [J]. 江西农业学报, 2021, 33(10):62−72. SHI N X, JIN J H, CHEN X R. Recombinase polymerase amplification technology and its application in field of life sciences [J]. Acta Agriculturae Jiangxi, 2021, 33(10): 62−72. (in Chinese)
[18] YANG Y, QIN X D, ZHANG W, et al. Development of an isothermal recombinase polymerase amplification assay for rapid detection of pseudorabies virus [J]. Molecular and Cellular Probes, 2017, 33: 32−35. DOI: 10.1016/j.mcp.2017.03.005
[19] 兰德松. 辽宁省PRV的分离鉴定与流行病学调查及PRV新型检测方法的研究与应用[D]. 哈尔滨: 东北农业大学, 2021. LAN D S. Isolation, identification and epidemiological investigation of PRV in Liaoning Province and research and application of new detection method of PRV[D]. Harbin: Northeast Agricultural University, 2021. (in Chinese)
[20] 汪一平, 游一, 李天宇, 等. 豫西地区猪伪狂犬病的分子流行病学调查与病毒分离鉴定 [J]. 畜牧与兽医, 2021, 53(9):95−102. WANG Y P, YOU Y, LI T Y, et al. Molecular epidemiological investigation of swine pseudorabies and virus identification in western Henan Province [J]. Animal Husbandry & Veterinary Medicine, 2021, 53(9): 95−102. (in Chinese)
-
期刊类型引用(5)
1. 王沛然,张家林,高祥斌,涂佳才. 配比施肥对‘聊红’椿幼苗生长及光合特性的影响. 山东林业科技. 2024(02): 30-36+7 .  百度学术
百度学术
2. 赵美荣,李永春,李春颖. 臭椿canthin-6-one对禾谷镰刀菌的抑菌作用. 湖北农业科学. 2024(09): 84-88 .  百度学术
百度学术
3. 李永春,赵美荣. 臭椿canthin-6-one对黄瓜幼苗生长生理的影响. 赤峰学院学报(自然科学版). 2022(09): 17-20 .  百度学术
百度学术
4. 张蔓蔓,郑聪慧,刘春鹏,徐振华,杜克久. 臭椿的研究进展与展望. 河北林业科技. 2021(02): 49-53 .  百度学术
百度学术
5. 胥鑫萌,童天娇,刘伟,刘军海. 天然植物源的抑菌活性及在洗涤中的应用现状. 中国洗涤用品工业. 2021(09): 73-78 .  百度学术
百度学术
其他类型引用(3)




 下载:
下载: