Propagating Stropharia rugosoannulata in Liquid Medium
-
摘要:目的 优化大球盖菇液体菌种培养基,探究液体培养过程中的生长规律,确立液体菌种繁育栽培种工艺参数。方法 以大球盖菇8号为试验菌株,以菌丝体生物量为评价指标,采用单因素和正交试验L9(34)优化液体菌种培养基。测定液体菌种菌丝体生物量,还原糖和氨基氮含量,羧甲基纤维素酶、淀粉酶、酸性蛋白酶、漆酶胞外酶酶活生理生化指标,确立优化配方的液体菌种最优培养时间。以平均满袋时间为指标,确立液体菌种扩繁栽培种接种量、培养基配方颗粒度和碳氮比。结果 优化得到大球盖菇液体菌种最优配方为葡萄糖20 g·L−1、小麦粉30 g·L−1、酵母粉0.75 g·L−1、磷酸二氢钾1.00 g·L−1、硫酸镁0.50 g·L−1、起始pH 5。培养第8 天时,大球盖菇菌丝体生物量最大,为1.66 g·hmL−1;液体培养过程中还原糖含量由12.23 mg·mL−1降至1.38 mg·mL−1,氨基氮含量由0.09 mg·mL−1降至0.06 mg·mL−1;羧甲基纤维素酶和淀粉酶酶活在第4 天最高,酶活分别为6.49 、5.16 U,酸性蛋白酶酶活在第2 天 最高,酶活为1.80 U,漆酶酶活在第6 天 最大,酶活为1.63 U。液体菌种扩繁栽培种生产工艺参数:接种量为15 mL,菌包培养基配方颗粒度的粗细木屑比为7∶3,碳氮比为50∶1。结论 大球盖菇液体菌种活性与上述指标具有一定的相关性,结合发酵液生理生化指标,判定第7天的液体菌种活力最高。利用大球盖菇液体菌种扩繁栽培种,平均满袋时间为23.7 d,缩短生长周期2.7 d。本研究建立配套的制种工艺,为大球盖菇栽培种工厂化生产技术奠定基础。Abstract:Objective PropagatingStropharia rugosoannulata in liquid culture medium was studied.Methods S. rugosoannulata No. 8 was cultivated in experimental media to determine the mycelial biomass increase in a single factor and orthogonal test L9(34) for formulation and culture conditions optimization. Mycelial biomass, reducing sugars, and amino nitrogen content as well as the extracellular enzyme activities of carboxymethyl cellulase, amylase, acid protease, and laccase of the culture were monitored to determine cultivation end point. Average full-bag filling time was used as indicator for the inoculation amount, substrate particle size, and carbon-to-nitrogen ratio in a maximized reproduction and yield.Results The optimized liquid culture medium was formulated with 20 g·L−1 glucose, 30 g·L−1 wheat flour, 0.75 g·L−1 yeast powder, 1.00 g·L−1 potassium dihydrogen phosphate, and 0.50 g·L−1 magnesium sulfate at an initial pH of 5. On the 8th day of culture, the mycelial biomass reached a maximum at 1.66 g·h mL−1. As the mycelia grew, the reducing sugar in the medium decreased from 12.23 mg·mL−1 to 1.38 mg·mL−1 and the amino nitrogen from 0.09 mg·L−1 to 0.06 mg·L−1 during the culture process. The activities of carboxymethyl cellulase and amylase were the highest on the 4th day with the activities of 6.49 U and 5.16 U, respectively. The activity of acid protease peaked at 1.80 U on the 2nd day; and that of laccase, at 1.63 U on the 6th day. The inoculum production was best carried out with an inoculation of 15 mL, a coarse-to-fine ratio of 7∶3 on the substrate particle size, and a carbon-to-nitrogen ratio of 50∶1.Conclusion Since the viability of the mushroom propagation correlated with some of the physiological and biochemical indicators of the liquid medium, 7 d was determined to be the peak for the cultivation. For filling a hyphal bag, 23.7d of culture was required, which was 2.7d shorter than what needed without the optimization. The results provided the basis for the development of a scale-up industrial operation.
-
Keywords:
- Stropharia rugosoannulata /
- liquid culture /
- medium /
- optimization /
- application
-
0. 引 言
【研究意义】大球盖菇(Stropharia rugosoannulata)又称皱环球盖菇、酒红球盖菇,商品名称赤松茸,红松茸、彩云菇,隶属担子菌门(Basidomycota),层菌纲(Hymenomycetes),伞菌目(Agaricales),球盖菇科(Strophariaceae),球盖菇属(Stropharia)[1]。大球盖菇是欧美各国人工栽培的著名食用菌之一,也是联合国粮农组织(FAO)向发展中国家推荐栽培的食用菌之一[2],因其色泽艳丽,美味爽口,营养丰富,深受广大消费者喜爱。据中国食用菌协会最新统计数据显示,2021年大球盖菇的产量超过21万t[3]。目前,大球盖菇主要有稻田生态栽培、林下生态栽培及大棚设施栽培3种栽培模式[4−5]。由于设施化栽培参数可控,大球盖菇品质较高,增加栽培效益,越来越多种植企业尝试大球盖菇工厂化栽培试验。菌种制作是食用菌栽培的首道工序,菌种质量尤为重要,关系栽培成败。目前大球盖菇制种仍沿用传统的固体菌种生产工艺,制备原种或栽培种时,一般需要 2~3个月甚至更长时间。通过产业调研发现,大球盖菇菌种多为小作坊制种模式生产,由于采用固体菌种扩繁栽培种时间长、制种工艺不规范等问题,造成菌种质量不稳定,严重制约大球盖菇产业发展。相对固体菌种,液体菌种具有培养时间短、萌发快、菌龄整齐一致、接种方便等优点,利于食用菌自动化、工厂化、规模化生产。近年来,液体菌种被广泛地应用在工厂化食用菌生产,如金针菇、杏鲍菇、海鲜菇,与自动化接种设备相结合,推动了食用菌产业的快速发展。大球盖菇液体菌种繁育技术的研究对提高大球盖菇制种自动化、工厂化生产水平,缩短栽培种培养时间,规范制种工艺,提高菌种质量具有重要意义。【前人研究进展】前人对大球盖菇的研究主要集中在栽培技术[4−6]和药理活性物质[7−10]方面。在液体菌种方面,李正鹏等[11]对大球盖菇液体菌种培养条件进行了研究,曾健勇等[12]利用磁化水培养提高大球盖菇菌丝生长速度、营养物质含量和酶活性,从而缩短大球盖菇原种制种周期。付婧璇等[13]在香蒲资源化开发中对大球盖菇液体菌种的制备与应用进行研究,使香蒲成为栽培菌类的新型基质。刘克芳等[14]优化了玉米面、黄豆面和稻壳浸出液为主要组分的大球盖菇液体菌种培养基配方。杜瑞垚[15]进行大球盖菇菌丝液体培养的原料筛选,并对液体培养基的配方进行优化,筛选出适合液体菌种固化培养的原料玉米芯,确定了利用液体菌种制作固态栽培种的关键工艺。【本研究切入点】虽然前人对大球盖菇液体菌种培养基和培养条件有一定的研究报道,但目前尚未掌握大球盖菇液体培养过程中生理生化变化规律,对利用液体菌种作为原种扩繁栽培种工艺参数尚不完善。【拟解决的关键问题】采用单因素法筛选出合适的碳、氮源,再用正交试验法进行液体菌种培养基配方优化;对液体菌种发酵过程中的菌丝体生物量、还原糖和氨基氮含量、胞外酶活性等主要生理指标进行测定分析,判断培养终点;使用经优化培养基培养获得的大球盖菇液体菌种进行扩繁栽培种试验,以菌丝满袋时间为指标,对制种过程中的最佳接种量、栽培种基质颗粒度和碳氮比进行探究,以期建立适用于大球盖菇工厂化生产的培养基配方及配套的制种工艺流程,为大球盖菇栽培种工厂化生产技术提供理论依据。
1. 材料与方法
1.1 试验材料
1.1.1 供试菌株
大球盖菇(Stropharia rugosoannulata)8号,由福建省农业科学院食用菌研究所育种室提供。
1.1.2 试验试剂
葡萄糖、蔗糖(分析纯,天津市科密欧化学试剂有限公司);硫酸镁、磷酸二氢钾、氢氧化钠、盐酸(分析纯,西陇化工股份有限公司);酵母粉、蛋白胨、牛肉膏(生化试剂,广东环凯微生物科技有限公司);麦芽汁,生化试剂(广州康凯信生物科技有限公司);小麦粉(规格200目)、玉米粉(规格200目)、小米粉(规格200目)、玉米淀粉、黄豆粉、麸皮(含碳量42.48%,含氮量2.71%)、轻质碳酸钙、粗木屑(规格长5~10 mm,宽2~3 mm,厚1~2 mm)、细木屑(规格长2~5 mm,宽1~2 mm,厚0.5~1 mm)、花生粕(含碳量47.71%,含氮量9.03%)购自福州市场。
1.1.3 主要仪器
恒温摇床 BSD-YX2200、洁净工作台 SW-CJ2F、奥豪斯pH计 STARTER3100、紫外分光光度计 UV1300、生化培养箱 SPX-250B-Z、电子分析天平 FA1104。
1.1.4 基础培养基
小麦粉 20 g·L−1,酵母粉3 g·L−1,磷酸二氢钾2 g·L−1,硫酸镁0.75 g·L−1,pH自然。
1.1.5 大球盖菇母种
按配方杂木屑粉末(规格100目)80%、麸皮19%、轻质碳酸钙1%、含水量65%,制备菌种。
1.1.6 大球盖菇原种
按配方杂木屑(粗、细木屑按质量比7∶3)80%,麸皮19%,轻质碳酸钙1%,含水量65%,配制培养基,装入750 mL玻璃瓶中,置于高压灭菌锅中高温126 ℃,灭菌2.5 h,冷却后接入大球盖菇母种,置于24 ℃培养箱,菌丝满瓶后备用。
1.2 试验方法
1.2.1 碳氮源筛选单因素试验
根据基础培养基配方,在碳源筛选试验时,配方中的碳源小麦粉,分别用葡萄糖、蔗糖、玉米粉、小米粉、玉米淀粉替换;在氮源筛选试验时,配方中的氮源酵母粉,分别用蛋白胨、牛肉膏、麦芽汁、黄豆粉、麸皮替换,配制不同碳氮源液体培养基,经121 ℃高温灭菌20 min冷却后,在超净工作台无菌操作接入大球盖菇母种0.5 g,后置于恒温摇床24 ℃,150 r·min−1培养8 d,分别收集菌丝体,置于电热干燥箱烘干至恒重,电子天平称重,分别记录菌丝体生物量。
1.2.2 液体培养基正交试验
参考前人的研究,在单因素试验的基础上,固定无机盐KH2PO4 1.0 g·L−1,MgSO4·7H2O 0.5 g·L−1添加量,以葡萄糖(A)、小麦粉(B)、酵母粉(C)和起始pH(D)为自变量,用L9(34)正交表安排正交试验,考察4个因素对大球盖菇菌丝体生物量为指标的影响,因素水平如表1所示。
表 1 正交试验因素和水平Table 1. Orthogonal factors and levels on factors affecting mycelial biomass水平
Levels因素 Factors/(g·L−1) A葡萄糖
A GlucoseB小麦粉
B Wheat flourC酵母粉
C Yeast powderD 起始pH
D Initial pH1 10 20 0.75 5 2 15 25 1.00 6 3 20 30 1.25 7 1.2.3 指标测定
(1)还原糖含量的测量。取不同培养时间的培养液,采用DNS法[16] 测定还原糖含量,重复3次,取平均数。
(2)氨基氮含量的测量。取不同培养时间的培养液,采用茚三酮比色法[17]测定氨基氮含量,重复3 次,取平均数。
(3)胞外酶活的测定。羧甲基纤维素酶、淀粉酶、酸性蛋白酶、漆酶活性测定及定义参考文献[18]。
(4)液体原种扩繁栽培种工艺参数研究。将优化配方发酵培养的大球盖菇液体菌种作为原种扩繁栽培种,培养基按照不同颗粒度、碳氮比(表2)参数配制,含水量60%,培养基500 g装入规格菌袋(15 cm × 30 cm × 0.05 cm),中间打孔至离菌包底部1~2 cm,经126 ℃高温灭菌150 min冷却后,接入相应量的液体菌种,置于24 ℃培养箱,记录菌丝满袋时间。
表 2 不同碳氮比的菌包培养基配方Table 2. Culture media with varied carbon-nitrogen ratio in bag编号
No.杂木屑
Wood
chips/%麸皮
Wheat
bran/%花生粕
Peanut
meal/%碳酸钙
calcium
carbonate/%碳氮比
Carbon
nitrogen
ratio1 83 14 2 1 70∶1 2 81 14 4 1 60∶1 3 80 14 5 1 50∶1 4 77 14 8 1 40∶1 5 73 14 12 1 30∶1 1.3 数据统计与分析
试验数据采用Excel进行统计整理、标准差分析和作图。
2. 结果与分析
2.1 液体培养基单因素筛选试验结果
2.1.1 不同碳源对大球盖菇菌丝体生物量的影响
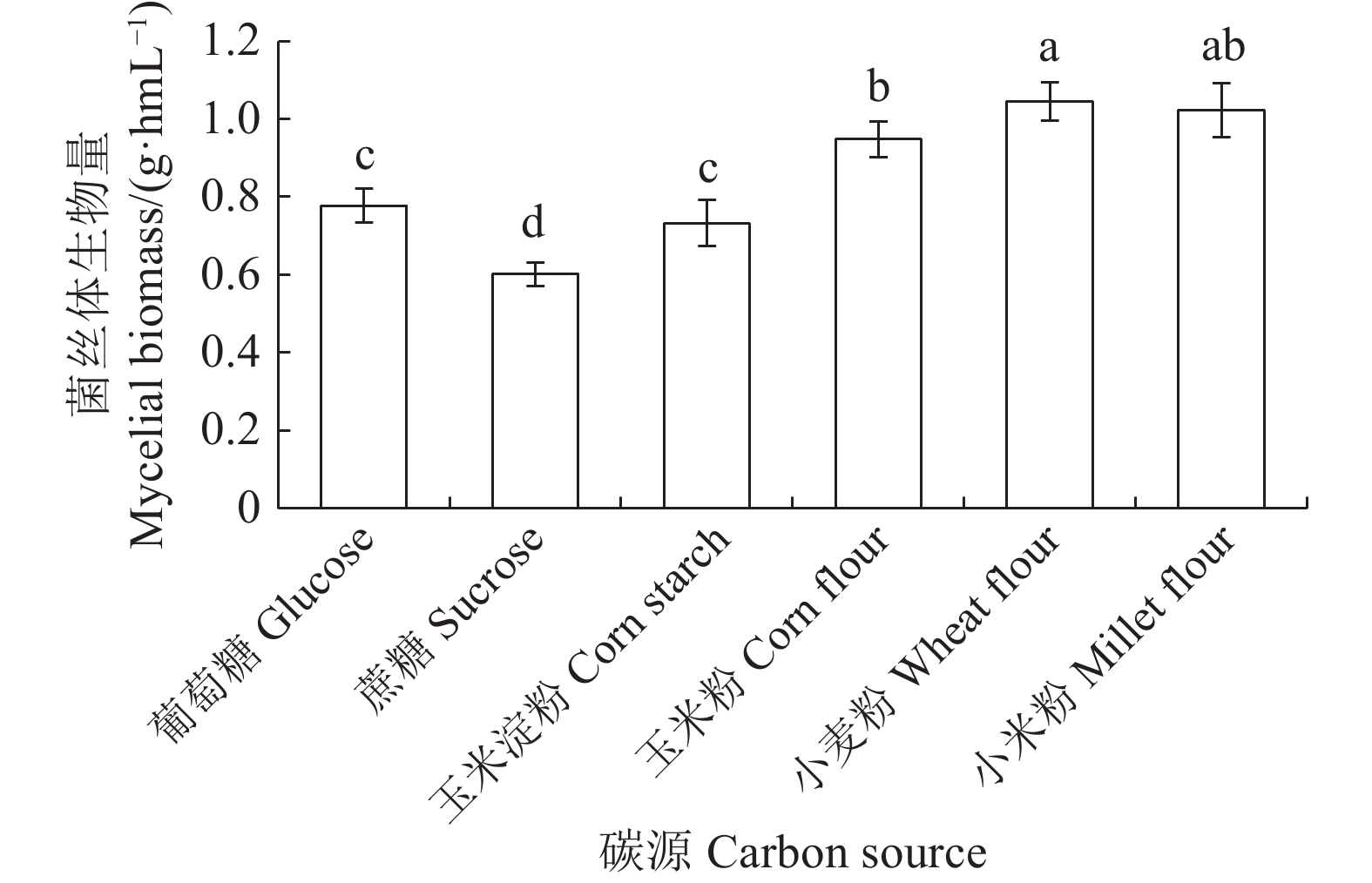
采用单因素试验,选取葡萄糖、蔗糖、玉米淀粉、玉米粉、小麦粉、小米粉,筛选大球盖菇液体培养基最优碳源。由图1可知,大球盖菇对碳源的利用较为广泛,对所有供试碳源均可利用,当碳源为蔗糖时,菌丝体生物量最小,为0.60 g·hmL−1;当碳源为小麦粉和小米粉时,菌丝体生物量较大,分别为1.05 g·hmL−1、1.02 g·hmL−1,两者差异不显著(P>0.05),考虑到小米粉成本较高,因此选择小麦粉作为最优碳源。
2.1.2 不同氮源对大球盖菇菌丝体生物量的影响
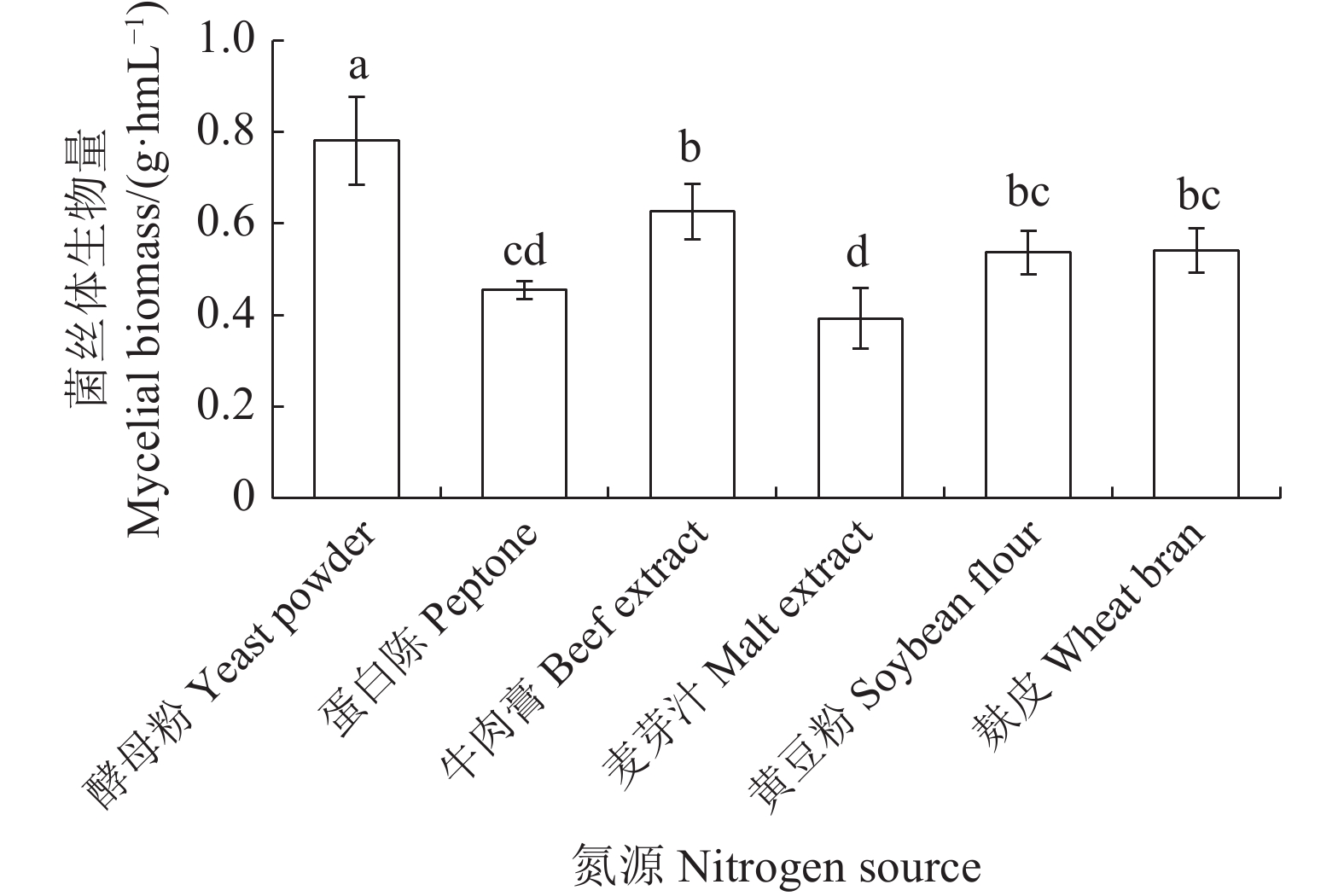
采用单因素试验,选取酵母粉、蛋白胨、牛肉膏、麦芽汁、黄豆粉和麸皮为氮源,筛选大球盖菇液体培养基最优氮源。由图2可知,大球盖菇对供试所有氮源均可利用,其中酵母粉是大球盖菇最优氮源,菌丝体生物量最大,达0.78 g·hmL−1,与其他氮源相比,差异显著(P<0.05);其次是牛肉膏、麸皮、黄豆粉,对麦芽汁和蛋白胨利用较差,菌丝体生物量分别为0.39、0.46 g·hmL−1。因此,考虑氮源的利用情况,选择酵母粉作为最优氮源。
2.1.3 小麦粉添加量对大球盖菇菌丝体生物量的影响
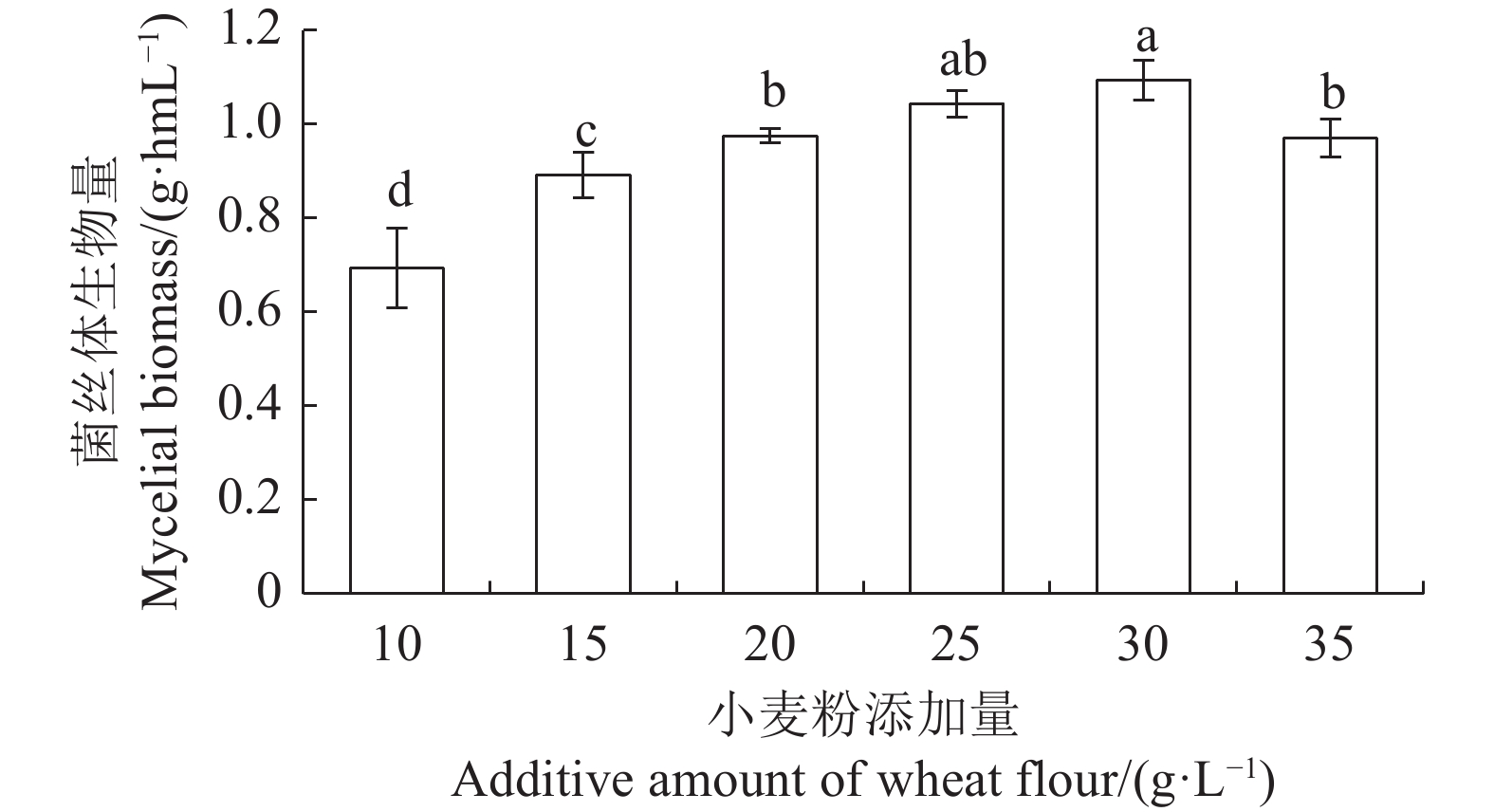
按照基础培养基配方,分别配制10、15、20、25、30、35 g·L−1不同小麦粉添加量的液体培养基,考察小麦粉添加量对菌丝体生物量的影响,试验结果如图3所示,小麦粉添加量为10~30 g·L−1时随着小麦粉添加量的增加,菌丝体生物量逐渐增大,其中小麦粉添加量为30 g·L−1时,菌丝体生物量最大,为1.09 g·hmL−1。小麦粉添加量为35 g·L−1时,菌丝体生物量减少。因此,确立小麦粉的添加量25 g·L−1进行优化。
2.1.4 酵母粉添加量对大球盖菇菌丝体生物量的影响
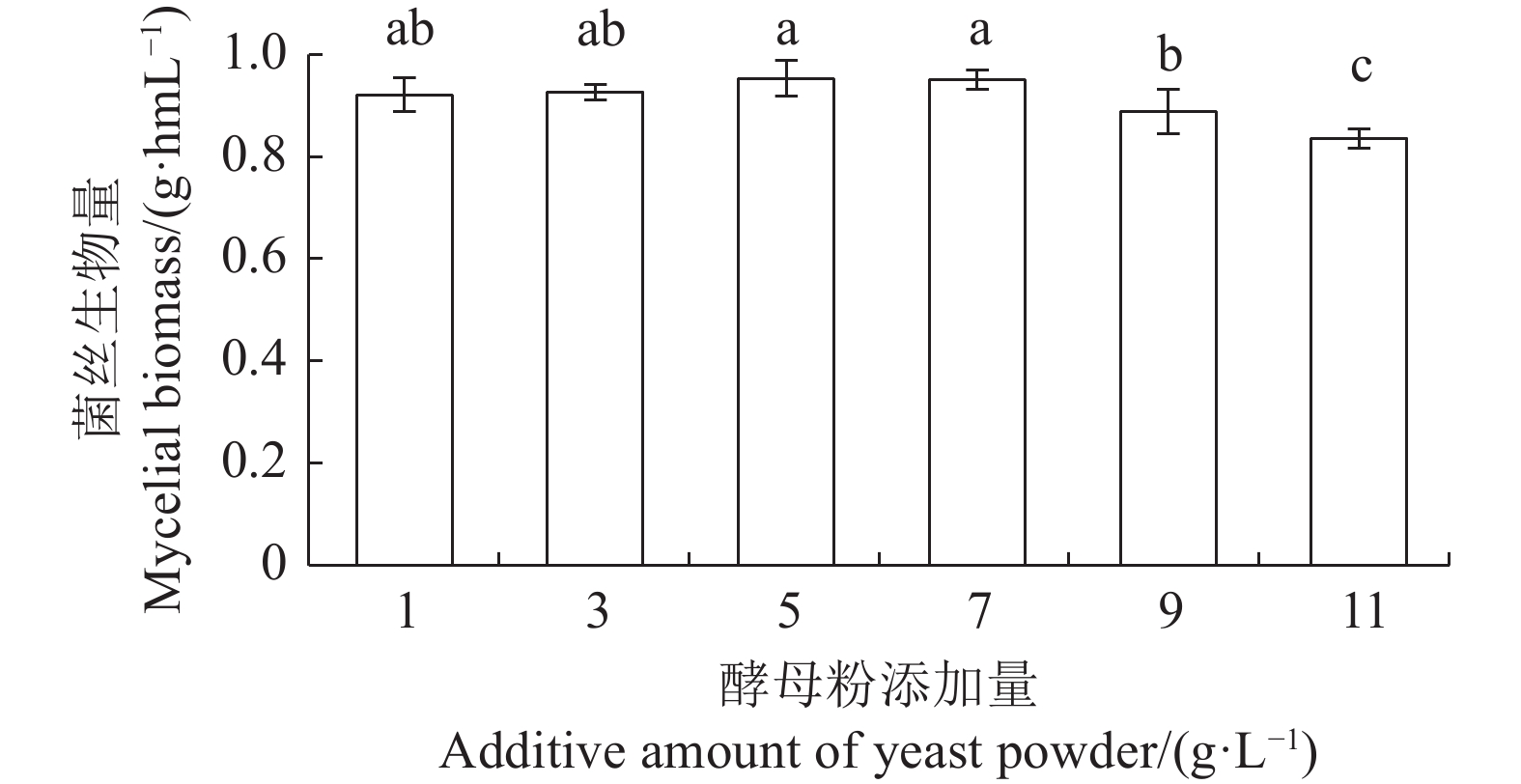
按照基础培养基配方,分别配制1、3、5、7、9、11 g·L−1不同酵母粉添加量的液体培养基,考察酵母粉添加量对菌丝体生物量的影响,如图4可知,当酵母粉添加量为1、3、5 g·L−1时,随着酵母粉添加量增加,菌丝体生物量逐渐增大,最大达0.95 g·hmL−1,但三者差异不显著(P>0.05);当酵母粉添加量7、9、11 g·L−1时,菌丝体生物量随着酵母粉添加量增加而逐渐减少,三者差异显著(P<0.05)。考虑培养基配方的经济性,确立酵母粉的添加量为1 g·L−1进行优化。
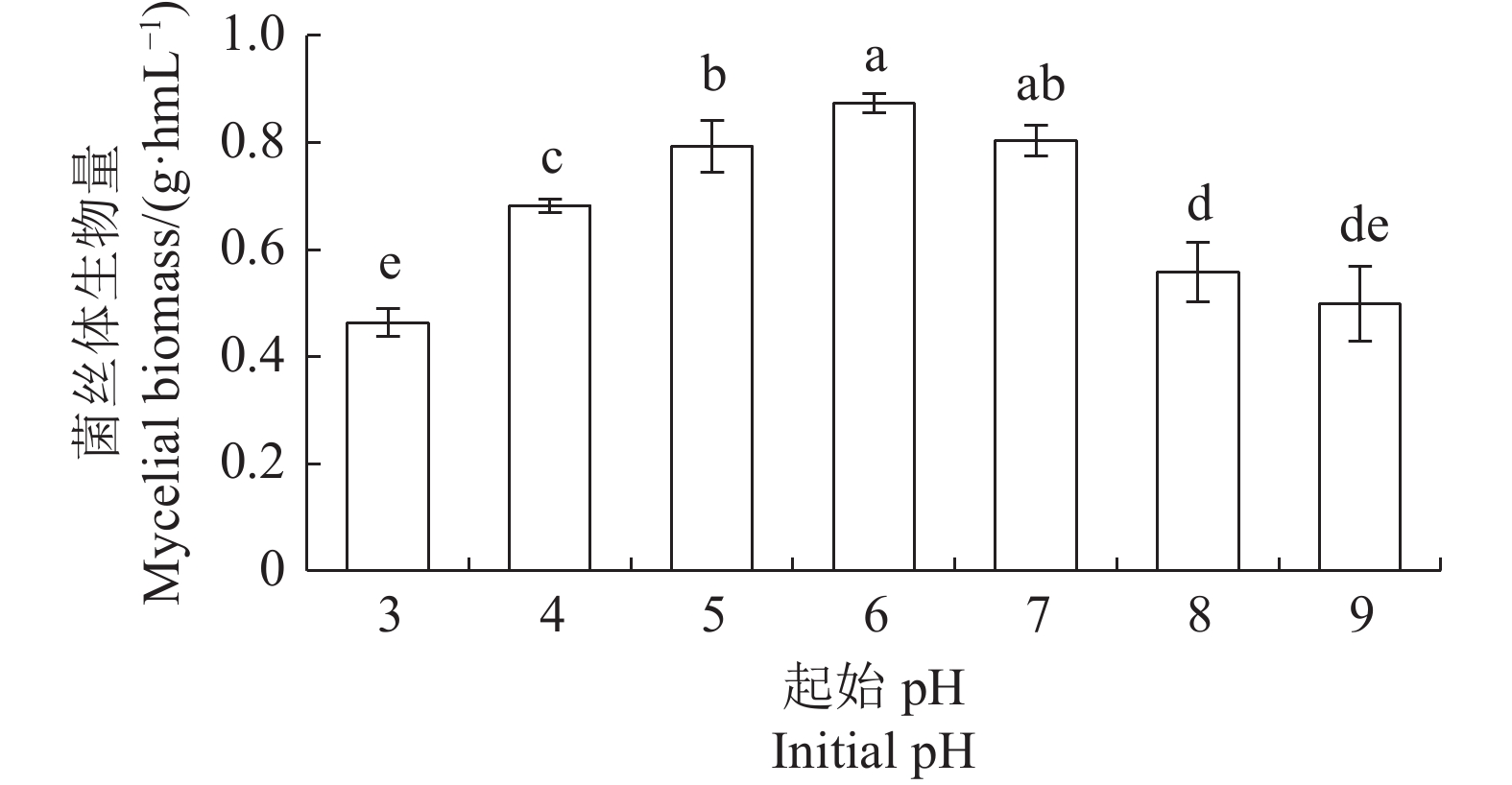
2.1.5 起始pH对大球盖菇菌丝体生物量的影响
pH影响菌丝体胞外酶活性,是食用菌液体培养过程中关键因素。按照基础培养基配方,用1 mol·L−1盐酸或1 mol·L−1氢氧化钠溶液调制pH,配制起始pH分别为3、4、5、6、7、8、9的液体培养基,考察起始pH对菌丝体生物量的影响,试验结果如图5所示,起始pH为3~9,菌丝体均可生长,其中起始pH为6时,菌丝体生物量最大,达0.87 g·hmL−1。因此,选择起始pH为6进行优化。
2.2 培养基优化试验结果
基于大球盖菇菌丝体生物量为指标的正交试验设计及结果(表3),试验号9的菌丝体生物量最大,为1.59 g·hmL−1,试验号2的菌丝体生物量最小,为1.12 g·hmL−1,两组间的差异较大。根据极差分析 R 值大小,各因素对大球盖菇菌丝体生物量影响主次顺序为: 葡萄糖(A)>小麦粉(B)>起始pH(D)>酵母粉(C)。表4为方差分析结果,可知配方中葡萄糖、小麦粉、酵母粉、起始pH都对菌丝生物量具有显著性的影响。根据极差分析原理,从表4中各因素k值可知,大球盖菇液体菌种培养基优化配方组合是A3B3C1D1,即葡萄糖20 g·L−1、小麦粉30 g·L−1、酵母粉0.75 g·L−1、起始pH 5。
表 3 培养基优化的正交试验结果Table 3. Orthogonal experiment results and range analysis for medium optimization试验号
No.因素 Factors 菌丝体
生物量
Mycelial
biomass/
( g·hmL-1)A葡萄糖
A GlucoseB小麦粉
B Wheat
flourC酵母粉
C Yeast
powderD起始pH
D Initial
pH1 1 1 1 1 1.23 2 1 2 3 3 1.12 3 1 3 2 2 1.29 4 2 1 3 2 1.18 5 2 2 2 1 1.34 6 2 3 1 3 1.44 7 3 1 2 3 1.28 8 3 2 1 2 1.56 9 3 3 3 1 1.59 K1j 3.64 3.68 4.23 4.17 K2j 3.96 4.02 3.91 4.03 K3j 4.43 4.33 3.89 3.84 k1j 1.21 1.23 1.41 1.39 k 2j 1.32 1.34 1.30 1.34 k 3j 1.48 1.44 1.30 1.28 极差 R 0.26 0.21 0.12 0.11 优化水平
Optimal level3 3 1 1 表 4 正交试验方差分析Table 4. Variance analysis on orthogonal experiment results方差来源
Source平方和
Sum of
squares自由度
Degree of
freedom均方
Mean squareF值
F value显著性
SignificanceA葡萄糖 0.41 2 0.20 80.13 ** B小麦粉 0.28 2 0.14 54.28 ** C酵母粉 0.06 2 0.03 11.01 ** D起始 pH 0.09 2 0.05 18.39 ** 误差 Error 0.05 18 0.01 总和 Sum 49.92 27 **表示差异显著(P<0.01)。
**means significant differences at P<0.01.2.3 菌丝体在优化培养基中的生理生化变化规律
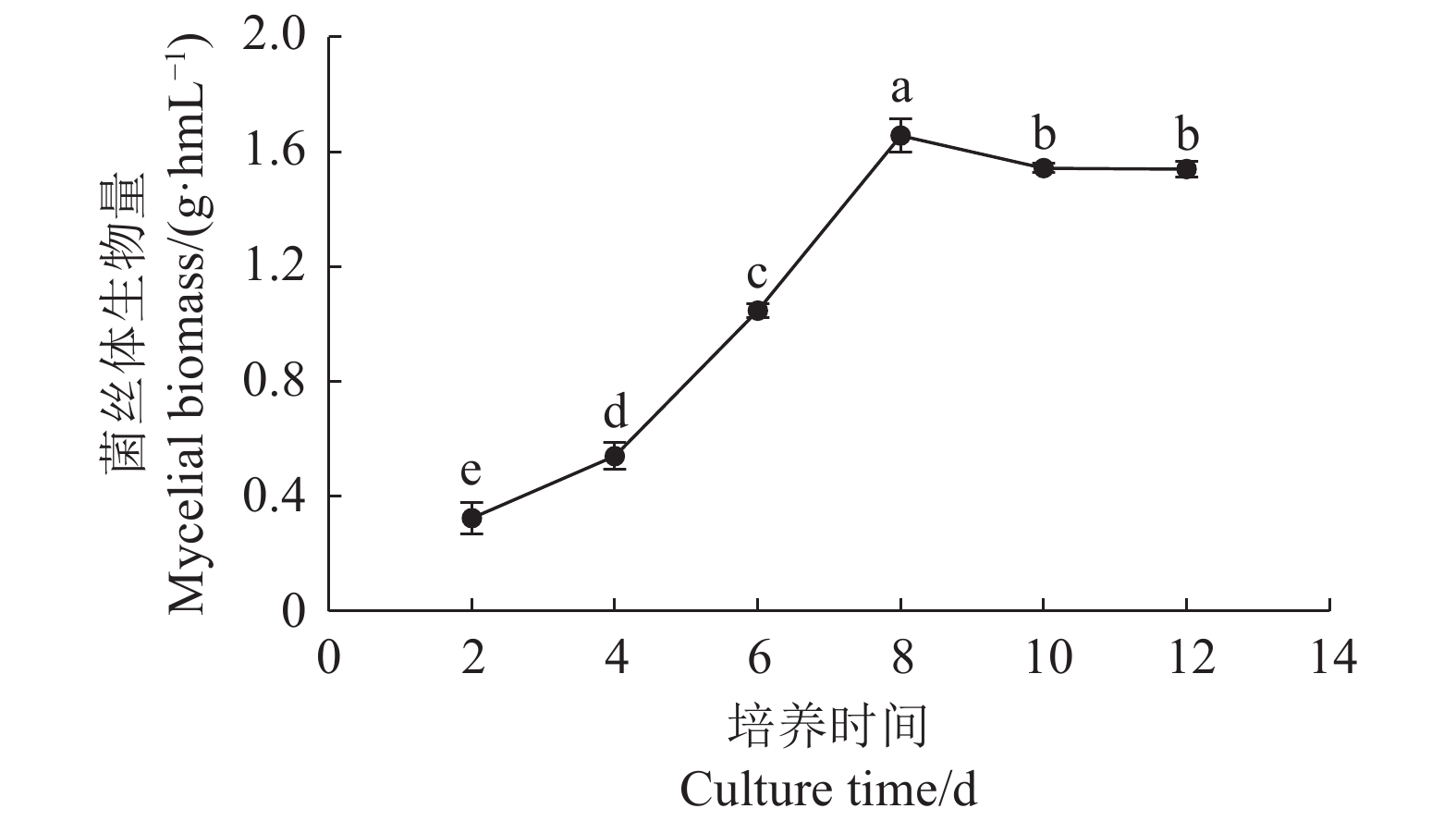
2.3.1 菌丝体生物量变化情况
采用正交优化的培养基进行发酵培养 2、4、6、8、10、12 d ,分别测量不同培养时间菌丝体干重生物量。由图6可知,培养时间0~4 d 菌丝体生物量增长缓慢;培养至 4~6 d,随着菌丝片段不断增多,菌丝体增长旺盛。培养至第 8天菌丝体生物量达到最高峰,为1.66 g·hmL−1,高于正交试验中的最大值(试验号9的1.59 g·hmL−1)。因此,极差分析获得的优化配方即为最优配方。
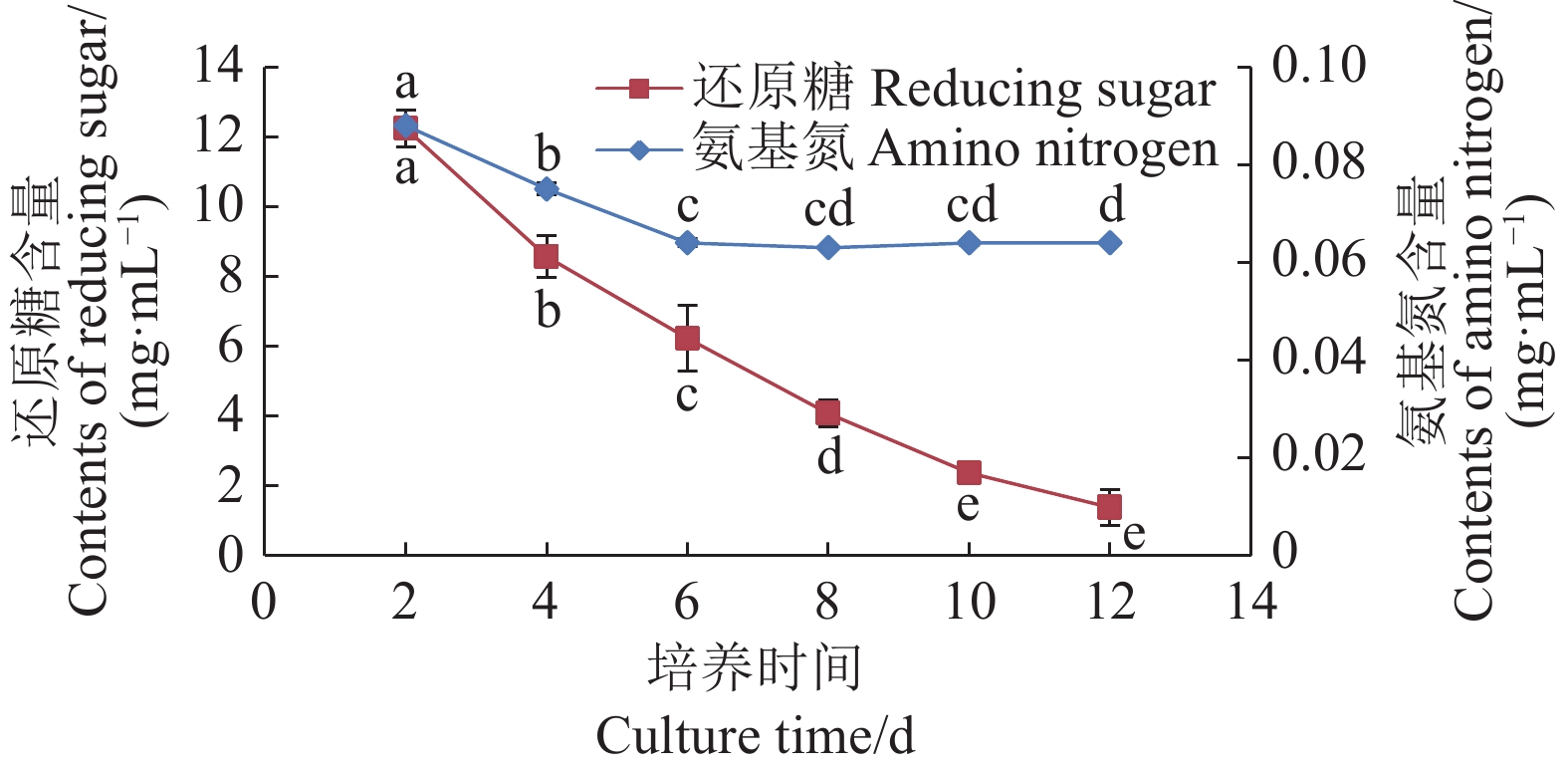
2.3.2 还原糖和氨基氮含量变化情况
发酵培养液还原糖和氨基氮含量变化分别反映菌丝体对碳氮源的代谢情况,绘制培养液还原糖和氨基氮含量的变化曲线如图7所示,培养时间 2~12 d,随着培养时间增加,还原糖含量由12.23 mg·mL−1降至1.38 mg·mL−1,呈不断下降趋势,表明大球盖菇菌丝体对碳源良好利用。培养时间 2~6 d,氨基氮含量由0.09 mg·mL−1降至0.06 mg·mL−1,菌丝体主要利用培养液中的原始氨基氮,代谢消耗培养液中的原始氨基氮大于分解培养液中氮源物质生成的氨基氮,表现为氨基氮含量不断下降趋势;培养时间6~12 d,代谢消耗培养液中的原始氨基氮与分解培养液中氮源物质生成的氨基氮达到动态平衡,表现为培养液氨基氮含量维持稳定。
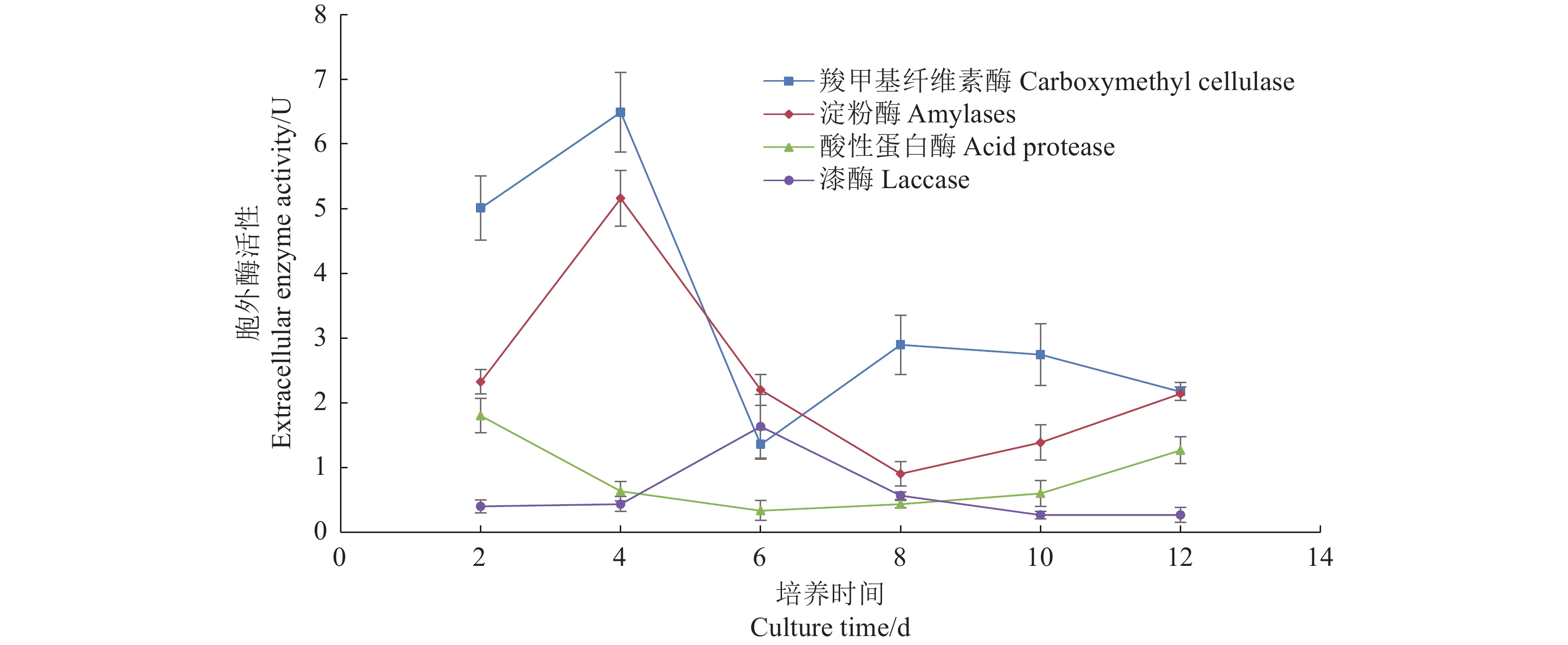
2.3.3 胞外酶活性变化情况
分别测定培养2、4、6、8、10、12 d时培养液中羧甲基纤维素酶、淀粉酶、酸性蛋白酶和漆酶的活性,绘制大球盖菇液体菌种生长过程中胞外酶活性变化曲线。结果(图8)表明,在培养时间0~4 d,随着菌丝体生物量不断增加,菌丝体分泌的胞外酶酶活逐渐增加,其中羧甲基纤维素酶和淀粉酶酶活在第4天达到峰值,酶活分别为6.49 、5.16 U,羧甲基纤维素酶活性在第6天最低,为1.36 U,第8 天上升至2.90 U,随后逐渐降低至2.17 U;淀粉酶酶活在第8 天最低,为0.90 U,随后逐渐升高至2.14 U。羧甲基纤维素酶和淀粉酶活性变化情况反映菌丝体碳代谢情况,结合培养液还原糖含量变化情况,判定菌丝体活力在培养第6~8 天较好。酸性蛋白酶活性在第2天最大,酶活为1.80 U,第6天最小,酶活为0.33 U,第6 ~12天,酸性蛋白酶酶活又逐渐升高至1.27 U。漆酶酶活在培养时间0~6 d逐渐升高,至第6天最大,酶活为1.63 U,随后第6 ~12天,酶活又逐渐降低至0.27 U。
2.4 大球盖菇液体菌种应用研究
2.4.1 液体原种与固体原种扩繁栽培种对比
分别将大球盖菇15 mL液体原种和15 g固体原种接入菌包中,每个处理接种10袋,比较2种菌种扩繁栽培种平均满袋时间。结果表明,液体原种扩繁栽培种平均满袋时间为23.7 d,较固体原种扩繁栽培种平均满袋时间26.4 d缩短2.7 d,两者差异显著( P<0.05)。由图9可知,由于液体原种的流动性,其菌丝体更均匀地分散在菌包接菌孔和底部,因此采用液体原种扩繁栽培种的菌丝走菌速度优于固体原种。
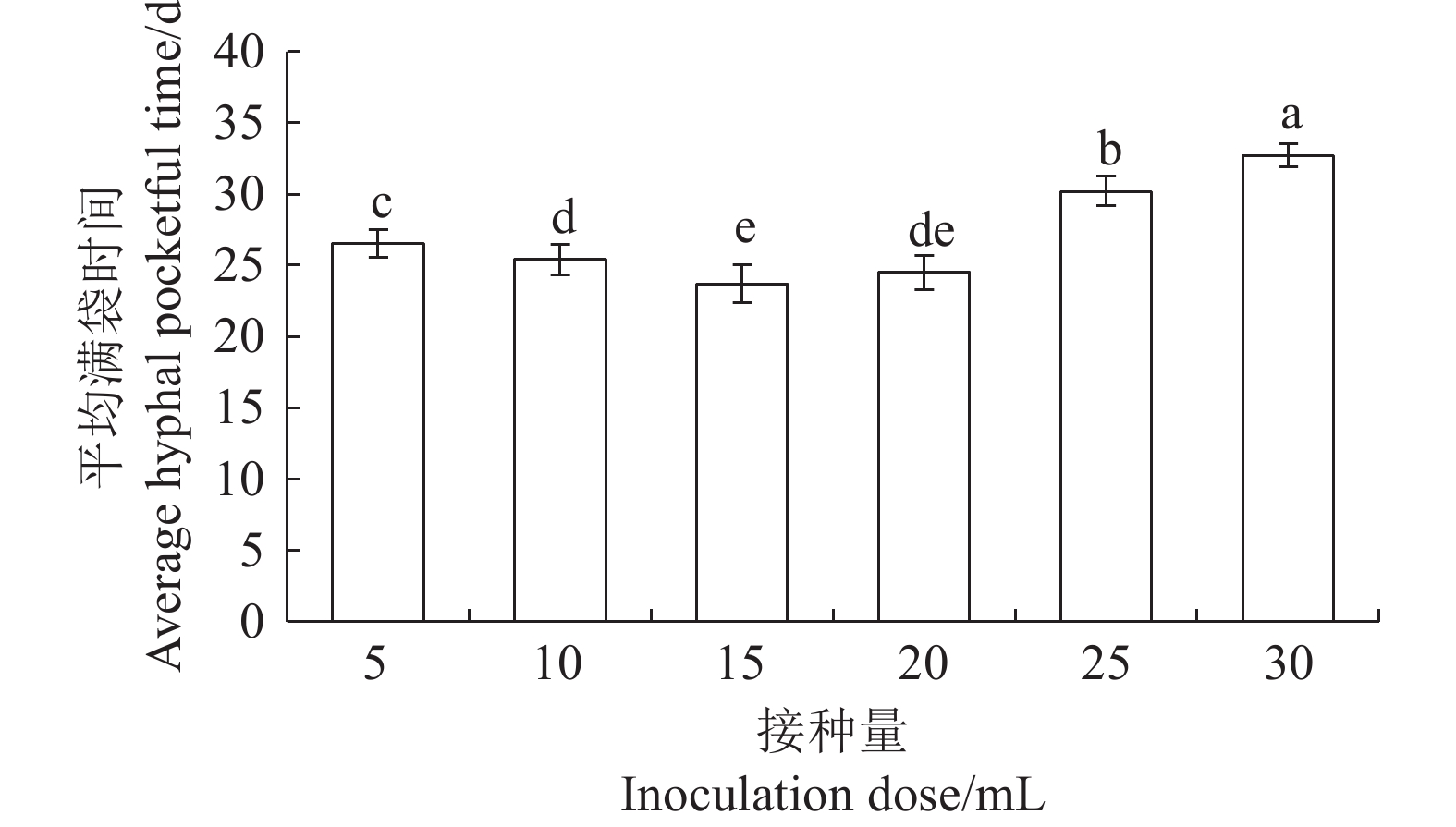
2.4.2 不同接种量对菌包满袋时间的影响
按照接种量5、10、15、20、25、30 mL向菌包接入大球盖菇液体菌种,每个处理接种10袋,比较不同接种量对栽培种平均满袋时间的影响。由图10可知,在接种量5~15 mL,随着接种量增加,平均满袋时间逐渐减少,当接种量15 mL,平均满袋时间最短,与其他接种量比较差异显著( P<0.05);在接种量20~30 mL,随着的接种量增加,平均满袋时间逐渐增长,由于接种量增大,造成菌包中培养基含水量增加,甚至菌包底部积液,影响培养基的透气性,菌丝走菌速度减小,导致平均满袋时间增长。因此,选择15 mL作为扩繁大球盖菇栽培种所需的接种量。
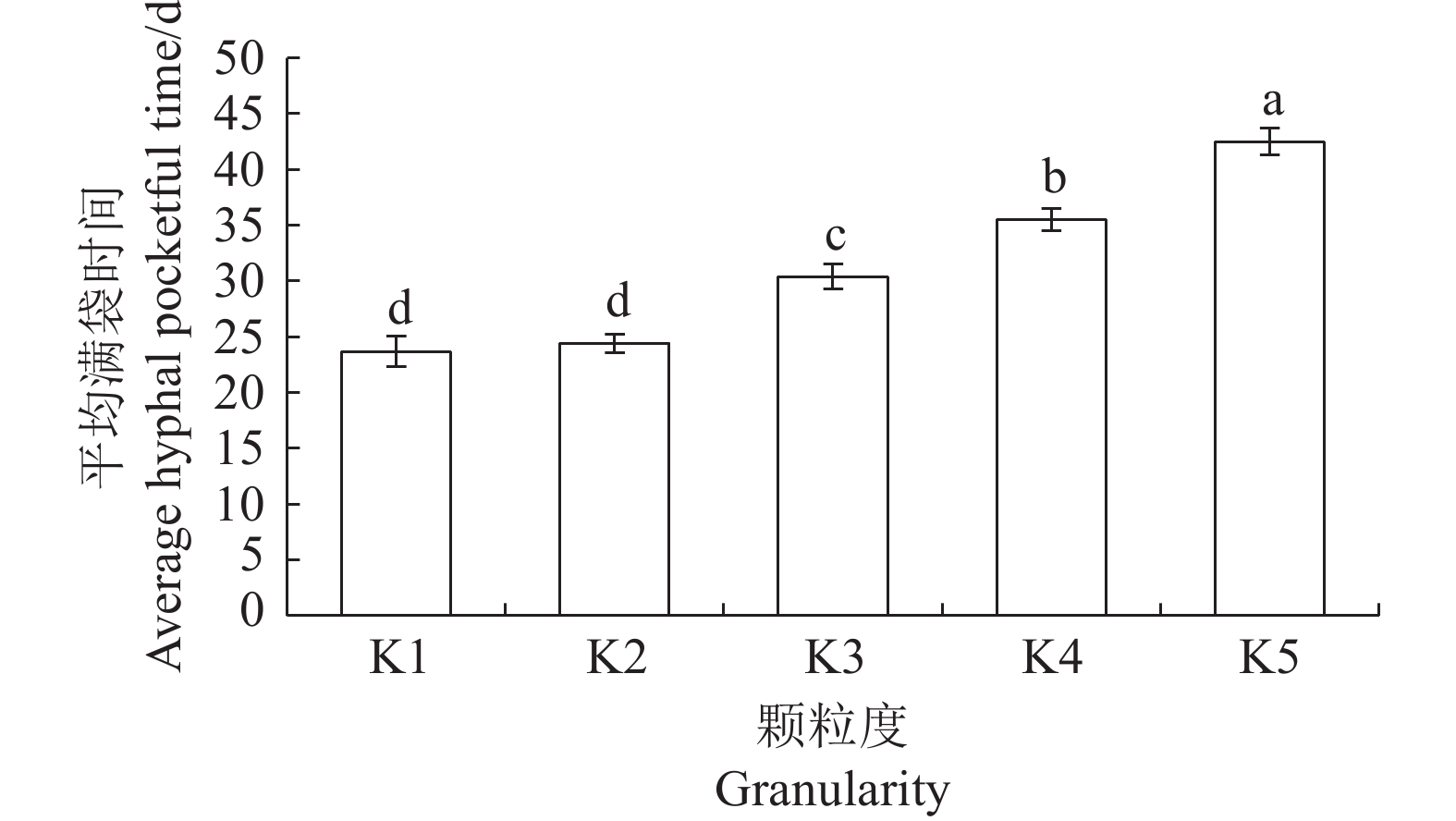
2.4.3 栽培种培养基颗粒度对菌包满袋时间的影响
将粗、细木屑按照质量比10∶0、7∶3、5∶5、3∶7、0∶10比例,配制不同颗粒度的栽培种培养基,分别标记为K1~K5,每个处理接种10袋,比较不同颗粒度对栽培种平均满袋时间的影响。结果(图11)表明,随着颗粒度降低,平均满袋时间逐渐增加,其中颗粒度为7∶3比10∶0的平均满袋时间稍大,但两者差异不显著(P>0.05),由于颗粒度为7∶3菌包菌丝粗壮、浓白,因此选择栽培种培养基木屑组分颗粒度为7∶3。
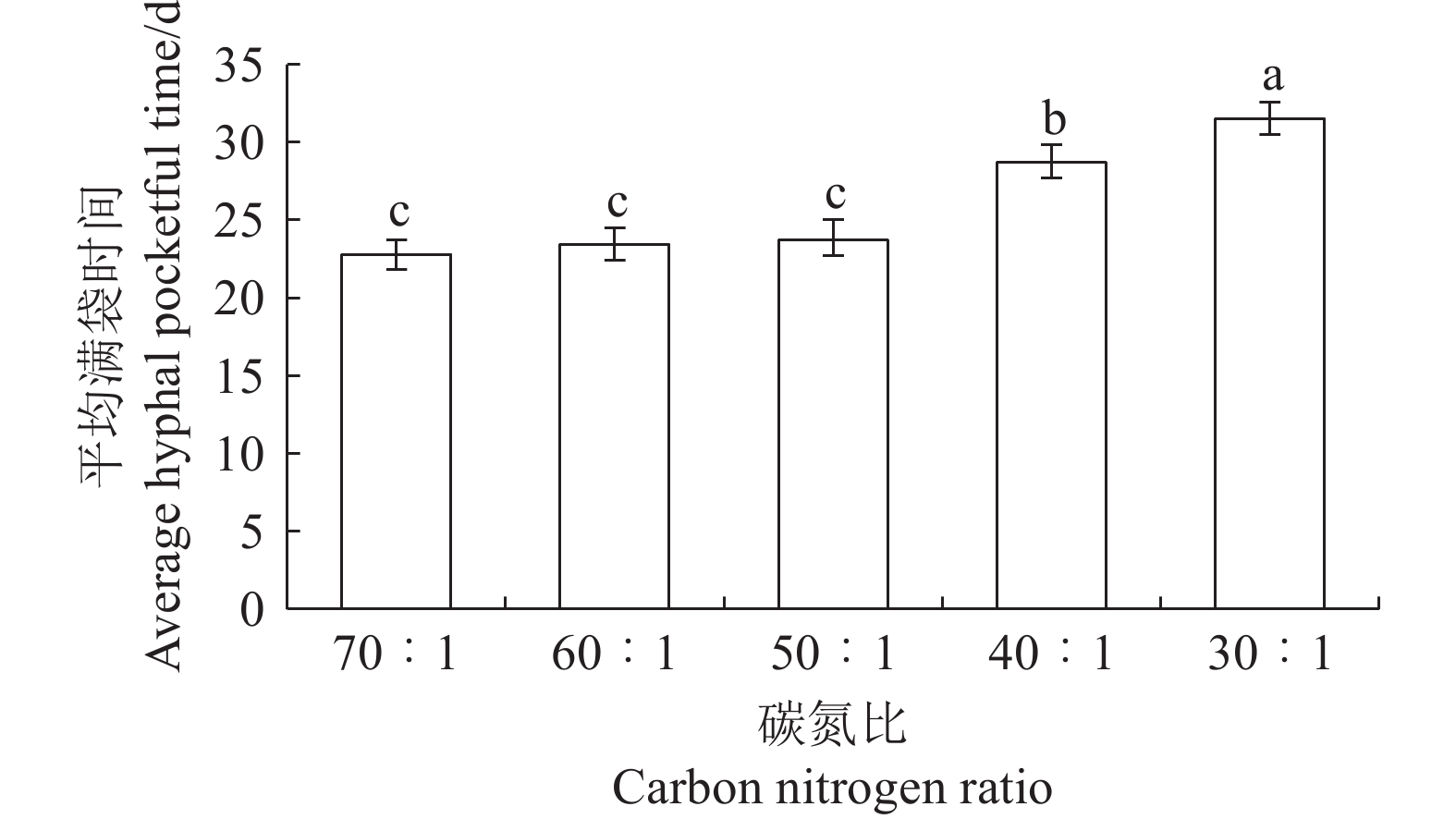
2.4.4 栽培种培养基碳氮比对菌包满袋时间的影响
不同碳氮比按表4配方,配制碳氮比为70∶1、60∶1、50∶1、40∶1、30∶1的菌包培养基,比较不同碳氮比对栽培种平均满袋时间的影响,由图12可知,随着碳氮比降低,平均满袋时间逐渐增加,其中碳氮比为70∶1、60∶1、50∶1的平均满袋时间分别为22.8 d、23.4 d和23.5 d,三者差异不显著(P>0.05),但碳氮比为50∶1,菌包菌丝粗壮、浓白,因此选择栽培种培养基碳氮比为50∶1。
3. 讨论
在培养基组成中,碳源是影响菌丝体生长最主要的成分之一。碳源主要为大球盖菇菌丝体供应生命活动所需要的能源,组成菌丝体细胞成分的碳架,构成代谢产物[19]。大球盖菇可以利用的碳源范围广泛,碳源筛选试验表明,天然培养基组分玉米淀粉、玉米粉、小麦粉、小米粉优于葡萄糖和蔗糖,这与刘金力等[20]研究结果类似。小麦粉来源广泛、价格低廉,对大球盖菇菌丝体液体培养最有利,因此,选择小麦粉作为大球盖菌液体培养基碳源。前人研究结果表明菌丝体前期生长过程中需要单糖作为速效碳源使菌种快速定殖[20−21] ,故在碳源上组分还选择了葡萄糖。氮源用于食用菌细胞内蛋白质与核酸等物质的合成,根据前人的研究基础,氮源为有机氮源处理的大球盖菇菌丝体干重显著高于无机氮源的处理[20],本研究只选取有机氮源酵母粉、蛋白胨、牛肉膏、麦芽汁、黄豆粉和麸皮进行筛选试验,酵母粉对液体培养大球盖菇菌丝体生物量影响最大,因此,氮源选择酵母粉。pH是发酵培养过程的重要参数之一,影响培养液胞外酶活性和菌丝体的生长和产物的合成[22]。单因素试验表明,大球盖菇菌丝体对培养基的起始pH适应范围较广,起始pH为6时对菌丝体生物量影响最大,这与李正鹏等[11]对大球盖菇液体菌种培养条件的研究得到最适起始pH为6.5的研究结果不同,这可能是由于不同大球盖菇供试菌株所造成的。考虑到各因素的互作影响,因此,有必要通过正交试验优化最佳起始pH。对葡萄糖、小麦粉、酵母粉和起始pH进行L9(34)正交试验,结果表明,当培养基含葡萄糖20 g·L−1、小麦粉30 g·L−1、酵母粉0.75 g·L−1、磷酸二氢钾1.00 g·L−1、硫酸镁0.50 g·L−1,起始pH 5时为最优配方,优化后培养7 d时大球盖菇菌丝体生物量为1.66 g·hmL−1,比基础培养基培养的菌丝体1.05 g·hmL−1增长了58.6%,比刘克芳等[14]优化培养得到大球盖菇最大菌丝体生物量1.51 g·hmL−1增加了近10%,说明本研究优化的液体培养基可以显著提高菌丝体生物量。
孙萌[23]、戴建成[24]对不同培养料栽培大球盖菇不同生长期间的碳氮代谢相关酶活性的变化规律进行研究。而本研究选择液体发酵培养过程中菌丝体生物量、还原糖和氨基氮含量、羧甲基纤维素酶、淀粉酶、酸性蛋白酶和漆酶活等4种胞外酶生理生化指标反映菌丝体生命活动状态。胞外酶活性变化规律与菌丝体生长趋势基本符合,大球盖菇液体菌种活性与上述指标具有一定的相关性,但与双孢蘑菇液体菌种发酵液中的4种胞外酶变化规律有所不同[18]。当液体培养8 d时,虽然此时菌丝体生物量最大,但还需参考还原糖、氨基氮含量和胞外酶酶活指标,确定液体菌种最佳活力的培养时间。随着培养时间增加,还原糖和氨基氮含量呈不断下降趋势,结合培养液的羧甲基纤维素酶、淀粉酶和酸性蛋白酶活性由峰值逐步下降,在第8天羧甲基纤维素酶、酸性蛋白酶酶活增强,淀粉酶酶活降至最低,此时菌丝体生物量最大,表现为培养基中碳、氮源物质代谢充分,考虑到氨基氮含量在培养时间第6天维持动态平衡,因此,确认液体培养第7天能获得活力最优大球盖菇液体菌种。
传统的大球盖菇栽培种制种周期长,原种扩繁栽培种一般需要2~3个月甚至更长时间才能完成菌包满袋,往往造成较高的污染率,尤其在高温高湿的南方,有时污染率竟高达50 %以上,导致制种成本过高,从而影响推广[14, 25]。液体制种具有生长快速、菌龄整齐、接种方便等诸多优点,可以弥补固体制种的缺点。利用液体菌种的流动性,接入中间打孔的菌包,能进一步缩短走菌满袋时间,使菌包上下菌丝培养时间短且整齐一致,从而保证了大球盖菇栽培种质量。菌包培养料的颗粒度影响菌丝走菌速度,适宜的颗粒度能改善和提高培养基透气性,促进菌丝生长[26],以满袋时间为指标,培养料颗粒度粗细木屑比为7∶3的菌包菌丝粗壮、浓白。适当的培养料碳氮比,为菌丝的生长提供营养物质,在一定范围内,培养料配方碳氮比越小,即氮含量越高,菌丝平均生长速度越慢[27],这与本研究试验结果类似。
4. 结论
本研究通过单因素、正交试验优化得到最优配方为葡萄糖20 g·L−1、小麦粉30 g·L−1、酵母粉0.75 g·L−1、磷酸二氢钾1.00 g·L−1、硫酸镁0.50 g·L−1,起始pH 5。利用最优配方发酵培养大球盖菇液体菌菌种,掌握了液体培养过程中菌丝体生物量、还原糖和氨基氮含量、羧甲基纤维素酶、淀粉酶、酸性蛋白酶和漆酶酶活4种胞外酶生理生化指标变化规律,确认大球盖菇液体培养7 d能获得活力最优液体菌种用于扩繁栽培种。确立液体菌种扩繁栽培种生产工艺参数:接种量为15 mL,菌包培养基配方颗粒度按质量比粗木屑与细木屑比为7∶3,碳氮比为50∶1。利用大球盖菇液体菌种扩繁栽培种,平均满袋时间为23.7 d,缩短生长周期2.7 d,提高菌种质量,优化了大球盖菇液体菌种培养基配方,建立了配套的制种工艺,为大球盖菇栽培种工厂化生产技术奠定了基础。
-
表 1 正交试验因素和水平
Table 1 Orthogonal factors and levels on factors affecting mycelial biomass
水平
Levels因素 Factors/(g·L−1) A葡萄糖
A GlucoseB小麦粉
B Wheat flourC酵母粉
C Yeast powderD 起始pH
D Initial pH1 10 20 0.75 5 2 15 25 1.00 6 3 20 30 1.25 7 表 2 不同碳氮比的菌包培养基配方
Table 2 Culture media with varied carbon-nitrogen ratio in bag
编号
No.杂木屑
Wood
chips/%麸皮
Wheat
bran/%花生粕
Peanut
meal/%碳酸钙
calcium
carbonate/%碳氮比
Carbon
nitrogen
ratio1 83 14 2 1 70∶1 2 81 14 4 1 60∶1 3 80 14 5 1 50∶1 4 77 14 8 1 40∶1 5 73 14 12 1 30∶1 表 3 培养基优化的正交试验结果
Table 3 Orthogonal experiment results and range analysis for medium optimization
试验号
No.因素 Factors 菌丝体
生物量
Mycelial
biomass/
( g·hmL-1)A葡萄糖
A GlucoseB小麦粉
B Wheat
flourC酵母粉
C Yeast
powderD起始pH
D Initial
pH1 1 1 1 1 1.23 2 1 2 3 3 1.12 3 1 3 2 2 1.29 4 2 1 3 2 1.18 5 2 2 2 1 1.34 6 2 3 1 3 1.44 7 3 1 2 3 1.28 8 3 2 1 2 1.56 9 3 3 3 1 1.59 K1j 3.64 3.68 4.23 4.17 K2j 3.96 4.02 3.91 4.03 K3j 4.43 4.33 3.89 3.84 k1j 1.21 1.23 1.41 1.39 k 2j 1.32 1.34 1.30 1.34 k 3j 1.48 1.44 1.30 1.28 极差 R 0.26 0.21 0.12 0.11 优化水平
Optimal level3 3 1 1 表 4 正交试验方差分析
Table 4 Variance analysis on orthogonal experiment results
方差来源
Source平方和
Sum of
squares自由度
Degree of
freedom均方
Mean squareF值
F value显著性
SignificanceA葡萄糖 0.41 2 0.20 80.13 ** B小麦粉 0.28 2 0.14 54.28 ** C酵母粉 0.06 2 0.03 11.01 ** D起始 pH 0.09 2 0.05 18.39 ** 误差 Error 0.05 18 0.01 总和 Sum 49.92 27 **表示差异显著(P<0.01)。
**means significant differences at P<0.01. -
[1] 贺新生. 现代菌物分类系统[M]. 北京: 科学出版社, 2015: 238. [2] 黄年来. 大球盖菇的分类地位和特征特性 [J]. 食用菌, 1995, 17(6):11. HUANG N L. Taxonomic status and characteristics of Pleurotus ostreatus [J]. Edible Fungi, 1995, 17(6): 11. (in Chinese)
[3] 姚春馨, 王小艳, 王小蓉, 等. 大球盖菇栽培研究现状与绿色发展前景 [J]. 中国食用菌, 2023, 42(6):90−97. YAO C X, WANG X Y, WANG X R, et al. Research progress on cultivation and green development of Stropharia rugosoannulata [J]. Edible Fungi of China, 2023, 42(6): 90−97. (in Chinese)
[4] 边银丙. 大球盖菇栽培技术及其创新发展方向 [J]. 食药用菌, 2023, 31(06):370−377. BIAN Y B. Cultivation technology and its innovative development direction of Stropharia rugosoannulata [J]. Edible and Medicinal Mushrooms, 2023, 31(06): 370−377. (in Chinese)
[5] 杨晓波, 蔡为明, 金群力, 等. 大球盖菇大棚设施栽培试验 [J]. 食药用菌, 2020, 28(5):328−331. YANG X B, CAI W M, JIN Q L, et al. Cultivation experiment of Stropharia rugoso-annulata in greenhouse [J]. Edible and Medicinal Mushrooms, 2020, 28(5): 328−331. (in Chinese)
[6] 霍捷, 王卫平, 滑帆, 等. 大球盖菇栽培模式研究进展与发展方向探讨 [J]. 中国食用菌, 2020, 39(2):35−38. HUO J, WANG W P, HUA F, et al. Research progress and development direction of the cultivation model of Stropharia rugosoannulata [J]. Edible Fungi of China, 2020, 39(2): 35−38. (in Chinese)
[7] LIU Y T, SUN J, LUO Z Y, et al. Chemical composition of five wild edible mushrooms collected from Southwest China and their antihyperglycemic and antioxidant activity [J]. Food and Chemical Toxicology: an International Journal Published for the British Industrial Biological Research Association, 2012, 50(5): 1238−1244. DOI: 10.1016/j.fct.2012.01.023
[8] LI X P, CUI W J, CUI Y F, et al. Stropharia rugoso-annulata acetylated polysaccharides alleviate NAFLD via Nrf2/JNK1/AMPK signaling pathways [J]. International Journal of Biological Macromolecules, 2022, 215: 560−570. DOI: 10.1016/j.ijbiomac.2022.06.156
[9] JIN M Z, ZHANG W Q, ZHANG X M, et al. Characterization, chemical modification and bioactivities of a polysaccharide from Stropharia rugosoannulata [J]. Process Biochemistry, 2023, 128: 30−39. DOI: 10.1016/j.procbio.2023.02.008
[10] WU J, SUZUKI T, CHOI J H, et al. An unusual sterol from the mushroom Stropharia rugosoannulata [J]. Tetrahedron Letters, 2013, 54(36): 4900−4902. DOI: 10.1016/j.tetlet.2013.06.142
[11] 李正鹏, 吴萍, 陆晓民. 大球盖菇液体菌种培养条件的研究 [J]. 中国林副特产, 2006, (4):12−14. DOI: 10.3969/j.issn.1001-6902.2006.04.005 LI Z P, WU P, LU X M. Study on the training condition of liquid culture Stropharia rugoso-annulata [J]. Forest by-Product and Speciality in China, 2006(4): 12−14. (in Chinese) DOI: 10.3969/j.issn.1001-6902.2006.04.005
[12] 曾健勇, 张国财, 赵博, 等. 磁化水培养对大球盖菇菌丝生长特性的影响 [J]. 食品工业科技, 2017, 38(20):110−114. ZENG J Y, ZHANG G C, ZHAO B, et al. Effect of magnetized water liquid cultivation on growth characteristics of Stropharia rugoso-annulata mycelium [J]. Science and Technology of Food Industry, 2017, 38(20): 110−114. (in Chinese)
[13] 付婧璇, 耿丹萌, 高华, 等. 香蒲资源化开发中大球盖菇液体菌种的制备与应用 [J]. 河北大学学报(自然科学版), 2019, 39(1):76−79. FU J X, GENG D M, GAO H, et al. Preparation and application of liquid strains of Stropharia rugoso-annulata in the development of Typha resources [J]. Journal of Hebei University (Natural Science Edition), 2019, 39(1): 76−79. (in Chinese)
[14] 刘克芳, 于国荣, 王华丽, 等. 大球盖菇液体菌种培养基的优化 [J]. 中国食用菌, 2021, 40(8):24−28. LIU K F, YU G R, WANG H L, et al. Optimization of liquid spawn formula of Stropharia rugosoannulata [J]. Edible Fungi of China, 2021, 40(8): 24−28. (in Chinese)
[15] 杜瑞垚. 大球盖菇菌丝液体培养及液体菌种固化技术研究[D]. 武汉: 华中农业大学, 2023. DU R Y. Study on the Technology of Mycelia Liquid Culture and Liquid Spawn Solidification in Stropharia Rugosoannulata[D]. Wuhan: Huazhong Agricultural University, 2023. (in Chinese)
[16] 曾志恒, 曾辉, 程翊, 等. 双孢蘑菇发酵液还原糖和总糖的含量测定 [J]. 中国食用菌, 2018, 37(6):40−43,49. ZENG Z H, ZENG H, CHENG Y, et al. Determination of reducing sugar and total sugar content in fermentation liquid of Agaricus bisporus [J]. Edible Fungi of China, 2018, 37(6): 40−43,49. (in Chinese)
[17] 曾志恒, 曾辉, 程翊, 等. 双孢蘑菇发酵液氨基氮含量测定方法的研究 [J]. 食用菌, 2019, 41(5):77−80. DOI: 10.3969/j.issn.1000-8357.2019.05.026 ZENG Z H, ZENG H, CHENG Y, et al. Study on determination method of amino nitrogen content in fermentation broth of Agaricus bisporus [J]. Edible Fungi, 2019, 41(5): 77−80. (in Chinese) DOI: 10.3969/j.issn.1000-8357.2019.05.026
[18] 戴建清. 双孢蘑菇W192液体菌种摇瓶培养过程中的生理生化分析 [J]. 福建农业学报, 2021, 36(2):182−187. DAI J Q. Physiological and biochemical properties of Agaricus bisporus in shaking flask culture [J]. Fujian Journal of Agricultural Sciences, 2021, 36(2): 182−187. (in Chinese)
[19] 田华. 现代菌物分类系统[M]. 北京: 化学工业出版社, 2019. [20] 刘金力, 唐琳, 陈思, 等. 大球盖菇液体菌种培养基碳氮源及培养条件的优化[J]. 黑龙江农业科学, 2019(4): 94-99. LIU J L, TANG L, CHEN S, et al. Optimization of carbon and nitrogen sources and culture conditions of liquid culture medium of Stropharia rugosoannulata[J]. Heilongjiang Agricultural Sciences, 2019(4): 94-99. (in Chinese)
[21] 周韬. 香菇液体菌种培养基优化及其菌种质量评价体系的建立[D]. 武汉: 华中农业大学, 2017. ZHOU T. Research on medium optimization and quality evaluation system of Lentinula edodes liquid spawn[D]. Wuhan: Huazhong Agricultural University, 2017. (in Chinese)
[22] 曾志恒, 程翊, 曾辉, 等. 双孢蘑菇W192菌株液体发酵培养的研究 [J]. 福建农业学报, 2013, 28(8):763−769. DOI: 10.3969/j.issn.1008-0384.2013.08.008 ZENG Z H, CHENG Y, ZENG H, et al. Study on fermentation of Agaricus bisporus strain W192 [J]. Fujian Journal of Agricultural Sciences, 2013, 28(8): 763−769. (in Chinese) DOI: 10.3969/j.issn.1008-0384.2013.08.008
[23] 孙萌. 大球盖菇菌丝培养及胞外酶活性变化规律研究[D]. 延吉: 延边大学, 2013. SUN M. Mycelium culture and the variation regularity of extracellular enzyme activity of stropharia rugosoannulata Farlow[D]. Yanji: Yanbian University, 2013. (in Chinese)
[24] 戴建成. 大球盖菇培养基质的优化及工厂化生产的初步探究[D]. 南京: 南京农业大学, 2021. DAI J C. Optimization of Medium Quality and Preliminary Study on Industrial Production of Stropharia Rugosoannulata[D]. Nanjing: Nanjing Agricultural University, 2021. (in Chinese)
[25] 王升厚, 李玉双. 大球盖菇液体母种制备培养基碳氮源的优化 [J]. 北方园艺, 2008, (5):219−221. WANG S H, LI Y S. The optimization of carbonaceous compounds and nitrogenous substances for liquid culture media of Stropharia rugoso annulata [J]. Northern Horticulture, 2008(5): 219−221. (in Chinese)
[26] 黄桂英, 杨林, 左天兴. 提高白僵菌培养基透气性的试验[J]. 云南林业科技, 1996, 25(2): 71-73. HUANG G Y, YANG L, ZUO T X. A Test on Raising BreathbiIity to Beauveria bassiana medium[J]. Yunnan Forestry Science and Technology, 1996(2): 71-73. (in Chinese)
[27] 曾志恒, 曾辉, 蔡志欣, 等. 双孢蘑菇新型颗粒原种配方的优化 [J]. 生物技术通报, 2021, 37(11):134−141. ZENG Z H, ZENG H, CAI Z X, et al. Formula optimization of the novel particle pre-culture spawn of Agaricus bisporus [J]. Biotechnology Bulletin, 2021, 37(11): 134−141. (in Chinese)




 下载:
下载: