Functional Bacillus Species in Camellia Seed Shell Compost
-
摘要:目的 从自然状态下的油茶壳堆肥产品中筛选功能芽孢杆菌,为油茶壳堆肥高效生产、饲料发酵等应用提供菌剂。方法 利用高通量测序技术测定广西某油茶壳堆肥中微生物群落分布,筛选适宜堆肥微生物生长的培养基以获得多样性较丰富的堆肥芽孢杆菌菌群,经平板稀释涂布法分离纯化菌株,使用水解圈法和酶活测定方法进行水解酶功能分析,利用菌株形态特征观察、16S rDNA分子鉴定法明确菌株的种属,并运用分子生物学软件 MEGAX构建系统发育树。使用重铬酸钾法测定腐殖酸含量。结果 芽孢杆菌科(Bacillaceae)是优势菌科,占比达55.58%;分离到15株芽孢杆菌,同时具有淀粉酶、纤维素酶、蛋白酶3种水解酶活性的菌株有6株;同时具有淀粉酶和纤维素酶活性的有1株;仅具有蛋白酶或纤维素酶一种酶活性的有2株。其中菌株Bacillus sp. YX11的蛋白酶活力达到27.07±3.28 U·mL−1,淀粉酶活力达123.97±3.19 U·mL−1,纤维素酶活力达15.75±0.23 U·mL−1。含有这15株菌的复合菌制剂有利于腐殖酸的生成,提高了堆肥品质。结论 鉴定出的Bacillus cereus YX02和 Bacillus flexus FYF01等菌株具有进一步研究开发的价值,可用于开发油茶壳堆肥微生物菌制剂。Abstract:Objective Bacillus spp that contribute to the fermentation of Camellia oleifera seed shells were isolated for effective composting of the waste material.Method The microbial community in natural camellia seed shell compost found in Guangxi was studied using the high-throughput sequencing technology. Suitable culture medium to foster the growth of richly diverse Bacillus spp from the compost was selected. Flora isolation by dilution with a streaking plate method followed. The hydrolase activities of the isolates were determined by using the hydrolysis circle method and enzyme activity analysis, the species identified by a 16S rDNA analysis, and the phylogeny constructed by MEGAX. The content of humic acid in the compost was measured by a potassium dichromate method.Result Bacillaceae was the dominant family in the compost. It accounted for 55.58% of all isolated flora. Among the 15 Bacillus isolates, 6 exhibited activities of amylase, cellulase, and protease, one of amylase and cellulase, and 2 of protease or protease. Strain YX11 showed a protease activity of 27.07±3.28 U·mL−1, an amylase activity of 123.97±3.19 U·mL−1, and a cellulase activity of 15.75±0.23 U·mL−1. In the presence of numerous Bacillus spp that secreted varieties of hydrolases, formation of humic acid in the compost was enhanced.Conclusion Some of the isolated strains, such as B. cereus YX02 and B. flexus FYF01, might warrant further investigation to develop microbial inoculants for efficient composting camellia seed shells.
-
Keywords:
- camellia seed shell compost /
- bacillus /
- functional /
- screening /
- application
-
0. 引言
【研究意义】油茶是我国特有的木本食用油料树种。油茶壳是油茶果实加工茶油的副产品,随着油茶产业的发展,每年都有大量油茶壳产生。油茶壳占整个油茶果实质量的60%以上,其主要成分是纤维素、半纤维素、木质素[1],已经在有机肥料、钾盐、活性炭的生产中得到利用,具有广阔的发展空间与市场空间[2]。以油茶壳为主要原料的堆肥,可以把储量丰富、价格低廉的油茶壳资源充分利用。油茶壳堆肥产品的生产和使用,不仅减少对大气、土壤、水质的污染,也减少化肥投入,增加农产品产量,提高了农民收入。【前人研究进展】微生物在堆肥生产中有重要的作用,添加微生物加速农业副产品堆肥的研究开发已经比较普遍。如Shrestha等[3]进行微生物强化牛瘤胃内容物堆肥的研究。Song等[4]开发一种协同降解有机酸的微生物联合体(MCDOA),加速蛋白质类化合物的降解和复杂的类腐殖质物质的形成,并改善醋酸、丙酸降解菌和木质素降解菌的原生菌群结构和多样性,有效缩短餐厨垃圾堆肥周期。Yu等[5]将嗜热芽孢杆菌接种于污泥堆肥中,提高了堆肥的质量和效率。由于芽孢杆菌在农业副产品堆肥生产中有重要作用,其现已成为应用最多的微生物菌制剂[6, 7],如:可以从堆肥中分离出降解纤维素的嗜热芽孢杆菌[8];将松树皮制成堆肥,接种芽孢杆菌属等有益的微生物,可以增强对树木根病菌的抑制作用,减少在苗圃使用杀菌剂[9];以萝卜细菌性叶斑病为例,探讨堆肥对植物叶面病害的抑制作用,并对堆肥中可能起抑制作用的根际细菌进行了鉴定,发现抑制病害最显著的是芽孢杆菌属[10];利用芽孢杆菌研制固体菌制剂可促进园林废弃物堆肥过程中木质素、纤维素的降解和腐殖质的合成[11];从完全腐熟的餐厨垃圾有机肥中筛选出芽孢杆菌复合菌剂,能够明显缩短堆肥周期和提高餐厨垃圾降解率[12]。这些研究表明芽孢杆菌具有降解纤维素、抑制致病菌、提高餐厨垃圾降解率和缩短堆肥周期等功能。【本研究切入点】目前,油茶壳堆肥存在生产效率低和品质不高等问题,对油茶壳堆肥的研究报道[13-15]还比较少,且对油茶壳堆肥中功能性芽孢杆菌的研究有待进一步深入。【拟解决的关键问题】利用高通量测序技术[16]探究广西某农场自然状态下的油茶壳堆肥产品中的微生物多样性组成,再通过选择合适的培养基,获得实验室环境下物种多样性相对比较丰富的堆肥芽孢杆菌菌群。从中筛选具有水解酶功能特性和其他功能特点的芽孢杆菌,并应用16S rDNA鉴定其系统发育关系和分类学地位,最终完成应用效果试验。为今后开发油茶壳堆肥微生物菌制剂、提升油茶壳堆肥的生产效率和品质,以及饲料发酵等应用方面提供了菌种资源。
1. 材料与方法
1.1 试验材料
1.1.1 样品来源
堆肥样品来自广西某农场自然状态下的油茶壳堆肥,呈褐色固体颗粒或团状,pH7.96,含水率37.35%。
1.1.2 试剂
EazyTaq酶,北京聚合美生物科技有限公司生产,λDNA/Hind Ⅲ DNA Marker、DL2000 DNA Marker、dNTPMix,TaKaRa试剂 (大连)公司生产;柱式PCR产物纯化试剂盒,上海生工生物技术有限公司生产;革兰氏染色液,购自广东环凯微生物科技有限公司;酵母粉和蛋白胨,均购自Oxoid (英国)公司;MiSeq Reagent Kit v3测序试剂盒,购自美国Illumina公司;biowest agArose琼脂糖,购自西班牙biowest公司;其他试剂均为国产分析纯。
1.1.3 培养基
采用的4 种常规培养基:(1)LB培养基[17]。(2)淀粉培养基:蛋白胨10 g·L−1,NaCl 5 g·L−1,牛肉膏5 g·L−1,可溶性淀粉10 g·L−1,琼脂15 g·L−1,pH 7.0~7.2。(3)脱脂乳培养基:用于蛋白酶活性的鉴定试验,分别配制A液和B液。A液:牛肉膏0.5 g,蛋白胨1.0 g,NaCl 0.5 g,琼脂2 g,pH 7.0~7.2,共50 mL;B液:脱脂奶粉3 g,pH 7.0~7.2,50 mL。A、B单独灭菌,使用时混合。(4)刚果红纤维素培养基:K2HPO4 0.5 g·L−1,MgSO4 0.25 g·L−1,刚果红0.2 g·L−1,CMC-Na 2 g·L−1,NaCl 1.0 g·L−1,琼脂20 g·L−1,pH 7.0~7.2。通过参考适宜芽孢杆菌生长的培养基[18-20],设定堆肥微生物生长的6组筛选培养基:M1:红糖6 g·L−1,酵母粉 1 g·L−1,豆粕1 g·L−1,硫酸铵 4 g·L−1,MgSO4 1 g·L−1,MnSO4 0.03 g·L−1,蛋白胨4 g·L−1,pH 7.0~7.2;M2:葡萄糖6 g·L−1,酵母粉 1 g·L−1,豆粕1 g·L−1,硫酸铵 4 g·L−1,MgSO4 1 g·L−1,MnSO4 0.03 g·L−1,蛋白胨4 g·L−1,pH 7.0~7.2;M3:红糖5 g·L−1,酵母粉 3 g·L−1,NaCl 2 g·L−1,乙酸钠5 g·L−1,L-半胱氨酸盐0.5 g·L−1,可溶性淀粉1 g·L−1,蛋白胨5 g·L−1,pH 7.0~7.2;M4:葡萄糖20 g·L−1,酵母粉 4 g·L−1,乙酸钠5 g·L−1,硫酸铵 2 g·L−1,MgSO4 0.5 g·L−1,MnSO4 0.2 g·L−1,蛋白胨12 g·L−1,柠檬酸氢二胺2 g·L−1,吐温-80 1 g·L−1,CaCO3 2 g·L−1,K2HPO4 0.5 g·L−1,pH 7.0~7.2;M5:红糖5 g·L−1,FeSO4 0.2 g·L−1,KCl 0.5 g·L−1,硫酸铵 3 g·L−1,MgSO4 0.5 g·L−1,MnSO4 0.06 g·L−1,K2HPO4 4 g·L−1,pH 7.0~7.2;M6:红糖10 g·L−1,酵母粉 2 g·L−1,豆粕2 g·L−1,尿素10 g·L−1,pH 7.0~7.2。
1.2 试验设计
1.2.1 油茶壳堆肥微生物多样性分析
采集适量油茶壳堆肥样品,送至Shanghai Majorbio Bio-pharm Technology Co., Ltd完成16S rDNA高通量测序,细菌的通用引物序列为:806R(5′-GGACTACHVGGGTWTCTAAT-3′)与338F(5′-ACTCCT-ACGGGAGGCAGCAG-3′);测序区域V3~V4区,测序平台为IIIumina MiSeq。使用UPARSE软件(version 7.1, http://drive5.com/uparse/),以 97%的相似度对序列进行OTU聚类,以UCHIME 软件剔除嵌合体。通过RDP classifier对测定的序列完成物种分类注释,然后比对Silva 数据库(SSU128),设置70%的比对阈值最终确定堆肥中微生物的种群结构。
1.2.2 堆肥微生物培养基的筛选
比较M1~M6共6组培养基对堆肥微生物生长的影响,每组培养基设3个试验组,代表3种培养条件:胶塞封口厌氧静置培养,按M1~M6编号为1-Y,2-Y,3-Y,4-Y,5-Y,6-Y;纱布封口好氧静置培养,按M1~M6编号为1-HJ,2-HJ,3-HJ,4-HJ,5-HJ,6-HJ;纱布封口好氧摇床培养(100 r·min−1),按M1~M6编号为1-HY,2-HY,3-HY,4-HY,5-HY,6-HY。初始pH均为7.0~7.2。将新鲜堆肥样品的无菌生理盐水洗涤液以1%的量接种于各培养基中,培养温度37 ℃。于培养后的第1、2、3、5、7、15、22、30 d,使用紫外分光光度计测定OD600值。培养后的第3、7、15、30 d,使用平板计数法统计原核微生物菌数,并使用光学显微镜观察培养液的微生物形态。
1.2.3 芽孢杆菌平板初筛
堆肥样品经最佳培养基培养后,使用十倍稀释法[21]涂布平板,分离单菌落。
1.2.4 菌株的形态学鉴定
在平板上观察菌株的菌落形态、菌落颜色和质地等,并挑取菌落进行革兰氏染色[22]。
1.2.5 菌株的16S rDNA鉴定
分别提取菌株基因组DNA[23],通过PCR扩增其16S rDNA[24],送至北京六合华大基因科技有限公司进行测序。结果进行核酸BLAST[25]分析比对,利用MEGAX构建系统发育树[26]。
1.2.6 菌株的水解酶功能的初筛和测定
(1)水解酶活性的平板初筛
蛋白酶活性的初筛:将经纯化菌株点种在脱脂乳培养基上,观察培养基的周围是否产生透明的水解圈[27]。淀粉酶活性的初筛:使用Elamary等[28]的方法对菌株淀粉酶水解活性进行了筛选,水解圈的出现作为菌株产淀粉酶的依据。纤维素酶活性的初筛:使用刚果红纤维素培养基法,进行纤维素酶活性鉴定[29]。
(2)菌株的基础发酵
将菌株接种到LB液体发酵培养基,于37 ℃培养24 h后测定水解酶活性。
(3)水解酶活力的测定
粗酶液的制备:将初筛菌株的发酵液于4 ℃、8000 r·min−1条件下离心10 min,除菌体后上清液即为粗酶液。蛋白酶活力检测采用福林酚法[30],蛋白酶活力单位定义为:在37 ℃、pH 7.8的条件下,每分钟催化酪蛋白水解生成1 μg酪氨酸的酶量。淀粉酶活力检测采用曹丹等[31]使用的方法,淀粉酶活力单位定义为在37 ℃、pH 6.0的条件下,每分钟催化可溶性淀粉水解生成1 μg还原糖的酶量。纤维素酶活力检测采用DNS法[32],酶活定义为在37 ℃、pH 5.5的条件下每分钟催化羧甲基纤维素钠产生1 μg葡萄糖的酶量。
1.2.7 菌株在油茶壳堆肥中的应用试验
将筛到的15株菌使用LB发酵培养基单独培养24 h,然后各取1 mL混合,制成微生物菌制剂。设置一个添加菌制剂的试验组,不添加菌制剂的对照组,每个组3个平行。使用250 mL三角瓶,各试剂按表1的配方添加,初始pH 7.2,纱布封口,于37 ℃下,摇床转速120 r·min−1培养。使用重铬酸钾法[33]测定培养15 d的腐殖酸含量。
表 1 菌制剂应用试验配方Table 1. Proposed formulations of microbial inoculants组别
Group油茶壳
Camellia shell/g菌液
microbial inoculants/mL糖蜜
Molasses/mL花生枯
Peanut cake/g尿素
Urea/g水
H2O/mL菌制剂 experiment group 15 15 6 1.2 1.2 100 对照组 control group 15 0 6 1.2 1.2 115 2. 结果与分析
2.1 微生物群落分析结果
利用高通量测序技术对油茶壳堆肥中微生物的多样性进行测定,结果显示(图1),芽孢杆菌科(Bacillaceae)是堆肥中的优势菌科,其占比达到55.58%,表明芽孢杆菌在油茶壳堆肥微生物中占主导地位。
2.2 堆肥微生物在不同培养基中的培养效果
采用M1~M6六组培养基在不同条件下培养堆肥微生物,培养液的OD600和菌数变化结果如图2所示,结合镜检菌株形态多样性分析,表明M2培养基最佳:在厌氧培养下菌数可达到(1.91±0.10) ×108 CFU·mL−1;好氧静置培养下,菌数最高可达到(33.3±0.59) ×108 CFU·mL−1;好氧摇床培养下,菌数最高可达到(1.19±0.13) ×108 CFU·mL−1。且镜检结果表明,M2培养基培养的微生物多样性更丰富。
2.3 菌株形态学鉴定结果
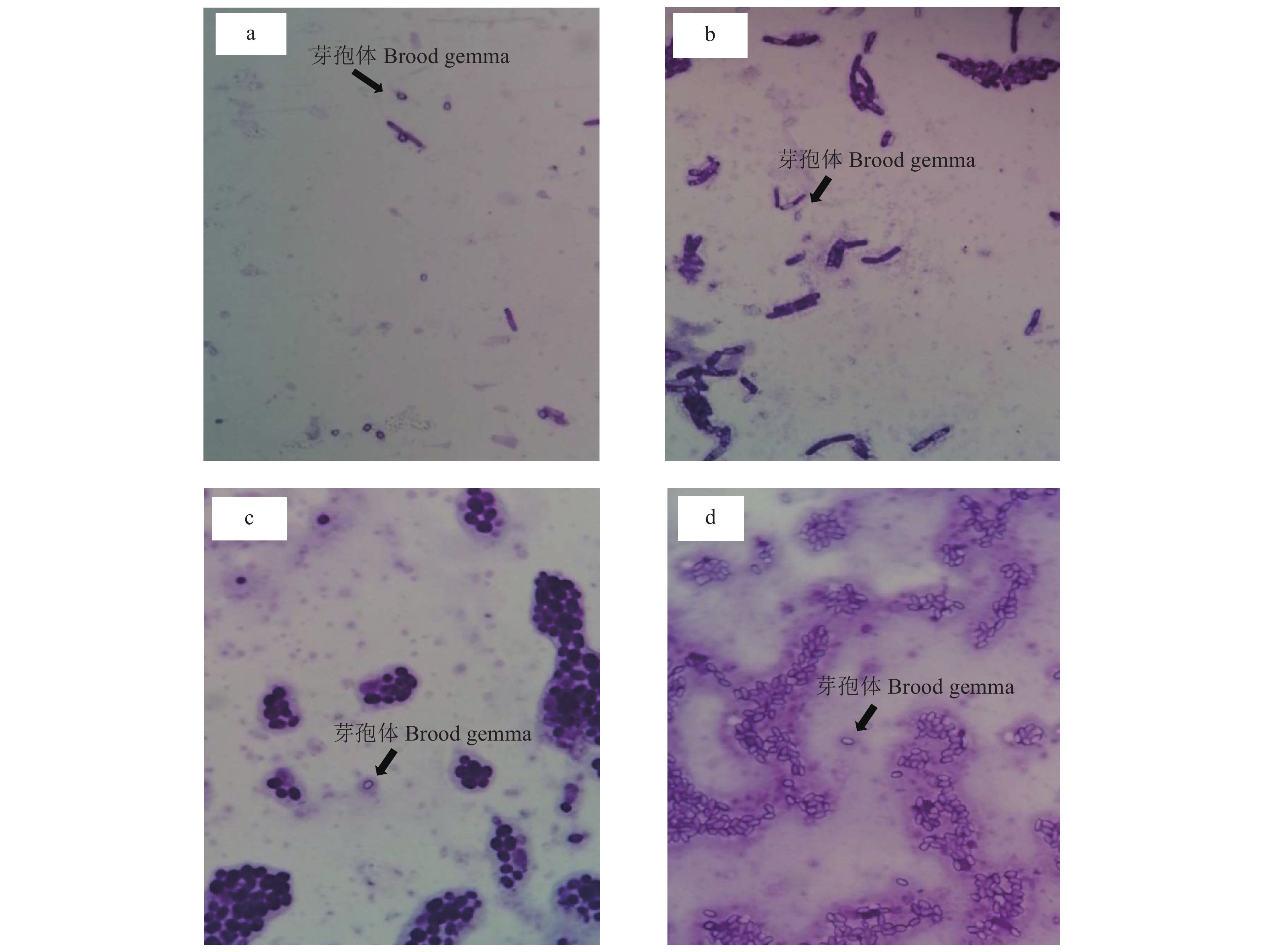
经平板划线纯化,分离到15株菌。它们在LB培养基上的菌落形态、菌落颜色和质地等如表2所示。经过染色后在光学显微镜下放大4 000倍观察到的菌体形态,如图3所示。
表 2 菌株形态特征Table 2. Morphological characteristics of isolated Bacillus spp菌株编号
Strains菌落质地
Colony texture菌落颜色
Colony color菌落形态
Colony morphologyYX01 干燥、皱褶 dry and wrinkled 半透明色 translucent color 不规则圆形,有毛边 irregular round with rough edges YX02 干燥、皱褶 dry and wrinkled 乳白色 milky white 较规则圆形,中间隆起 regular round, middle uplift YX03 光滑、湿润 smooth and moist 半透明色 translucent color 较规则圆形 regular round YX07 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX08 光滑、湿润 smooth and moist 半透明色 translucent color 圆形 round YX11 湿润、黏稠 wet and sticky 乳白色 milky white 圆形 round YX12 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX13 干燥、皱褶 dry and wrinkled 枯黄色 withered yellow 不规则圆形,有毛边 irregular round with rough edges YX15 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX16 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round FYF01 干燥、皱褶 dry and wrinkled 乳白色 milky white 不规则圆形,有毛边 irregular round with rough edges FYF04 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形 regular round FYF07 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形,中间隆起 regular round, middle uplift FYF08 干燥、皱褶 dry and wrinkled 半透明色 translucent color 不规则圆形,有毛边 irregular round with rough edges FYF10 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形 regular round 2.4 菌株的分子生物学鉴定结果
2.4.1 PCR扩增验证结果
将筛到的15株菌提取基因组DNA,通过PCR扩增其16S rDNA序列,使用琼脂糖凝胶电泳验证,如图4所示,结果显示扩增片段大小约为1.5 kb,与16S rDNA预期大小相符,可以用于测序分析。
2.4.2 菌株的16S rDNA序列分析
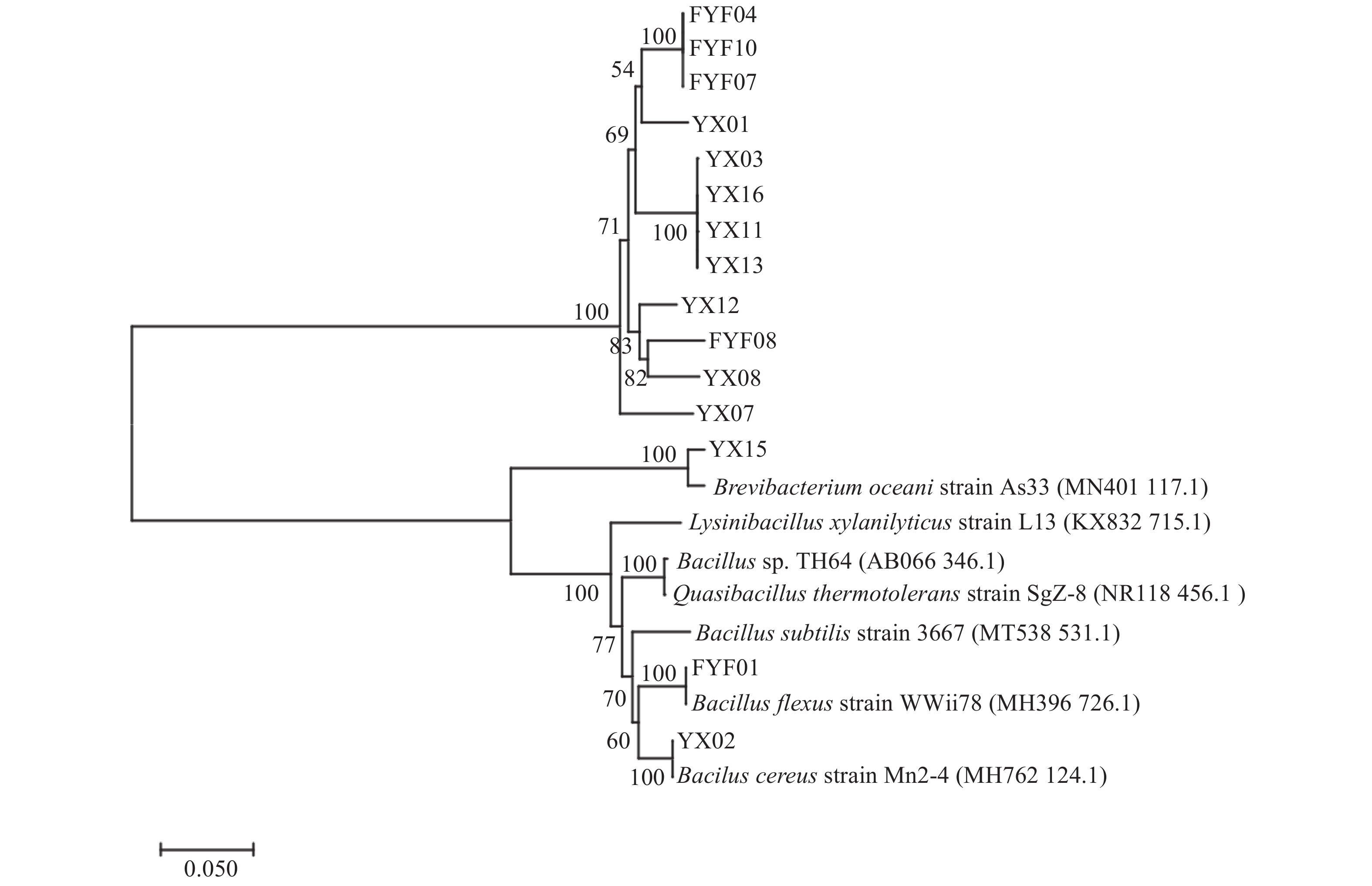
将分离到的菌株的16S rDNA测序结果在NCBI上比对后与相似性高的菌株共同构建系统发育树。根据相似性和系统发育树进化距离, 鉴定YX02为蜡状芽孢杆菌(Bacillus cereus[34]),YX15为海洋短杆菌(Brevibacterium oceani[35]),FYF01为弯曲芽孢杆菌(Bacillus flexus[36])。其他菌株由于在单独比对时有多个芽孢杆菌属内不同种的芽孢菌株与其相似性都很高且进化距离非常接近,单纯依赖16S rDNA序列比对尚不能准确鉴定到种,只能初步鉴定到芽孢杆菌属。从油茶壳堆肥中分离出的15菌株16S rDNA序列比对结果见表3。
表 3 菌株16S rDNA鉴定结果Table 3. Identifications by 16S rDNA序号 Serial number 编号 Number 菌种分类 Species classification 1 YX01 Bacillus sp. 2 YX02 Bacillus cereus 3 YX03 Bacillus sp. 4 YX07 Bacillus sp. 5 YX08 Bacillus sp. 6 YX11 Bacillus sp. 7 YX12 Bacillus sp. 8 YX13 Bacillus sp. 9 YX15 Brevibacterium oceani 10 YX16 Bacillus sp. 11 FYF01 Bacillus flexus 12 FYF04 Bacillus sp. 13 FYF07 Bacillus sp. 14 FYF08 Bacillus sp. 15 FYF10 Bacillus sp. 构建的系统发育树如图5所示,从发育树可以看到,有12株菌暂时鉴定为芽孢杆菌属(Bacillus spp.)的不同菌株。比如菌株YX03、YX16、YX11和YX13,以及菌株FYF07、FYF04和FYF10,在进化距离上非常接近,但根据菌落形态特征不同以及水解酶活性的差异,可推断是同一属内的不同菌株。在今后的研究中,将通过生理生化、DNA分子杂交技术鉴定等方式,进一步确定这些菌株的菌种类别。
2.5 酶学水解酶活性的初步鉴定结果
2.5.1 蛋白酶活性分析
将各菌株点种在脱脂乳培养基上,平板初筛蛋白酶的结果见表4所示。有7株菌产生蛋白酶水解圈,其中,透明圈和菌落直径比值(D/d)最大的是菌株FYF04,其次是菌株FYF07。D/d值一定程度上说明了菌株产蛋白酶能力的大小,但还需要测定发酵液中酶的活性,以进一步验证菌株的产酶能力。
表 4 不同培养基上菌落直径与透明圈直径比Table 4. Ratio of transparent ring diameter to colony diameter on different mediums菌株编号
Strains脱脂乳糖培养基
Skim milk medium淀粉培养基
Starch medium刚果红培养基
Congo red medium透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratio透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratio透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratioYX01 0.0 7.5 0.00 13.0 7.5 1.73 18.0 5.0 3.60 YX02 28.0 26.5 1.06 0.0 16.0 0.00 0.0 11.0 0.00 YX03 0.0 0.0 0.00 0.0 4.0 0.00 20.0 8.0 2.50 YX07 0.0 0.0 0.00 0.0 6.5 0.00 0.0 8.5 0.00 YX08 0.0 0.0 0.00 0.0 11.0 0.00 0.0 2.0 0.00 YX11 25.0 20.0 1.25 19.5 6.0 3.25 30.0 11.0 2.73 YX12 0.0 0.0 0.00 0.0 5.0 0.00 0.0 8.0 0.00 YX13 29.0 23.0 1.26 20.0 8.0 2.50 18.0 8.5 2.12 YX15 0.0 0.0 0.00 0.0 6.5 0.00 0.0 10.0 0.00 YX16 0.0 0.0 0.00 0.0 4.0 0.00 0.0 7.0 0.00 FYF01 14.0 12.0 1.17 16.0 6.0 2.67 32.0 6.5 4.92 FYF04 30.0 21.5 1.39 14.0 7.0 2.00 24.5 6.0 4.08 FYF07 26.0 19.0 1.37 20.0 11.5 1.74 24.0 9.0 2.67 FYF08 0.0 0.0 0.00 0.0 7.0 0.00 0.0 2.0 0.00 FYF10 25.5 19.5 1.31 18.0 12.5 1.44 25.0 9.0 2.78 2.5.2 淀粉酶活性分析
将各菌株点种在淀粉培养基上,平板初筛淀粉酶的结果如表4所示,共有7株菌产生淀粉酶水解圈,其中,透明圈和菌落直径比值(D/d)最大的是菌株YX11,其次是菌株FYF01。D/d值一定程度上说明了菌株产淀粉酶能力的大小,但还需要测定发酵液中酶的活性,以进一步验证菌株的产淀粉酶的能力。
2.5.3 纤维素酶活性分析
将各菌株点种在刚果红培养基上,平板初筛纤维素酶的结果如表4所示,共有8株菌产生纤维素酶水解圈,其中,透明圈和菌落直径比值(D/d)最大的是菌株FYF01,其次是菌株FYF04。D/d值一定程度上说明了菌株产纤维素酶能力的大小,但还需要测定发酵液中酶的活性,以进一步验证菌株的产纤维素酶的能力。
2.5.4 三种水解酶活力的测定
将各菌株进行液体发酵,测定粗酶液的水解酶的活力。最终初步测定初筛菌株的各酶活力的结果如图6所示。其中,蛋白酶活力最高菌株是Bacillus sp. YX11,27.07±3.28 U·mL−1;Bacillus sp. FYF10次之,为13.67±3.18 U·mL−1。淀粉酶活力最高菌株是Bacillus sp. YX13,达144.10±2.65 U·mL−1;Bacillus sp.YX11次之,为123.97±3.19 U·mL−1。纤维素酶活力最高菌株是Bacillus sp.YX11,达15.75±0.23 U·mL−1;Bacillus sp. YX03次之,为13.83±0.10 U·mL−1。
这些芽孢杆菌有9株菌初步显示具有一定的水解酶功能特性,其中同时具有淀粉酶、纤维素酶、蛋白酶三种水解酶活性的菌株有6株,同时具有淀粉酶和纤维素酶活性的有1株,仅具有蛋白酶或纤维素酶一种酶活性的有2株。表明这些菌株在油茶壳堆肥中具有促进纤维素向小分子葡萄糖转化、促进蛋白质向小分子肽和氨基酸转化以及促进淀粉向小分子麦芽糖和葡萄糖转化的功能性作用。
2.6 菌株在油茶壳堆肥中的初步应用
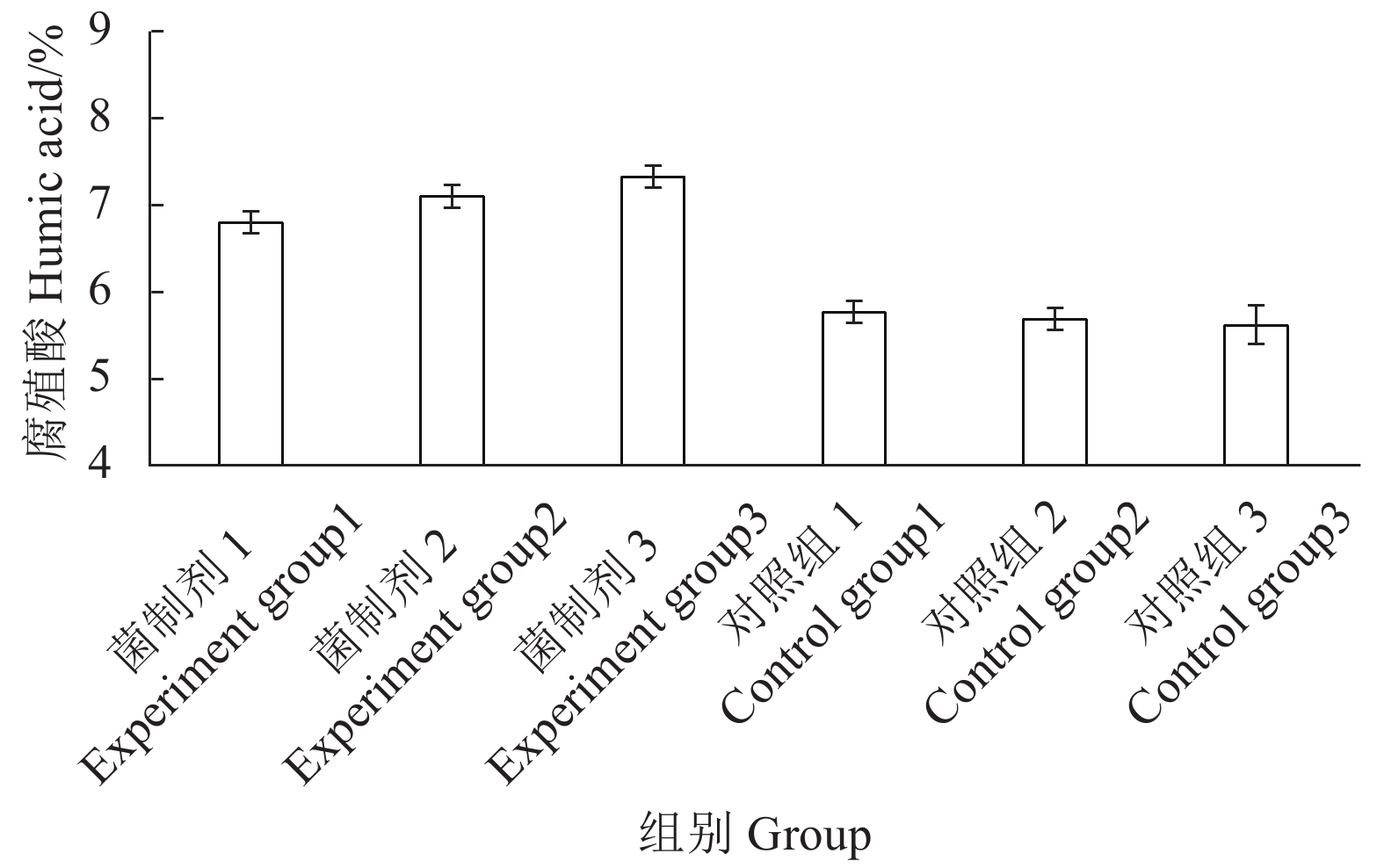
腐殖酸是堆肥过程中生成的最具代表性的次生产物,对于肥料的发酵腐熟程度具有一定的表征性,是衡量堆肥品质的重要指标。培养15 d后,测定添加15株菌菌制剂的试验组腐殖酸平均含量是7.08%,是对照组腐殖酸平均含量(5.68%)的1.25倍,如图7所示。试验组高于对照组,添加15株菌的菌制剂有利于油茶壳堆肥腐殖酸的生成,提高了堆肥品质。
3. 讨论
目前,研究农业副产品堆肥中微生物的影响和作用机理的研究报道已经比较普遍。其中有关微生物水解酶的研究已经成为研究的热点之一,且已有很多研究证实,芽孢杆菌分泌的水解酶对纤维素或蛋白质的降解尤为关键。如Liu等[37]研究了城市固体废物堆肥中不同堆肥阶段产纤维素酶的关键微生物种群,发现纤维素的有效分解依赖于细菌和真菌的协同作用。聂文翰等[38]将含有芽孢杆菌的复合菌剂添加到秸秆堆肥中,施加这种秸秆堆肥后,土壤纤维素酶活性提高了30.8%,普通白菜产量比对照组提高46.4%。从高温堆肥中分离到1株芽孢杆菌(Geobacillus stearothermophilus),在最适条件下能分泌大量的降解木质纤维素的酶,被认为是一种潜在的提高堆肥效率的菌种[39]。在农业副产品豆粕微生物发酵中添加蜡状芽孢杆菌(Bacillus cereus)和粪肠球菌,抗原蛋白降解率达到90%以上[40]。本研究探索了自然状态下油茶壳堆肥中的芽孢杆菌,9株芽孢杆菌初步显示具有一定的水解酶功能特性,其中同时具有淀粉酶、纤维素酶、蛋白酶3种水解酶活性的菌株有6株。因此,在后续研究中,利用微生物发酵工艺条件优化以及酶活测定方法,集中对产酶活性较强的菌株的研究,以期获得高产纤维素酶或蛋白酶的微生物,有助于提升油茶壳堆肥的生产效率和提高堆肥品质,并将在饲用酶制剂中具有较大的应用潜力。
此外,利用微生物来消除农业生产中的农药污染是一种非常安全、经济、有效的方法[41]。本研究从油茶壳堆肥中筛选到蜡状芽孢杆菌,即菌株Bacillus cereus YX02。关于蜡状芽孢杆菌的报道已有很多,如研究了对重金属铅、锌、铬有强吸附能力的一株蜡状芽孢杆菌[42],完成了蜡状芽孢杆菌吸附铅的研究[43],分离鉴定了强抗镉蜡状芽孢杆菌[44],发现蜡状芽孢杆菌对毒死蜱有很高的降解率[45]。也有研究证实,利用植物高羊茅与羊茅共植,结合蜡状芽孢杆菌,可显著修复被重金属与十溴二苯醚BDE-209共污染的土壤[46];从矿山尾矿中分离到的蜡状芽孢杆菌(T1B3),具有促进植物生长的特性,并可以提高植物修复重金属污染的效率[47]。这些结论表明了本研究发现的菌株(Bacillus cereus YX02)可能具有处理重金属、促进植物生长和消除农药污染的应用价值。另外,本研究中筛选到的菌株FYF01是弯曲芽孢杆菌(Bacillus flexus)。已有研究表明某些弯曲芽孢杆菌具有促进植物生长、处理造纸废水、杀灭害虫等应用价值。如弯曲芽孢杆菌在盐胁迫下能促进寄主植物生长,在盐渍土的植物修复中具有潜在的应用前景[48];一株弯曲芽孢杆菌能够降解碱木质素,利用该菌能够处理复杂的造纸废水,是一种很有前途的微生物修复剂[49];一种弯曲芽孢杆菌对蒽醌类染料有脱色和脱毒作用,可用于染料废水的生物处理[50];弯曲芽孢杆菌可以成为生物杀虫剂,用作合成杀虫剂的环境安全替代品[51]。在今后的研究中,将继续挖掘菌株上述方面的功能,或将为油茶壳堆肥产品增加改善生态环境的作用提供理论依据和菌种资源。
当今世界常年大量使用化学农药和肥料,土壤结构被严重污染和破坏,这给生态环境带来灾难性后果。因此,各国竞相研究和开发微生物资源,希望研制出高效、无毒、无污染的微生物肥料和农药。开发微生物复合菌制剂,利用群落协同作用以增强微生物的处理能力已经成为一种发展趋势。比如韩国蔚山的B3(Bio-Best Bacillus)工艺,是先进的污水处理系统。它的主要原理是利用一个以芽孢杆菌占优势的微生物群落处理污水,能够有效地去除氮、磷和有机物[52]。本研究中这些功能性芽孢杆菌,在今后的研究中,将继续探究它们在促进植物生长、处理重金属、消除污染或杀灭害虫等方面的功能。以这些功能微生物作为优势菌种,进行复合培养,提高它们的产酶能力和菌密度,充分利用功能性芽孢杆菌种群的协同作用。在油茶壳堆肥中发现的这些独特功能的芽孢杆菌,或将对开发出一种既可以消除土壤污染,又能同时杀死农业害虫的生物肥料有所启发。
4. 结论
本研究通过高通量测序技术,确认芽孢杆菌科(Bacillaceae)是油茶壳自然堆肥中的优势菌科,其占比达到55.58%,对油茶壳堆肥中微生物的群落结构有了进一步了解。通过6组培养基的堆肥微生物培养试验,筛选出相对最佳的生长培养基,获得了实验室环境下物种多样性相对比较丰富的堆肥芽孢杆菌菌群。最终分离出15株芽孢杆菌,其中有3株菌明确了种属,分别是Bacillus cereus YX02,Brevibacterium oceani YX15,和Bacillus flexus FYF01,它们有促进植物生长、消除污染和杀灭农业害虫的潜在应用价值。这些芽孢杆菌有9株菌初步显示具有一定的水解酶功能特性,包括Bacillus sp. YX11等6株菌同时具有3种水解酶的特性。如菌株Bacillus sp. YX11的蛋白酶活力达到27.07±3.28 U·mL−1,淀粉酶活力达123.97±3.19 U·mL−1,纤维素酶活力达15.75±0.23 U·mL−1。这表明这些菌株在油茶壳堆肥和饲用酶制剂等方面有较大的应用潜力。将分离到的15株芽孢杆菌制备复合菌剂,在油茶壳堆肥中获得较好的初步应用效果,促进腐殖酸的生成,提高了堆肥品质。
-
表 1 菌制剂应用试验配方
Table 1 Proposed formulations of microbial inoculants
组别
Group油茶壳
Camellia shell/g菌液
microbial inoculants/mL糖蜜
Molasses/mL花生枯
Peanut cake/g尿素
Urea/g水
H2O/mL菌制剂 experiment group 15 15 6 1.2 1.2 100 对照组 control group 15 0 6 1.2 1.2 115 表 2 菌株形态特征
Table 2 Morphological characteristics of isolated Bacillus spp
菌株编号
Strains菌落质地
Colony texture菌落颜色
Colony color菌落形态
Colony morphologyYX01 干燥、皱褶 dry and wrinkled 半透明色 translucent color 不规则圆形,有毛边 irregular round with rough edges YX02 干燥、皱褶 dry and wrinkled 乳白色 milky white 较规则圆形,中间隆起 regular round, middle uplift YX03 光滑、湿润 smooth and moist 半透明色 translucent color 较规则圆形 regular round YX07 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX08 光滑、湿润 smooth and moist 半透明色 translucent color 圆形 round YX11 湿润、黏稠 wet and sticky 乳白色 milky white 圆形 round YX12 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX13 干燥、皱褶 dry and wrinkled 枯黄色 withered yellow 不规则圆形,有毛边 irregular round with rough edges YX15 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round YX16 光滑、湿润 smooth and moist 乳白色 milky white 圆形 round FYF01 干燥、皱褶 dry and wrinkled 乳白色 milky white 不规则圆形,有毛边 irregular round with rough edges FYF04 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形 regular round FYF07 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形,中间隆起 regular round, middle uplift FYF08 干燥、皱褶 dry and wrinkled 半透明色 translucent color 不规则圆形,有毛边 irregular round with rough edges FYF10 光滑、湿润 smooth and moist 乳白色 milky white 较规则圆形 regular round 表 3 菌株16S rDNA鉴定结果
Table 3 Identifications by 16S rDNA
序号 Serial number 编号 Number 菌种分类 Species classification 1 YX01 Bacillus sp. 2 YX02 Bacillus cereus 3 YX03 Bacillus sp. 4 YX07 Bacillus sp. 5 YX08 Bacillus sp. 6 YX11 Bacillus sp. 7 YX12 Bacillus sp. 8 YX13 Bacillus sp. 9 YX15 Brevibacterium oceani 10 YX16 Bacillus sp. 11 FYF01 Bacillus flexus 12 FYF04 Bacillus sp. 13 FYF07 Bacillus sp. 14 FYF08 Bacillus sp. 15 FYF10 Bacillus sp. 表 4 不同培养基上菌落直径与透明圈直径比
Table 4 Ratio of transparent ring diameter to colony diameter on different mediums
菌株编号
Strains脱脂乳糖培养基
Skim milk medium淀粉培养基
Starch medium刚果红培养基
Congo red medium透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratio透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratio透明圈直径D
Transparent ring
diameter/mm菌落直径d
Colony
diameter/mm直径比D/d
Diameter
ratioYX01 0.0 7.5 0.00 13.0 7.5 1.73 18.0 5.0 3.60 YX02 28.0 26.5 1.06 0.0 16.0 0.00 0.0 11.0 0.00 YX03 0.0 0.0 0.00 0.0 4.0 0.00 20.0 8.0 2.50 YX07 0.0 0.0 0.00 0.0 6.5 0.00 0.0 8.5 0.00 YX08 0.0 0.0 0.00 0.0 11.0 0.00 0.0 2.0 0.00 YX11 25.0 20.0 1.25 19.5 6.0 3.25 30.0 11.0 2.73 YX12 0.0 0.0 0.00 0.0 5.0 0.00 0.0 8.0 0.00 YX13 29.0 23.0 1.26 20.0 8.0 2.50 18.0 8.5 2.12 YX15 0.0 0.0 0.00 0.0 6.5 0.00 0.0 10.0 0.00 YX16 0.0 0.0 0.00 0.0 4.0 0.00 0.0 7.0 0.00 FYF01 14.0 12.0 1.17 16.0 6.0 2.67 32.0 6.5 4.92 FYF04 30.0 21.5 1.39 14.0 7.0 2.00 24.5 6.0 4.08 FYF07 26.0 19.0 1.37 20.0 11.5 1.74 24.0 9.0 2.67 FYF08 0.0 0.0 0.00 0.0 7.0 0.00 0.0 2.0 0.00 FYF10 25.5 19.5 1.31 18.0 12.5 1.44 25.0 9.0 2.78 -
[1] HU J B, SHI Y, LIU Y, et al. Anatomical structure of Camellia oleifera shell [J]. Protoplasma, 2018, 255(6): 1777−1784. DOI: 10.1007/s00709-018-1271-8
[2] 覃佐东, 谢吉勇, 黄生辉, 等. 油茶壳综合利用研究进展 [J]. 生物加工过程, 2016, 14(5):74−78. DOI: 10.3969/j.issn.1672-3678.2016.05.014 QIN Z D, XIE J Y, HUANG S H, et al. Progress in utilization of camellia shells [J]. Chinese Journal of Bioprocess Engineering, 2016, 14(5): 74−78.(in Chinese) DOI: 10.3969/j.issn.1672-3678.2016.05.014
[3] SHRESTHA K, SHRESTHA P, WALSH K B, et al. Microbial enhancement of compost extracts based on cattle rumen content compost - characterisation of a system [J]. Bioresource Technology, 2011, 102(17): 8027−8034. DOI: 10.1016/j.biortech.2011.06.076
[4] SONG C, ZHANG Y, XIA X, et al. Effect of inoculation with a microbial consortium that degrades organic acids on the composting efficiency of food waste [J]. Microbial Biotechnology, 2018, 11(6): 1124−1136. DOI: 10.1111/1751-7915.13294
[5] FANG Y, JIA X B, CHEN L J, et al. Effect of thermotolerant bacterial inoculation on the microbial community during sludge composting [J]. Canadian Journal of Microbiology, 2019, 65(10): 750−761. DOI: 10.1139/cjm-2019-0107
[6] THATOI H, BEHERA B C, MISHRA R R, et al. Biodiversity and biotechnological potential of microorganisms from mangrove ecosystems: A review [J]. Annals of Microbiology, 2013, 63(1): 1−19. DOI: 10.1007/s13213-012-0442-7
[7] 胡亚杰, 韦建玉, 卢健, 等. 枯草芽孢杆菌在农作物生产上的应用研究进展 [J]. 作物研究, 2019, 33(2):167−172. HU Y J, WEI J Y, LU J, et al. Research prog ress of Bacillus subtilis application in crops production [J]. Crop Research, 2019, 33(2): 167−172.(in Chinese)
[8] MAYENDE L, WILHELMI B, PLETSCHKE B. Cellulases (CMCases) and polyphenol oxidases from thermophilic Bacillus spp. isolated from compost [J]. Soil Biology and Biochemistry, 2006, 38(9): 2963−2966. DOI: 10.1016/j.soilbio.2006.03.019
[9] JOSÉ V C. Inoculating composted pine bark with beneficial organisms to make a disease suppressive compost for container production in mexican forest nurseries [J]. Plants Journal, 2004, 2(5): 181−185.
[10] KRAUSE M S, DE CEUSTER T J J, TIQUIA S M, et al. Isolation and characterization of rhizobacteria from composts that suppress the severity of bacterial leaf spot of radish [J]. Phytopathology, 2003, 93(10): 1292−1300. DOI: 10.1094/PHYTO.2003.93.10.1292
[11] 付冰妍, 孙向阳, 余克非, 等. 芽孢杆菌B01固态发酵及其对园林废弃物堆肥的影响 [J]. 环境科学研究, 2020(2):450−457. FU B Y, SUN X Y, YU K F, et al. Solid state fermentation of Bacillus B01 and its effect on green waste composting [J]. Research of Environmental Sciences, 2020(2): 450−457.(in Chinese)
[12] 余培斌, 杜晶, 陈建新. 高温好氧堆肥过程中芽孢杆菌的筛选、鉴定及应用 [J]. 食品与发酵工业, 2020, 46(12):199−205, 212. YU P B, DU J, CHEN J X. Study on screening and identification of Bacillus in the process of high-temperature aerobic composting and its application [J]. Food and Fermentation Industries, 2020, 46(12): 199−205, 212.(in Chinese)
[13] ZHANG J P, YING Y, LI X B, et al. Physical and chemical properties of Camellia oleifera shell composts with different additives and its maturity evaluation system [J]. Environmental Science and Pollution Research, 2020, 27(28): 35294−35302. DOI: 10.1007/s11356-020-09861-3
[14] 詹孝慈, 罗在柒, 武忠亮, 等. 不同氮源及微生物菌剂能提高油茶壳堆肥效果 [J]. 分子植物育种, 2019, 17(12):4153−4160. ZHAN X C, LUO Z Q, WU Z L, et al. Different nitrogen sources and microbial inoculants could improve the composting of Camellia oleifera shell [J]. Fenzi Zhiwu Yuzhong (Molecular Plant Breeding), 2019, 17(12): 4153−4160.(in Chinese)
[15] ZHANG J P, YING Y, YAO X H. Effects of turning frequency on the nutrients of Camellia oleifera shell co-compost with goat dung and evaluation of co-compost maturity [J]. PLoS One, 2019, 14(9): e0222841. DOI: 10.1371/journal.pone.0222841
[16] 秦楠, 栗东芳, 杨瑞馥. 高通量测序技术及其在微生物学研究中的应用 [J]. 微生物学报, 2011, 51(4):445−457. QIN N, LI D F, YANG R F. Next-generation sequencing technologies and the application in microbiology-A review [J]. Acta Microbiologica Sinica, 2011, 51(4): 445−457.(in Chinese)
[17] 葛慈斌, 蓝江林, 刘波, 等. 解淀粉芽胞杆菌FJAT-8754产纤维素酶和淀粉酶发酵动力学模型的构建 [J]. 福建农业学报, 2019, 34(6):697−704. GE C B, LAN J L, LIU B, et al. Kinetics of cellulase and amylase-producing fermentation of Bacillus amylolique faciens FJAT-8754 [J]. Fujian Journal of Agricultural Sciences, 2019, 34(6): 697−704.(in Chinese)
[18] 赵国群, 牛梦天, 卢士康, 等. 梨渣固态发酵培养多粘类芽孢杆菌的工艺 [J]. 农业工程学报, 2016, 32(7):303−308. ZHAO G Q, NIU M T, LU S K, et al. Cultivation of Paenibacillus polymyxa by solid-state fermentation of pear residues [J]. Transactions of the Chinese Society of Agricultural Engineering (Transactions of the CSAE), 2016, 32(7): 303−308.(in Chinese)
[19] 胡瑞萍, 丁贤, 李来好, 等. 响应面法优化枯草芽孢杆菌NHS1产芽孢发酵培养 [J]. 生态学杂志, 2018, 37(2):605−612. HU R P, DING X, LI L H, et al. Optimization of fermentation medium composition by response surface methodology for the spore production of Bacillus subtilis [J]. Chinese Journal of Ecology, 2018, 37(2): 605−612.(in Chinese)
[20] 董佩佩, 汪祥燕, 刘元香, 等. 一株凝结芽孢杆菌(Bacillus coagulans)发酵培养基的优化 [J]. 中国酿造, 2018, 37(4):28−32. DOI: 10.11882/j.issn.0254-5071.2018.04.006 DONG P P, WANG X Y, LIU Y X, et al. Optimization of fermentation medium of Bacillus coagulans [J]. China Brewing, 2018, 37(4): 28−32.(in Chinese) DOI: 10.11882/j.issn.0254-5071.2018.04.006
[21] MATHAKIYA R A, ROY A, NANDASANA K N, et al. Evaluation of a rapid molecular method for detection of Listeria monocytogenes directly from broth culture[J]. Veterinary World, 2009, 2(5): 177-178.
[22] 何深宏, 程方俊, 罗干, 等. 解淀粉芽孢杆菌高产纤维素酶菌株的筛选与鉴定 [J]. 福建农业学报, 2020, 35(7):781−787. HE S H, CHENG F J, LUO G, et al. Screening and identifying cellulase-producing Bacillus amyloliquefaciens [J]. Fujian Journal of Agricultural Sciences, 2020, 35(7): 781−787.(in Chinese)
[23] YU D, TONG W, CHEN Y, et al. Improvement of bacterial genomic DNA extraction in clinical specimens [J]. Chinese Journal of Microecology, 2007, 6(19): 519−520.
[24] 王佳楠, 石妍云, 郑力燕, 等. 石油降解菌的分离鉴定及4株芽胞杆菌种间效应 [J]. 环境科学, 2015, 36(6):2245−2251. WANG J N, SHI Y Y, ZHENG L Y, et al. Isolation and identification of petroleum degradation bacteria and interspecific interactions among four Bacillus strains [J]. Environmental Science, 2015, 36(6): 2245−2251.(in Chinese)
[25] DUNLAP C A, SCHISLER D A, PERRY E B, et al. Bacillus swezeyi sp. nov. and Bacillus haynesii sp. nov., isolated from desert soil [J]. International Journal of Systematic and Evolutionary Microbiology, 2017, 67(8): 2720−2725. DOI: 10.1099/ijsem.0.002007
[26] ADAWAREN E O, DU PLESSIS M, SULEMAN E, et al. The complete mitochondrial genome of Gyps coprotheres (Aves, Accipitridae, Accipitriformes): Phylogenetic analysis of mitogenome among raptors [J]. PeerJ, 2020, 8: e10034. DOI: 10.7717/peerj.10034
[27] QIAN Y, SUN Y, ZHONG L, et al. The GATA-Type Transcriptional Factor Are1 Modulates the Expression of Extracellular Proteases and Cellulases in Trichoderma reesei [J]. International Journal of Molecular Sciences, 2019, 20(17): 4100. DOI: 10.3390/ijms20174100
[28] ELAMARY R, SALEM W M. Optimizing and purifying extracellular amylase from soil bacteria to inhibit clinical biofilm-forming bacteria [J]. PeerJ, 2020, 8: e10288. DOI: 10.7717/peerj.10288
[29] HAJIABADI S, MASHREGHI M, REZA BAHRAMI A, et al. Isolation and molecular identification of cellulolytic bacteria from Dig Rostam hot spring and study of their cellulase activity [J]. BIOCELL, 2020, 44(1): 63−71. DOI: 10.32604/biocell.2020.08171
[30] WU C L, LIU D, YANG X H, et al. Improving production of protease from Pseudoalteromonas sp. CSN423 by random mutagenesis [J]. Marine Biotechnology (New York, N Y), 2016, 18(5): 610−618. DOI: 10.1007/s10126-016-9721-9
[31] 曹丹, 彭浩, 兰阿峰, 等. 一株α-淀粉酶产生菌的分离、鉴定及产酶条件研究 [J]. 食品研究与开发, 2020, 41(6):169−174. CAO D, PENG H, LAN A F, et al. Isolation, identification and enzyme production conditions of an α-amylase producing strain [J]. Food Research And Developmen, 2020, 41(6): 169−174.(in Chinese)
[32] 冯红梅, 秦永胜, 李筱帆, 等. 高温纤维素降解菌群筛选及产酶特性 [J]. 环境科学, 2016, 37(4):1546−1552. FENG H M, QIN Y S, LI X F, et al. Screening and enzyme production characteristics of thermophilic cellulase-producing strains [J]. Environmental Science, 2016, 37(4): 1546−1552.(in Chinese)
[33] 附录B(规范性附录)总腐植酸含量的测定方法[J]. 腐植酸, 2016(2): 47−48. Appendix B (normative appendix) determination method of total humic acid content[J]. Humic acid, 2016 (2): 47 − 48. (in Chinese).
[34] JAIN S, SALUJA B, GUPTA A, et al. Validation of arsenic resistance in Bacillus cereus strain AG27 by comparative protein modeling of arsC gene product [J]. The Protein Journal, 2011, 30(2): 91−101. DOI: 10.1007/s10930-011-9305-5
[35] BHADRA B, RAGHUKUMAR C, PINDI P K, et al. Brevibacterium oceani sp. nov., isolated from deep-sea sediment of the Chagos Trench, Indian Ocean [J]. International Journal of Systematic and Evolutionary Microbiology, 2008, 58(1): 57−60. DOI: 10.1099/ijs.0.64869-0
[36] JEBELI M A, MALEKI A, AMOOZEGAR M A, et al. Bacillus flexus strain As-12, a new arsenic transformer bacterium isolated from contaminated water resources [J]. Chemosphere, 2017, 169: 636−641. DOI: 10.1016/j.chemosphere.2016.11.129
[37] LIU D, LI M, XI B, et al. Metaproteomics reveals major microbial players and their biodegradation functions in a large‐scale aerobic composting plant [J]. Microbial Biotechnology, 2015, 8(6): 950−960. DOI: 10.1111/1751-7915.12290
[38] 聂文翰, 戚志萍, 冯海玮, 等. 复合菌剂秸秆堆肥对土壤碳氮含量和酶活性的影响 [J]. 环境科学, 2017, 38(2):783−791. NIE W H, QI Z P, FENG H W, et al. Steaw composts with composite inoculants and theie effects on soil caebon and niteogen contents and enzyme activity [J]. Environmental Science, 2017, 38(2): 783−791.(in Chinese)
[39] WANG M, MIAO J, WANG X, et al. Genomic and transcriptome analyses of a thermophilic bacterium Geobacillus stearothermophilus B5 isolated from compost reveal its enzymatic basis for lignocellulose degradation [J]. Microorganisms, 2020, 8(9): 1−18.
[40] 王腾浩, 潘岳龙, 沈炜, 等. 蜡样芽孢杆菌与粪肠球菌协同发酵豆粕工艺条件优化 [J]. 饲料研究, 2020, 43(3):74−77. WANG T H, PAN Y L, SHEN W, et al. The optimization of fermentation conditions of soybean meal by using Bacillus Cereus and Enterococcus Faecalis [J]. Feed Research, 2020, 43(3): 74−77.(in Chinese)
[41] LI Y, CHI M, GE X, et al. Identification of a novel hydrolase encoded by hy-1 from Bacillus amyloliquefaciens for bioremediation of carbendazim contaminated soil and food [J]. International journal of agricultural and biological engineering, 2019, 12(2): 218−224. DOI: 10.25165/j.ijabe.20191202.4190
[42] 阚洪媛, 杨世鑫, 孙梁伦, 等. 一株耐铅、锌、铬菌株的分离鉴定及其吸附能力 [J]. 微生物学通报, 2020(12):3974−3986. KAN H Y, YANG S X, SUN L L, et al. Isolation, identification and adsorption capacity of a strain resistant to lead, zinc and chromium [J]. Microbiology China, 2020(12): 3974−3986.(in Chinese)
[43] 潘建华, 刘瑞霞. 蜡状芽孢杆菌Bacillus cereus吸附铅的研究 [J]. 环境科学, 2004, 25(2):166−169. DOI: 10.3321/j.issn:0250-3301.2004.02.034 PAN J H, LIU R X. Biosorption of Pb 2+ by Bacillus cereus Biomass [J]. Environmental Science, 2004, 25(2): 166−169.(in Chinese) DOI: 10.3321/j.issn:0250-3301.2004.02.034
[44] 呼庆, 齐鸿雁, 窦敏娜, 等. 强抗镉蜡状芽孢杆菌的分离鉴定及其抗性机理 [J]. 环境科学, 2007, 28(2):427−430. DOI: 10.3321/j.issn:0250-3301.2007.02.038 HU Q, QI H Y, DOU M N, et al. Isolation, molecular characterization and resistance mechanism study on a cadmium hyperresistant Bacillus cereus [J]. Environmental Science, 2007, 28(2): 427−430.(in Chinese) DOI: 10.3321/j.issn:0250-3301.2007.02.038
[45] 段海明. 两株蜡状芽孢杆菌对毒死蜱的降解动力学研究 [J]. 中国生态农业学报, 2013, 21(2):207−211. DUAN H M. Kinetics of chlorpyrifos degradation by Bacillus cereus strains [J]. Chinese Journal of Eco-Agriculture, 2013, 21(2): 207−211.(in Chinese)
[46] LU M, ZHANG Z Z. Phytoremediation of soil co-contaminated with heavy metals and deca-BDE by co-planting of Sedum alfredii with tall fescue associated with Bacillus cereus JP12 [J]. Plant and Soil, 2014, 382(1/2): 89−102.
[47] NAYAK A K, PANDA S S, BASU A, et al. Enhancement of toxic Cr (VI), Fe, and other heavy metals phytoremediation by the synergistic combination of native Bacillus cereus strain and Vetiveria zizanioides L [J]. International Journal of Phytoremediation, 2018, 20(7): 682−691. DOI: 10.1080/15226514.2017.1413332
[48] XIONG Y W, LI X W, WANG T T, et al. Root exudates-driven rhizosphere recruitment of the plant growth-promoting rhizobacterium Bacillus flexus KLBMP 4941 and its growth-promoting effect on the coastal halophyte Limonium sinense under salt stress [J]. Ecotoxicology and Environmental Safety, 2020, 194: 110374. DOI: 10.1016/j.ecoenv.2020.110374
[49] KUMAR A, PRIYADARSHINEE R, SINGHA S, et al. Biodegradation of alkali lignin by Bacillus flexus RMWW II: Analyzing performance for abatement of rice mill wastewater [J]. Water Science and Technology, 2019, 80(9): 1623−1632. DOI: 10.2166/wst.2020.005
[50] MOHANTY S S, KUMAR A. Response surface methodology mediated optimization of Indanthrene Blue RS by a novel isolated bacterial strain Bacillus flexus TS8 [J]. Water Environment Research, 2020, 92(4): 569−578. DOI: 10.1002/wer.1246
[51] REDA F M, HASSANEIN W A, MOABED S, et al. Potential exploitation of Bacillus flexus biofilm against the cowpea weevil, Callosobruchus maculatus (F.) (Coleoptera: Bruchidae) [J]. Egyptian Journal of Biological Pest Control, 2020, 30(1): 1−7. DOI: 10.1186/s41938-020-0205-x
[52] NAM J H, BAE W, LEE D H. Oceanobacillus caeni sp. nov., isolated from a Bacillus-dominated wastewater treatment system in Korea [J]. International Journal of Systematic and Evolutionary Microbiology, 2008, 58: 1109−1113. DOI: 10.1099/ijs.0.65335-0
-
期刊类型引用(7)
1. 曾斌,唐敏,唐伟,于桂阳,曾健青. 花生粕和花生秸秆在动物饲用中的研究进展. 中国饲料. 2023(05): 152-162 .  百度学术
百度学术
2. 田永国,胡廷会,丁广刚,成良强,饶庆琳,姜敏,王金花,吕建伟,王军. 花生荚果发育和成熟阶段的秸秆品质变化分析. 花生学报. 2023(02): 91-95 .  百度学术
百度学术
3. 马雪儿,边高瑞,孙新文,沈文,Rizabek,毛胜勇,成艳芬,王新峰. 发酵核桃叶在哈萨克羊瘤胃内降解特性研究. 饲料研究. 2022(08): 6-13 .  百度学术
百度学术
4. 陈恩瑶,王志敬. 花生秸秆在草食动物中的应用. 养殖与饲料. 2022(12): 55-59 .  百度学术
百度学术
5. 张耀,赵菁菁,陈鑫珠,黄小云,黄秀声,黄勤楼,庄益芬. 百香果果皮和果藤在山羊瘤胃降解特性研究. 畜牧与兽医. 2021(07): 52-57 .  百度学术
百度学术
6. 董朝霞,章瑜,陈鑫珠,黄小云,黄秀声,黄勤楼,庄益芬. 甘薯藤和甘薯皮山羊瘤胃降解率的动态变化. 江苏农业科学. 2021(11): 115-119 .  百度学术
百度学术
7. 吕建伟,姜敏,田永国,胡廷会,成良强,饶庆琳,王金花,王军. 花生植株养分分析及饲用性评价. 中国油料作物学报. 2021(06): 1031-1041 .  百度学术
百度学术
其他类型引用(0)




 下载:
下载: