Sequences and Spatiotemporal Expressions of Vitellogenin and Vitellogenin Receptor Genes of Tessaratoma papillosa
-
摘要:目的 为荔枝蝽Tessaratoma papillosa的产卵繁殖行为提供分子层面的理论基础,并为荔枝蝽防治的靶点筛选提供有益思路。方法 采用转录组测序的方法,对荔枝蝽不同发育时期及组织进行转录组测序。通过筛选荔枝蝽的转录组数据和分子克隆的方法获得荔枝蝽卵黄原蛋白及其受体基因,并利用实时荧光定量PCR(qRT-PCR)分析其在不同发育阶段和组织部位的时空表达情况。结果 获得荔枝蝽3个卵黄原蛋白基因(T.papi_Vg1,T.papi_Vg2,T.papi_Vg3)和1个卵黄原受体蛋白基因(T.papi_VgRs)。对4个基因进行分析,发现其均具有典型的保守结构域,是典型的昆虫Vg和VgRs基因。从进化关系看,荔枝蝽的Vg和VgRs基因的分子进化与物种之间的进化关系较为匹配。qRT-PCR结果显示Vg1基因在雌虫各个组织中表达量都比较高,雄成虫中仅在淋巴液中表达量较高,而Vg2和Vg3基因仅在雌虫脂肪体中较高表达。VgRs的表达与Vg的表达部位基本一致,在雌虫卵巢中表达量最高,其次是雌虫、雄虫淋巴液和若虫的脂肪体当中,在若虫触角、雄虫触角和雄虫精巢中也有少量表达。结论 获得了荔枝蝽3个卵黄原蛋白基因和1个卵黄原蛋白受体基因,对其结构和进化关系进行探讨,并对其时空表达情况进行分析,为后续对荔枝蝽新防治靶标的筛选奠定基础。Abstract:Objective Molecular information associated with the oviposition and reproduction of Tessaratoma papillosa was studied for control of the pest on lychee trees.Method Transcriptome sequencing of T. papillosa in various tissues and developmental stages was conducted. The vitellogenin and vitellogenin receptor genes were obtained by screening the transcriptome database and applying molecular cloning methods. Temporal and spatial expressions of the genes were analyzed using qRT-PCR.Result Three vitellogenin genes (i.e., T. papi_Vg1
, Vg2, and Vg3) and one receptor gene, T. papi_VgRs, were obtained after screening. Homologous analysis showed the genes contained conserved domains typical in the Vg and VgRs of insects. The molecular evolution of Vg and VgRs of T. papillosa paralleled that of the species. The temporal and spatial expressions of Vg1 shown by qRT-PCR were relatively high in all female tissues, but only the lymphatic fluid in adult males, whereas those of Vg2 and Vg3 highly expressed only in female adipose tissue. The expression of VgRs, as well as Vg, was highest in female ovary, followed by female, male lymph fluid, nymph adipose tissue, and minute in nymph antenna, male antenna, and male testis. Conclusion The structures and evolution of the 3 vitellogenin genes and one vitellogenin receptor gene were analyzed. The information on the spatiotemporal expressions of the genes would aid target selection in study for the control ofT. papillosa. -
0. 引言
【研究意义】荔枝蝽Tessaratoma papillosa隶属于半翅目Hemiptera荔蝽科Tessaratomidae,是我国及东南亚等地荔枝、龙眼产区的重要害虫。荔枝蝽以成虫和若虫刺吸危害果树幼枝、嫩芽、花和幼果,导致果树嫩枝萎蔫、落花落果。成、若虫臭腺分泌物还可灼伤植株幼嫩部位,造成枯死,同时还可传播龙眼鬼帚病[1-2],荔枝蝽常年危害严重,造成巨大的经济损失。在发生严重年份,荔枝、龙眼可减产20%~30%,甚至部分地区减产达到70%~80%,甚至绝收[3]。【前人研究进展】卵黄原蛋白(Vg)是一类大分子糖脂复合蛋白,广泛存在于非哺乳类性成熟卵生雌性动物的血淋巴、脂肪体和卵中,是几乎所有卵生动物卵黄蛋白的前体,能为正在发育的胚胎提供氨基酸、脂肪、碳水化合物、维生素和微量元素等营养和功能性物质[4-8]。目前已知的昆虫卵黄原蛋白序列约30条,主要有蜚蠊目的美洲大蠊Periplaneta americana[9],德国小蠊Blattella germanica[10];鳞翅目的柞蚕Antherea pernyi[11],野桑蚕Bombyx mandarina[12],眉纹天蚕蛾Samia cynthia,绿尾大蚕蛾Actias ningpoana,半目大蚕蛾Antheraea yamamai,舞毒蛾Lymantria dispar;膜翅目的意大利蜜蜂Apis mellifera[13],蚜小蜂Aphytis sp.;双翅目的埃及伊蚊Aedes aegypti[14],疟蚊Anopheles sp.;半翅目的褐飞虱Nilaparvata lugens[15]等。昆虫卵黄原蛋白一般在雌性成虫的脂肪体合成,随后进入血淋巴,经血淋巴运输到卵巢,与膜上卵黄原蛋白受体结合,经胞吞作用,使卵黄原蛋白进入卵巢细胞,并行使功能[7-8, 16- 17]。昆虫卵黄原蛋白的mRNA全长大约为6 000 bp,在整个加工过程中,经蛋白水解,在完全变态昆虫和不完全变态昆虫中切割成两段或多个小的片段[7, 17-18]。根据卵黄原蛋白前体被切割的形式,可以将其分为三类:①没有被酶切的蛋白前体,仅含有一个大分子量亚基[7];②酶切为一个大分子量的亚基(>180 ku)和一个小分子量的亚基(<50 ku),绝大多数完全变态昆虫中的Vg蛋白前体属于这一类型[7, 19];③酶解为几个分子量约为80~110 ku的多肽,大部分不完全变态昆虫中的Vg蛋白前体属于这一类型[17]。昆虫的卵黄原蛋白受体(VgRs)属于低密度脂蛋白受体家族成员,昆虫的VgRs具有LDLR(low density lipoprotein receptor)家族典型的保守结构域[17, 20- 21]。一般来说,VgRs在成虫羽化前的卵巢中合成,随后经过血淋巴运输到卵巢与卵黄原蛋白结合,昆虫的VgRs具有卵巢特异性,是卵黄原蛋白Vg的专一性胞吞作用受体,可介导Vg进入昆虫卵母细胞,而后沉淀积累形成昆虫生殖必需的卵黄蛋白[8, 22]。VgRs与昆虫卵巢激活,卵黄发生,卵子形成密切相关,同时在昆虫信息交流、社会分化、行为构建以及免疫调控等行为过程中起到至关重要的作用。【本研究切入点】荔枝蝽新成虫大规模发生以后,由于抗药性强[23],在采取化学防治时不能产生较好的防治效果。而通过人工释放平腹小蜂Anastatus fulloi进行生物防治较为可行,但平腹小蜂抗寒能力较弱,容易被农药杀伤,野外种群需要较多营养使种群复壮,需要在防治时错峰喷洒农药才能产生较好的防治效果[24]。在愈加重视食品安全和绿色植保的今天,筛选出新的荔枝蝽防治靶标迫在眉睫。本研究通过分子生物学技术,从基因层面分析荔枝蝽的产卵过程。【拟解决的关键问题】通过转录组获得荔枝蝽卵黄原蛋白及其受体基因序列,并分析其进化关系、结构和时空表达情况。为了解荔枝蝽产卵的生理过程提供分子层面的信息,同时亦可为从卵期防控荔枝蝽的发生奠定理论基础。
1. 材料与方法
1.1 供试昆虫
野外虫源采自福建省福清市龙眼果园内,将荔枝蝽雌、雄成虫若虫分别保存等待解剖处理。
1.2 荔枝蝽的解剖与处理
荔枝蝽的解剖采用蜡盘解剖法,解剖时先用剪刀剪去翅、足、中胸小盾片和腹侧板,随后自腹部两侧剪开,再横向在消化道上方剪断前胸背板,并用镊子掀开背板,用昆虫针将剩余的组织固定在蜡盘中,注入清水至淹没虫体,在昆虫双目解剖镜下解剖,取得荔枝蝽雌雄成虫和若虫的脂肪体、中肠,雌雄成虫的卵巢和精巢、若虫和雄成虫触角[25]。解剖后得到的组织置于1.5 mL离心管中,在−80 ℃冰箱保存,样品来源及名称如表1所示。
表 1 供试荔枝蝽组织Table 1. Tissues of T. papillosa under study组织 Tissue 名称 Name 雌虫 Female insect TP_M 雌虫卵巢 Female ovary TP_MO 雌虫中肠 Female midgut TP_MM 雌虫脂肪体 Female fat body TP_MF 雄虫 Male insect TP_FM 雄虫触角 Male antenna TP_FMA 雄虫精巢 Male testis TP_FMT 雄虫中肠 Male midgut TP_FMM 雄虫脂肪体 Male fat body TP_FMF 雄虫淋巴液 Male lymph TP_FMH 若虫触角 Nymph antennae TP_AA 若虫中肠 Nymph midgut TP_AM 若虫脂肪体 Nymph fat body TP_AF 若虫 Nymph TP_A 1.3 RNA抽提及全长cDNA的扩增
总RNA的提取使用TRIzol® Reagent(Invitrogen)进行,并严格按照实验手册要求进行。在1 mL TRIzol中加入用研磨柱(使用前用DEPC浸泡并高温灭菌)充分研磨的液氮速冻过的样品,充分混匀,并室温静置5 min。在混合溶液中加入200 μL氯仿,充分震荡混匀,并室温静置5 min(氯仿要在阴凉避光处保存,避免暴露空气中被阳光照射产生毒气)。将混合溶液用4 ℃低温离心机离心15 min,12 000 r·min−1。离心后溶液分为3层,下层为有机相、中层为白色界面、上层为水相,RNA全部在水相中溶解。将上层溶液转移至新的离心管中,加入500 μL预冷的异丙醇(无水乙醇),充分震荡混匀,置于−80 ℃超低温冰箱静置30 min,使RNA沉淀。将样品取出后,4 ℃,12 000 r·min−1,高速离心10 min,倒掉上清,注意不要将沉淀倒出。用500 μL预冷的无RNase 75%乙醇洗涤沉淀,涡旋仪震荡10 s,充分溶解沉淀中的盐离子。4 ℃,12 000 r·min−1,高速离心5 min,小心吸取上清后在室温下静置5 min,使沉淀干燥,加入适量无RNase ddH2O溶解沉淀,即可得到总RNA样品。在分光光度计下检测吸光度,1%琼脂凝胶电泳检测总RNA质量,−80 ℃保存待用。
使用试剂盒ReverTra Ace® qPCR RT Master Mix with gDNA Remover(TOYOBO),并按照说明书进行实验操作。初次使用时,将试剂盒中的4×DN Master Mix与gDNA Remover按照50∶1的比例混合。将2 µg RNA样品在65 ℃水浴锅中热变性5 min,立即置于冰上冷却。在冰上配制反应液(RNA template,2 µg;4×DN Master Mix(gDNA Remover),4 µL;Nuclease-free Water补足16 µL;在加入5×RT Master Mix II,4 µL),将反应液轻轻混匀后,在37 ℃条件下孵育5 min。
将配置好的反应液轻轻混匀后,按照以下程序进行逆转录反应(37 ℃,15 min;50 ℃,5 min;98 ℃,5 min)。反应结束后,将样品稀释10倍放置在−20 ℃备用。
1.4 PCR扩增
引物设计及全长序列扩增:用Geneious R11软件设计引物,本试验所用引物见表2。以荔枝蝽cDNA为模板进行PCR扩增,反应体系:cDNA template 2 µL;2×PCR MIX 25 µL;Primer F 1 µL;Primer R 1 µL;Nuclease-free Water 21 µL。用高保真Taq酶(Takara)扩增目标片段全长序列,反应程序为:95 ℃ 1 min,95 ℃ 30 s,58 ℃ 30 s,72 ℃ 1 min,72 ℃ 7 min,4 ℃保存,反应结束后,将样品进行测序反应,测序委托上海铂尚生物技术有限公司进行。
表 2 PCR扩增引物序列Table 2. PCR primer sequences引物名 Primer name 序列 Sequence Vg1-R-all ATGGCGTGGAGTACAGCCCTTCTC Vg1-F-all TCAGCTTGAAATACAGGCCTCTGG Vg2-R-all CATGTGCTGGTCAAGAACACTT Vg2-F-all TTACAAACTGGAAACACA Vg3-R-all ATGTGGACACAAATTTCACTG Vg3-F-all TTACAAACTGGAAACACATT VgR-R-all AGGCACCAAAGGCTTCCAGTTCG VgR-F-all TTACTCTCATCACTCCCATCACGG 1.5 基因序列的生物信息分析
利用ORF finder预测ORF全长(https://www.ncbi.nlm.nih.gov/orffinder/),利用SignalP5.0进行信号肽预测(http://www.cbs.dtu.dk/services/SignalP/),EXPASY 计算pI/Mw(https://web.expasy.org/compute_pi/),利用SMART软件分析基因的蛋白结构域(http://smart. embl-heidelberg.de/),用Clustal X v2.1软件对荔枝蝽3个卵黄原蛋白的氨基酸序列进行同源比对分析,利用MEGA X软件,建立NJ树(Bootstrap值1000)进行系统进化分析。
1.6 实时定量PCR(Real-time quantitative PCR,qRT-PCR)
qRT-PCR反应使用试剂盒为SYBR® Premix Ex Taq ™ II(Takara),所有操作过程使用的试剂均放置在冰上进行。反应所用的PCR 96孔板或八连管为荧光定量试验专用,引物见表3。
表 3 PCR扩增引物序列Table 3. qRT-PCR primer sequences引物名 Primer name 序列 Sequence Vg1-R-RT TTTCGCCGCATCCTACGCCG Vg1-F- RT ACAGGACCTGCCGCCATCCT Vg2-R- RT CTGGGCCAGTTCCGGCTTGG Vg2-F- RT GCAGCCTTGACGAGCGCAGT Vg3-R- RT CGGTGCTGTGAGCTAAGGCGG Vg3-F- RT CGGCCCGGCCCTTGTTTCAA VgR-R- RT TGTTCCAATGCACCAGCGGCA VgR-F- RT GTCGCTTCCGTCAGCGCAGT 按如下组分配置反应液:cDNA template 2 µL;SYBR® Premix Ex Taq ™ II 12.5 µL;PCR Forward Primer(10 µmol·L−1)1 µL;PCR Reverse Primer(10 µmol·L−1)1 µL;Nuclease-free Water 8.5 µL。整个过程保持在冰上进行(通常模板量在100 ng以下,引物终浓度为0.4 µmol·L−1时结果通常较好),轻轻混匀,避免产生气泡。采用两步法PCR程序进行实时定量PCR反应,反应体系如下:95 ℃ 30 s,95 ℃ 5 s,60 ℃ 30 s,40个循环。
为了消除个体差异,每个试验组的样品为3个同一组织RNA反转录的cDNA等量混合,作为一个样品池进行检测。每个样品3次重复,其表达水平分析选用18S rRNA的表达量进行均一化处理。反应结束后根据Real Time PCR的扩增曲线和溶解曲线判断引物质量。数据分析参照2−ΔΔCT法进行[26]。数据间的差异显著性分析通过T. Test进行,通过计算均值与数据间的标准偏差(SD)得到相应结果。
2. 结果与分析
2.1 Vg基因全长序列CDS的获得及分析
通过筛选荔枝蝽的转录组数据(数据未发表)获得3个Vg序列和1个VgRs序列,其mRNA分别为Vg1
5 764 bp,Vg2 6 216 bp,Vg3 6 278 bp 和VgRs 3 239 bp,将其分别命名为T. papi_Vg1 ,T. papi_Vg2 ,T. papi_Vg3,T. papi_VgRs,将获得的序列进行PCR扩增,随后测序验证,最终将获得的序列进行ORF预测,蛋白二级结构分析,信号肽,等电点等分析,结果如表4所示。 表 4 荔枝蝽Vg和VgRs序列分析Table 4. Sequencing of T. papillosa Vg and VgRs名称
Name序列长度
Sequence
length/bpORF长度
ORF
length/bp编码氨基酸起始位点
Coded amino
acid start site/bp编码氨基酸长度
Coded amino
acid length/bp信号肽长度
Signal peptide
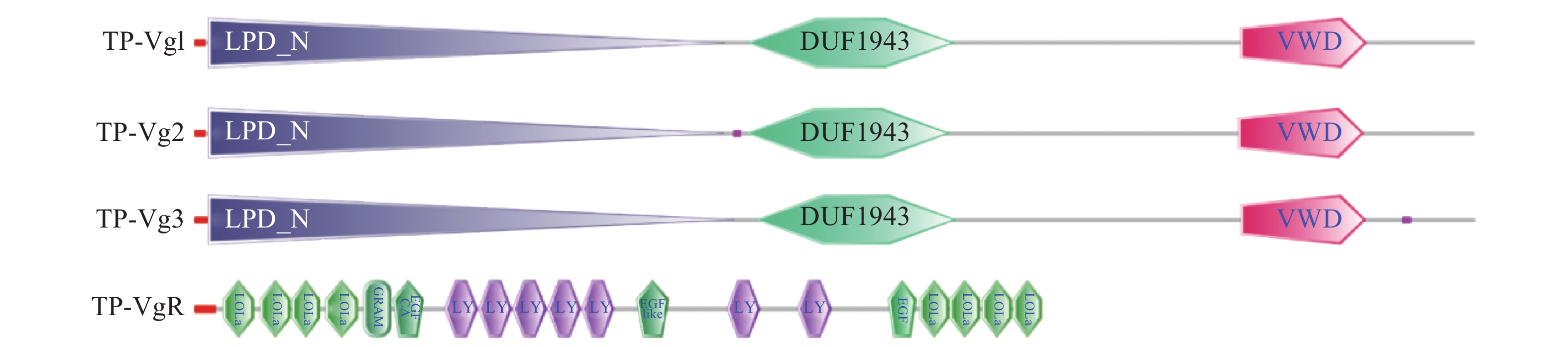
length/个Sec/SPI pI/Mw T. papi_Vg1 5 764 5 541 118-5 658 1 846 11 0.9868 6.53 / 209748.39 T. papi_Vg2 6 216 5 514 6 200-687 1 837 18 0.9214 6.28/209455.11 T. papi_Vg3 6 278 5 577 6 263-687 1 858 21 0.9721 7.89/208177.72 T. papi_VgRs 3 239 3 207 32-3 238 1 068 29 0.9033 4.96/119486.53 随后,用SMART软件分析了4个基因的蛋白结构域,结果显示,荔枝蝽3个Vg蛋白包含了卵黄原蛋白的3个典型结构域,一个完整的Vitellogenin_N Supperfamliy domain,一个DVF1943结构域和一个VWD结构域,所不同的是,Vg2在DUF1943结构域前面,包含一个low complexity(774-785)结构域,而Vg3在VWD结构域之后,包含一个low complexity(1752-1756)结构域,卵黄原受体蛋白包含了8个LDLRA,3个EGF,7个LY和1个GRAM结构域(图1)。
![]() 图 2 荔枝蝽3个卵黄原蛋白的氨基酸序列一致性分析注:红色方框标记为信号肽序列,紫色横线为LPD_N结构域,绿色横向标记为DUF1943结构域,粉色横线为VWD结构域,红色横线标记为low complexity结构域。Figure 2. Homology of amino acid sequences of 3 T. papillosa vitellogenin genesNote: Red box contains signal peptide sequence; purple line indicates LPD_N domain; green line indicates DUF1943 domain; pink line indicates VWD domain; and red line indicates low complexity domain.
图 2 荔枝蝽3个卵黄原蛋白的氨基酸序列一致性分析注:红色方框标记为信号肽序列,紫色横线为LPD_N结构域,绿色横向标记为DUF1943结构域,粉色横线为VWD结构域,红色横线标记为low complexity结构域。Figure 2. Homology of amino acid sequences of 3 T. papillosa vitellogenin genesNote: Red box contains signal peptide sequence; purple line indicates LPD_N domain; green line indicates DUF1943 domain; pink line indicates VWD domain; and red line indicates low complexity domain.![]() 图 1 荔枝蝽3个卵黄原蛋白及1个卵黄原受体蛋白的结构域注:3个卵黄原蛋白典型的卵黄原蛋白的结构域[LPD_N(紫色),DUF1943(绿色)和VWD结构域(红色)];Vg2在DUF1943结构域前面,包含一个low complexity(774-785)结构域(粉红色);Vg3在VWD结构域之后,包含一个low complexity(1752-1756)结构域(粉红色);卵黄原受体蛋白包含了8个LDLR,3个EGF,7个LY和1个GRAM结构域。Figure 1. Schematic diagram of the structural domains of three vitellogenin and one vitellogenin receptor protein in T. papillosaNote: Three typical vitellogenin domains [LPD_N (purple), DUF1943 (green) and VWD domain (red)]. Vg2 has one low complexity (774-785) domain (pink) before DUF1943 domain, while Vg3 contains a low complexity (1752-1756) domain (pink)after the VWD domain, and vitellogenin receptor protein contains 8 LDLRs, 3 EGFs, and 7 LY and 1 GRAM domain.
图 1 荔枝蝽3个卵黄原蛋白及1个卵黄原受体蛋白的结构域注:3个卵黄原蛋白典型的卵黄原蛋白的结构域[LPD_N(紫色),DUF1943(绿色)和VWD结构域(红色)];Vg2在DUF1943结构域前面,包含一个low complexity(774-785)结构域(粉红色);Vg3在VWD结构域之后,包含一个low complexity(1752-1756)结构域(粉红色);卵黄原受体蛋白包含了8个LDLR,3个EGF,7个LY和1个GRAM结构域。Figure 1. Schematic diagram of the structural domains of three vitellogenin and one vitellogenin receptor protein in T. papillosaNote: Three typical vitellogenin domains [LPD_N (purple), DUF1943 (green) and VWD domain (red)]. Vg2 has one low complexity (774-785) domain (pink) before DUF1943 domain, while Vg3 contains a low complexity (1752-1756) domain (pink)after the VWD domain, and vitellogenin receptor protein contains 8 LDLRs, 3 EGFs, and 7 LY and 1 GRAM domain.2.2 序列一致性及进化分析
用Clustal X v2.1软件对荔枝蝽3个卵黄原蛋白的氨基酸序列进行同源比对分析(图2),结果显示3个卵黄原蛋白之间序列一致性为59.73%,其中T. papi_Vg1与T. papi_Vg2的序列一致性为50%,T. papi_Vg1与T. papi_Vg3的序列一致性为42%,T. papi_Vg2与T. papi_Vg3的序列一致性为45%。
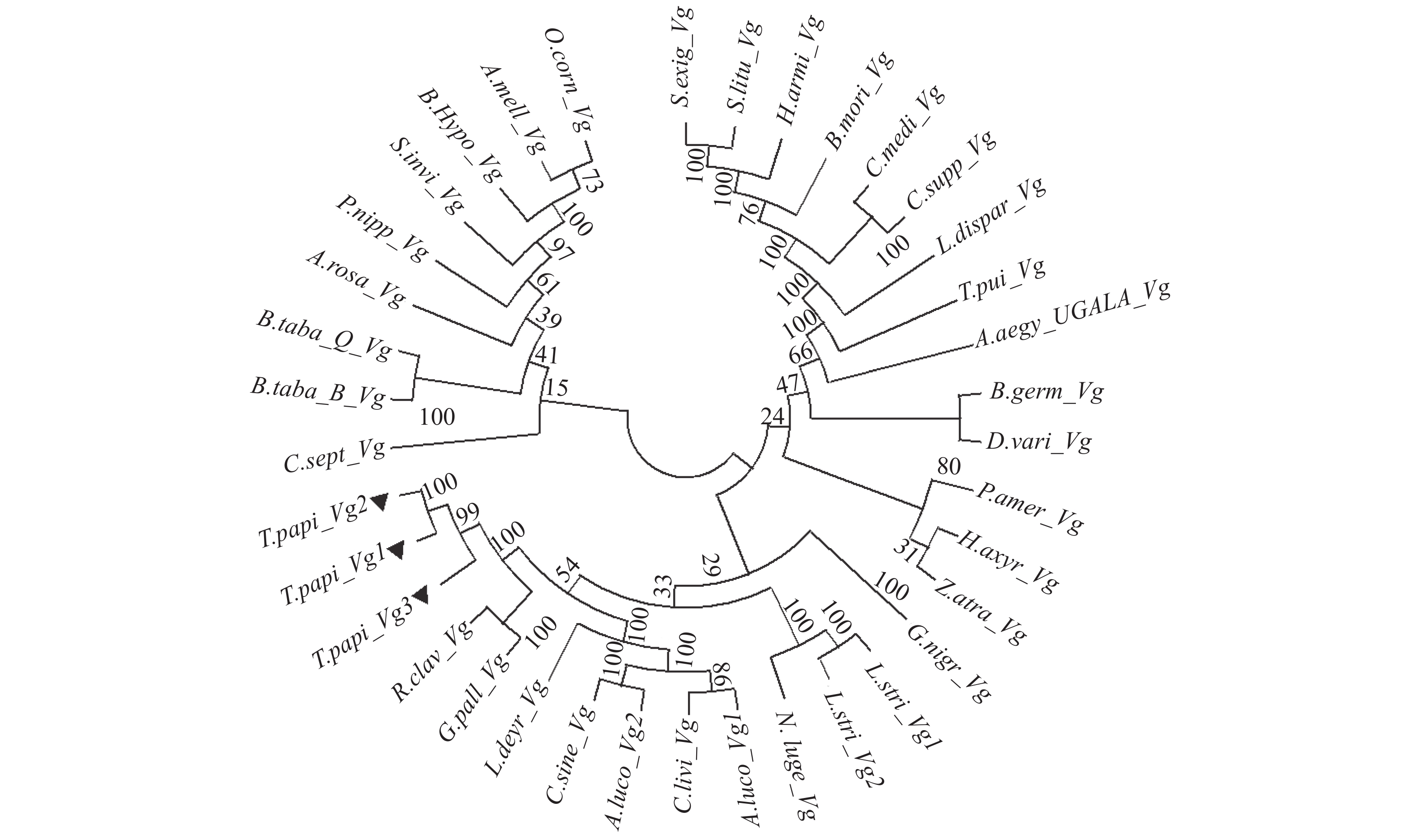
随后,利用34个其他物种昆虫Vg蛋白和28个其他物种昆虫的VgRs蛋白分别进行进化树分析(表5、6),利用MEGA X软件,建立NJ树(Bootstrap值1000)(图3),结果显示,在所获得的具有全长的37个Vg蛋白中序列之中,卵黄原蛋白分成3个大群,其中荔枝蝽的3个卵黄原蛋白与蝽科的豆类点蜂缘蝽Riptortus pedestris和大眼长蝽Geocoris pallidipennis聚集在了一支上,其次是负蝽科的大田负蝽Lethocerus deyrolli,盲蝽科的绿盲蝽Lygus lucorum和黑肩绿盲蝽Cyrtorhinus lividipennis聚集在一起。还发现,鳞翅目的荔枝蒂蛀虫Conopomorpha sinensis与绿盲蝽Lygus lucorum的A.luco_Vg2蛋白很好地聚集在一起,随后与其他半翅目昆虫灰飞虱Laodelphax striatellus、褐飞虱Nilaparvata lugens和油蝉Graptopsaltria nigrofuscata聚集形成了一个大群。说明宿主可能会改变昆虫的一些基因序列,从而产生进化中的相似性。其次,鳞翅目昆虫除了荔枝蒂蛀虫Conopomorpha sinensis之外的其他昆虫聚集形成一个大群,膜翅目昆虫和半翅目的烟粉虱Bemisia tabaci以及脉翅目的大草蛉Chrysopa septempunctata聚集形成一个大群。
表 5 用于进化树分析的Vg基因序列Table 5. Vg sequences for phylogenetic tree analysis序号
Serial number缩写
Abbreviations物种名称
Species name分类地位
Classification status学名
Latin name基因ID
Genebank NO.序列长度
Sequence length/bp1 A.aegy_UGALA_Vg 埃及伊蚊 双翅目,蚊科 Aedes aegypti AAU02548 6 504 2 A.luco_Vg1 绿盲蝽 半翅目,盲蝽科 Apolygus lucorum JQ867181 6 122 3 A.luco_Vg2 绿盲蝽 半翅目,盲蝽科 Apolygus lucorum KC136271 6 097 4 A.mell_Vg 意大利蜜蜂 膜翅目,蜜蜂科 Apis mellifera NM_001011578 5 441 5 A.rosa_Vg 黄翅菜叶蜂 膜翅目,叶蜂科 Athalia rosae AB007850 5 783 6 B.germ_Vg 德国小蠊 蜚蠊目,蜚蠊科 Blattella germanica AJ005115 5 749 7 B.Hypo_Vg 小峰熊蜂 膜翅目,蜜蜂科 Bombus hypocrita GQ340749 5 478 8 B.mori_Vg 家蚕 鳞翅目,蚕蛾科 Bombyx mori NM_001043844 5 734 9 B.taba_Q_Vg Q型烟粉虱 半翅目,粉虱科 Bemisia tabaci biotype Q GU332722 6 552 10 B.taba_B_Vg B型烟粉虱 半翅目,粉虱科 Bemisia tabaci biotype B GU332720 6 474 11 C.livi_Vg 黑肩绿盲蝽 半翅目,盲蝽科 Cyrtorhinus lividipennis KJ652904 5 912 12 C.medi_Vg 稻纵卷叶螟 鳞翅目,螟蛾科 Cnaphalocrocis medinalis JN408698 5 779 13 C.sept_Vg 大草蛉 脉翅目,草蛉科 Chrysopa septempunctata JX286617 5 664 14 C.sine_Vg 荔枝蒂蛀虫 鳞翅目,细蛾科 Conopomorpha sinensis MH553377 5 430 15 C.supp_Vg 二化螟 鳞翅目,草螟蛾科 Chilo suppressalis KT724958 5 373 16 D.vari_Vg 变异革蜱 寄螨目,硬蜱科 Dermacentor variabilis AY885250 5 744 17 G.nigr_Vg 油蝉 半翅目,蝉科 Graptopsaltria nigrofuscata AB026848 6 205 18 G.pall_Vg 大眼长蝽 半翅目,长蝽科 Geocoris pallidipennis KP688587 5 667 19 H.armi_Vg 棉铃虫 鳞翅目,夜蛾科 Helicoverpa armigera JX504706 5 271 20 H.axyr_Vg 异色瓢虫 鞘翅目,瓢甲科 Harmonia axyridis KX442718 5 403 21 L.deyr_Vg 大田负蝽 半翅目,土蝽科 Lethocerus deyrollei AB425334 5 865 22 L.disp_Vg 舞毒蛾 鳞翅目,毒蛾科 Lymantria dispar U60186 5 579 23 L.stri_Vg1 灰飞虱 半翅目,飞虱科 Laodelphax striatella KC469580 6 415 24 L.stri_Vg2 灰飞虱 半翅目,飞虱科 Laodelphax striatella KC469581 6 265 25 N. luge_Vg 褐飞虱 半翅目,飞虱科 Nilaparvata lugens AB353856 6 314 26 O.corn_Vg 角额壁蜂 膜翅目,切叶蜂科 Osmia cornifrons KM387561 5 477 27 P.amer_Vg 美洲蟑螂 蜚蠊目,蜚蠊科 Periplaneta americana AB034804 5 854 28 P.nipp_Vg 日本黑瘤姬蜂 膜翅目,姬蜂科 Pimpla nipponica AF026789 5 604 29 R.clav_Vg 豆类点蜂缘蝽 半翅目,缘蝽科 Riptortus clavatus RCU97277 5 736 30 S.exig_Vg 甜菜夜蛾 鳞翅目,夜蛾科 Spodoptera exigua KT599434 5 286 31 S.invi_Vg 红火蚁 膜翅目,蚁科 Solenopsis invicta AF512520 5 638 32 S.litu_Vg 斜纹夜蛾 鳞翅目,夜蛾科 Spodoptera litura EU095334 5 247 33 T.pui_Vg 蒲氏钩蝠蛾 鳞翅目,蝙蝠蛾科 Thitarodes pui MF622538 5 566 34 Z.atra_Vg 大麦虫 鞘翅目,拟步甲科 Zophobas atratus MK890211 5 457 表 6 用于进化树分析的VgRs基因序列Table 6. VgRs sequences for phylogenetic tree analysis序号
Serial number缩写
Abbreviations物种名称
Species name分类地位
Classification status学名
Latin name基因ID
Genebank NO.序列长度
Sequence length/bp1 S.invi_VgR 红火蚁 膜翅目,蚁科 Solenopsis invicta NM_001304596.1 5 764 2 B.mori_VgR 家蚕 鳞翅目,蚕蛾科 Bombyx mori NM_001197251.1 5 746 3 A.aegy_VgR 埃及伊蚊 双翅目,蚊科 Aedes aegypti L77800.1 5 544 4 P.amer_VgR 美洲大蠊 蜚蠊目,蜚蠊科 Periplaneta americana AB077047.2 5 722 5 B.germ_VgR 德国小蠊 蜚蠊目,蜚蠊科 Blattella germanica AM050637.1 5 768 6 T.cinn_VgR 棉花红蜘蛛 蜱螨目,叶螨科 Tetranychus cinnabarinus KR090060.1 5 559 7 B.dors_VgR 桔小实蝇 双翅目,实蝇科 Bactrocera dorsalis JX469118.1 6 595 8 D.mela_VgR 黑腹果蝇 双翅目,果蝇科 Drosophila melanogaster U13637.1 6 254 9 S.invi_VgR 红火蚁 膜翅目,蚁科 Solenopsis invicta AY262832.1 5 764 10 L.ento_VgR 嗜虫书虱 啮虫目,虱啮科 Liposcelis entomophila MN398904.1 5 916 11 S.furc_VgR 白背飞虱 半翅目,飞虱科 Sogatella furcifera MN327568.1 5 796 12 B.lant_VgR 兰州熊蜂 膜翅目,蜜蜂科 Bombus lantschouensis MN217253.1 5 519 13 C.cupp_VgR 二化螟 鳞翅目,草螟蛾科 Chilo suppressalis MN227162.1 5 484 14 C.sine_VgR 荔枝蒂蛀虫 鳞翅目,细蛾科 Conopomorpha sinensis KX987145.1 5 424 15 L.stri_VgR 灰飞虱 半翅目,飞虱科 Laodelphax striatella MH347273.1 6 065 16 C.bowr_VgR 大猿叶虫 鞘翅目,叶甲科 Colaphellus bowringi MH104867.1 5 774 17 B.taba_VgR 烟粉虱 半翅目,粉虱科 Bemisia tabaci complex sp. Asia KR818562.2 5 430 18 S.litu_VgR 斜纹夜蛾 鳞翅目,夜蛾科 Spodoptera litura GU983858.1 5 370 19 P.citr_VgR 柑橘全爪螨 蜱螨目,叶螨科 Panonychus citri KC978894.1 5 676 20 H.armi_VgR 棉铃虫 鳞翅目,夜蛾科 Helicoverpa armigera KC181922.2 5 891 21 A.pern_VgR 姬透目天蚕蛾 鳞翅目,天蚕蛾科 Antheraea pernyi JN003583.1 5 847 22 N.luge_VgR 褐飞虱 半翅目,飞虱科 Nilaparvata lugens GU723297.1 6 174 23 C.ital_VgR 意大利蝗 直翅目,蝗科 Calliptamus italicus MK358118.1 5 589 24 S.exig_VgR 甜菜夜蛾 鳞翅目,夜蛾科 Spodoptera exigua KT899978.1 5 445 25 O.furn_VgR 亚洲玉米螟 鳞翅目,螟蛾科 Ostrinia furnacalis MN058042.1 6 289 26 P.xylo_VgR 小菜蛾 鳞翅目,菜蛾科 Plutella xylostella MN044389.1 5 418 27 M.vitr_VgR 豆野螟 鳞翅目,螟蛾科 Maruca vitrata MG799569.1 5 397 28 D.virg_VgR 玉米根萤叶甲 鞘翅目,叶甲科 Diabrotica virgifera KY373243.1 5 612 ![]() 图 3 部分昆虫Vg蛋白进化树注:构建系统发育树所用到的基因信息见表3,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角形标记为荔枝蝽3个Vg基因。Figure 3. Phylogenetic tree of partial T. papillosa VgNote: Genes used to construct phylogenetic tree are shown in Table 3; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and 3 T. papillosa Vg are marked by black triangles.
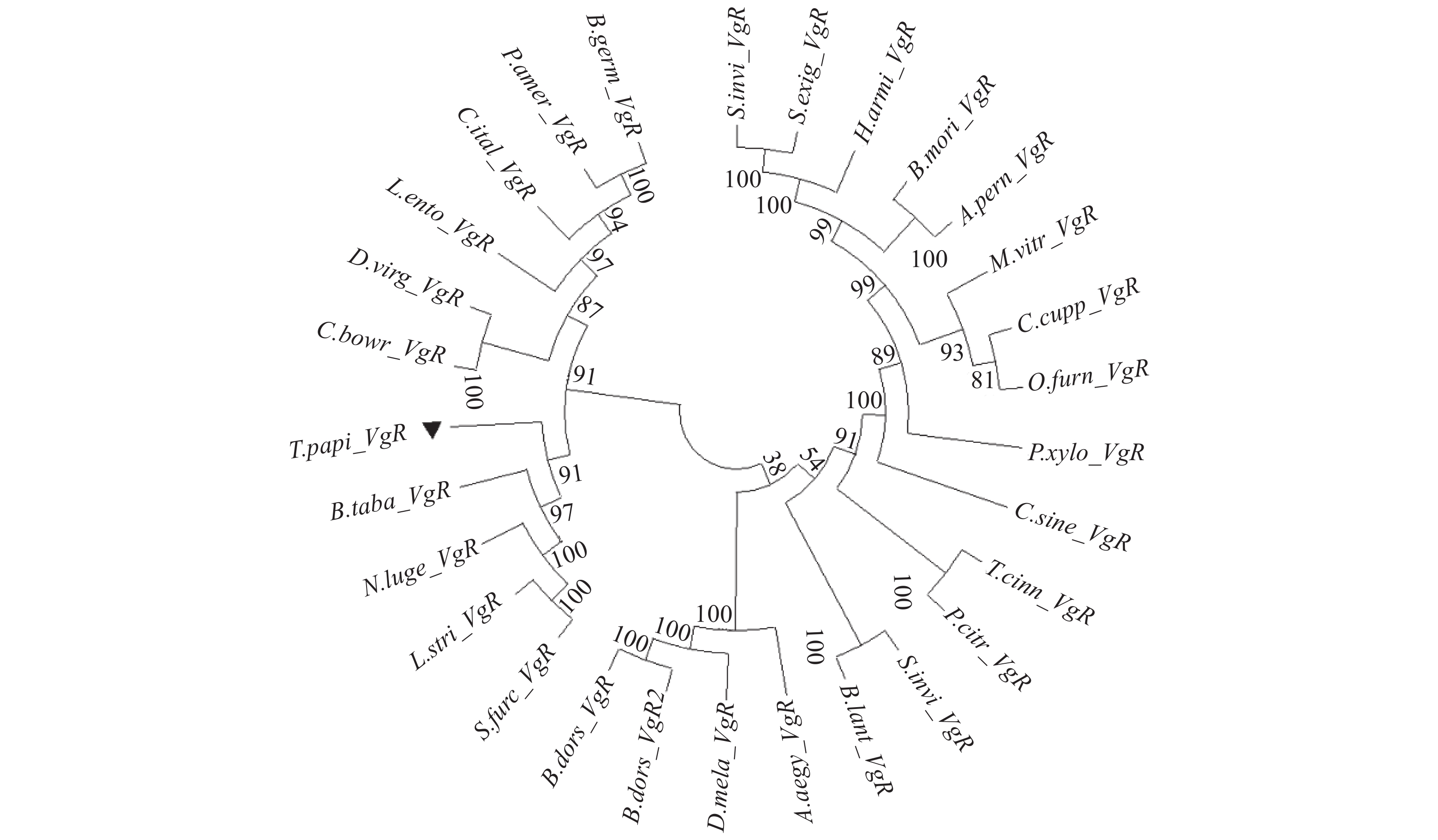
图 3 部分昆虫Vg蛋白进化树注:构建系统发育树所用到的基因信息见表3,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角形标记为荔枝蝽3个Vg基因。Figure 3. Phylogenetic tree of partial T. papillosa VgNote: Genes used to construct phylogenetic tree are shown in Table 3; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and 3 T. papillosa Vg are marked by black triangles.同样,对T. papi_VgRs的进化树分析(图4)结果显示,29个VgRs分别聚集,主要分为两大类,鳞翅目与双翅目昆虫聚集为一个大类,而荔枝蝽与半翅目其他昆虫烟粉虱B. tabaci、灰飞虱L. striatellus、褐飞虱N. lugens和白背飞虱Sogatella furcifera聚集在一起,随后与鞘翅目、蜚蠊目和啮虫目昆虫聚集形成一个大群,同目昆虫的VgRs进化关系更为接近,E值绝大多数都在50以上,说明VgRs与物种进化一致。
![]() 图 4 部分昆虫VgRs蛋白进化树注:构建系统发育树所用到的基因信息见表4,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角型标记为荔枝蝽VgRs基因。Figure 4. Phylogenetic tree of partial T. papillosa VgRsNote: Genes used to construct phylogenetic tree are shown in Table 4; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and T. papillosa VgRs is marked by black triangle.
图 4 部分昆虫VgRs蛋白进化树注:构建系统发育树所用到的基因信息见表4,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角型标记为荔枝蝽VgRs基因。Figure 4. Phylogenetic tree of partial T. papillosa VgRsNote: Genes used to construct phylogenetic tree are shown in Table 4; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and T. papillosa VgRs is marked by black triangle.2.3 荔枝蝽Vg及VgRs基因的时空表达分析
用实时荧光定量PCR(qRT-PCR)检测荔枝蝽14个不同发育阶段的不同组织中的Vg基因和VgRs基因的表达情况(图5、6),结果表明,Vg1
基因在各个组织中表达量相对比较高,尤其是在雄成虫淋巴液、雌虫、雌虫脂肪体、雌虫中肠和卵巢中,而Vg2和Vg3基因仅在雌虫脂肪体中较高表达。VgRs的表达量,与Vg的表达部位基本一致,在雌虫卵巢中,表达量最高,其次是雌虫,雄虫淋巴液和若虫的脂肪体当中,在若虫触角,雄虫触角和雄虫精巢中,也有少量表达。 ![]() 图 5 荔枝蝽卵黄原蛋白基因在不同组织、不同发育时期中的表达分析注:a、c、e分别为Vg1、Vg2、Vg3基因在不同发育时期表达量分析,不同发育时期以若虫为基础进行比较。b、d、f分别为Vg1、Vg2、Vg3基因在不同组织表达量分析,不同组织以若虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。Figure 5. Expressions of vitellogenin genes of T. papillosa in tissues at developmental stagesNote: a, c, and e are expression levels of Vg1, Vg2, and Vg3, respectively, at different developmental stages, and the comparison is based on nymph in different development stages. b, d, and f respectively show the expression levels of Vg1 , Vg2 , and Vg3 genes in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different determined by multiple comparison by LSD method at P<0.05.
图 5 荔枝蝽卵黄原蛋白基因在不同组织、不同发育时期中的表达分析注:a、c、e分别为Vg1、Vg2、Vg3基因在不同发育时期表达量分析,不同发育时期以若虫为基础进行比较。b、d、f分别为Vg1、Vg2、Vg3基因在不同组织表达量分析,不同组织以若虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。Figure 5. Expressions of vitellogenin genes of T. papillosa in tissues at developmental stagesNote: a, c, and e are expression levels of Vg1, Vg2, and Vg3, respectively, at different developmental stages, and the comparison is based on nymph in different development stages. b, d, and f respectively show the expression levels of Vg1 , Vg2 , and Vg3 genes in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different determined by multiple comparison by LSD method at P<0.05.![]() 图 6 荔枝蝽卵黄原蛋白受体基因在不同组织,不同发育时期中的表达分析注:a为VgR基因在不同发育时期表达量分析,不同发育时期以幼虫为基础进行比较。b为VgR基因在不同组织表达量分析,不同组织是以幼虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。Figure 6. Expressions of vitellogenin receptor gene of T. papillosa in tissues at developmental stagesNote: a is VgR expressions at different developmental stages, and the comparison is based on nymph in different development stages.b is VgR expressions in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different as determined by multiple comparison by LSD method at P<0.05.
图 6 荔枝蝽卵黄原蛋白受体基因在不同组织,不同发育时期中的表达分析注:a为VgR基因在不同发育时期表达量分析,不同发育时期以幼虫为基础进行比较。b为VgR基因在不同组织表达量分析,不同组织是以幼虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。Figure 6. Expressions of vitellogenin receptor gene of T. papillosa in tissues at developmental stagesNote: a is VgR expressions at different developmental stages, and the comparison is based on nymph in different development stages.b is VgR expressions in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different as determined by multiple comparison by LSD method at P<0.05.3. 讨论与结论
卵黄原蛋白基因是编码昆虫和许多其他卵生生物卵内的主要蛋白-卵黄蛋白前体。在昆虫中,Vg基因以性别、组织和阶段特异性的方式在脂肪体内和卵巢外表达。在生殖阶段,Vg蛋白mRNA大量表达,然后被翻译,分泌到血淋巴中,并最终通过受体介导的内吞作用被发育中的卵母细胞吸收。Vgs以卵黄蛋白(Vn)的形式储存,卵黄蛋白(Vn)是发育中的胚胎的主要营养储备[27]。
Vgs和VgRs已在许多脊椎动物和无脊椎动物中被广泛鉴定,并且昆虫的Vgs和VgRs得到了广泛的研究,在蜚蠊目、直翅目、鞘翅目、双翅目、鳞翅目、半翅目和膜翅目等昆虫中均有相关基因被报道。通常,昆虫Vg的氨基酸结构和组成高度保守[27]。它通常具有20个残基的信号肽,N端区域的脂质结合结构域(LPD_N),C端区域的von Willebrand因子D型结构域(VWD)[27],以及未知的功能域(DUF1943)。
本研究通过筛选荔枝蝽T. papillosa的转录组数据(数据另文发表),利用分子克隆的方法获得了荔枝蝽3个Vg基因和1个VgRs基因,在序列结构方面荔枝蝽与其他报道的昆虫Vgs相似,3个荔枝蝽Vg基因均含有20 bp左右的信号肽,并且均具有3个典型的Vg蛋白的功能结构域,高度保守的卵黄蛋白原结构域LPD_N和VWFD结构域[28]。以及目前仅在少数昆虫中(例如果斑螟Cadra cautella和白背飞虱S. furcifera等)被报道发现的未知功能的DUF1943结构域[29-32]。同时,3个荔枝蝽Vg蛋白序列也具有不同的特征,例如:Vg2在DUF1943结构域N端区域包含一个low complexity(774-785)结构域,而Vg3在VWD结构域之后,C端区域的包含一个low complexity(1752-1756)结构域。
对其他昆虫物种的研究结果显示,Vg蛋白的基因数量因昆虫而异[33]。例如,意大利蜜蜂A. mellifera[34]、佛罗里达弓背蚁Camponotus floridanus[35],家蚕B. mori[36]和德国小蠊B. germanica[37]仅有1个Vg基因,而美洲大蠊P. americana[38]带有2个Vg基因。最近的研究表明,褐飞虱N. lugens具有3个Vg基因[39]。目前,埃及伊蚊A. aegypti[40]和阿根廷蚁Linepithema humile[35, 41]中基因数最高的是5个。这些基因数差异被认为是基因复制事件的结果。本研究在荔枝蝽中发现的3个Vg基因,序列一致性为59.73%,T. papi_Vg1与其他物种的结构相似性最高,具有比价保守的3个功能结构域,与在NCBI数据库中获得的几种蝽科昆虫的序列一致性相对较高,而T. papi_Vg2与T. papi_Vg3中均在不同的位置中插入了一个low complexity结构域,LCRs功能域是常见的通过减数分裂形成的重组事件,这些区域的动态多样化和无中间的变异和多态性水平较高,被认为是物种间表型变异的重要来源[42],这一结构特征,可能说明T. papi_Vg2与T. papi_Vg3是在长期的进化过程中,由T. papi_Vg1基因复制及变异而来的,基因复制是基因组进化的重要机制,并且是基因表达模式和功能进化新颖的重要手段[43]。因此,这3个基因在具有类似的生理功能的同时,发生了什么样的改变,值得进一步探讨。
对荔枝蝽VgRs序列的分析表明,它由多个保守的模块化元件组成,与其他昆虫VgRs相似,并且是LDLR超家族的典型成员[17]。鳞翅目中的VgRs的特征是在两个LBD结构域中存在11个富含半胱氨酸的LDLRA重复,其中在第一和第二LBD结构域中分别为4个和7个重复。但是,LDLRA重复序列的数量和排列方式与其他昆虫顺序有很大不同。蜚蠊目和双翅目中有5和8个LDLRA重复序列,膜翅目中有2个、4个和8个重复序列,鞘翅目有8个重复序列[44-45]。与鳞翅目昆虫VgRs相比,荔枝蒂蛀虫C.sinensis在2个EGF前体结构域中的EGF /钙结合样重复序列的数量和排列都不同。通常,在第1个EGF前体结构域中出现了2个或3个类似EGF的重复序列,但在荔枝蒂蛀虫VgRs中多了1个额外的重复序列[46]。本研究在荔枝蝽中发现,T. papi_VgRs包含了8个LDLRA、3个EGF、7个LY和1个GRAM结构域,这与半翅目昆虫的结构域较为类似。
本研究获得的4个基因,均具有典型的保守结构域,是典型的昆虫Vg和VgRs基因,通过构建两个系统进化树,推断了3个荔枝蝽Vg基因和1个荔枝蝽VgRs基因与其他目昆虫Vgs和VgRs的进化关系。从进化关系来看,Vg和VgRs基因的分子进化与物种之间的进化关系较为匹配,不论是荔枝蝽Vg基因还是荔枝蝽VgRs基因均与半翅目昆虫较好地聚集在一起,从荔枝蝽Vg基因进化树来看,先后与蝽科、负蝽科、盲蝽科昆虫聚集在一个大支上,荔枝蝽VgRs基因进化树也很好地支持这一结果,这一结论也很好地说明荔枝蝽的Vg和VgRs基因具有较为保守的功能。
同时,发现荔枝蒂蛀虫C. sinensis的Vg2基因在分子进化水平上没有和鳞翅目其他昆虫显示出更为接近的关系,反而是聚集在与荔枝蝽更为接近的半翅目分支上,其与绿盲蝽的Vg2和荔枝蝽的T. papi_Vg2在进化关系上更为接近,但在VgRs基因支序图中并没有和半翅目在相近的分支,根据Vg基因的功能特征,推测其原因可能是在长期的进化过程中,由于昆虫长期取食专一性宿主,在遗传变异的过程中,对生殖相关的卵黄原蛋白造成了相应的结构变异造成的。VgRs基因由于具有极强的卵巢特异性,所以可能在昆虫生殖系统的进化中由于不同目昆虫生殖方式及转运物质的需求不同,从而产生了不同的基因结构变异。因此,这些基因可能的功能,还需要进一步的深入研究。
卵黄原蛋白的结构、合成、摄取过程与激素的调控激励是昆虫生理学研究的热点之一,昆虫卵黄原蛋白基因存在着明显的分子多态性,同一种昆虫也存在几个编码卵黄原蛋白的基因,因此,常常被作为分子进化研究的对象,同时,卵黄原蛋白作为昆虫体内的贮藏蛋白,为胚胎发育提供营养,这为害虫防治提供了新的思路,4种杀虫剂对荔枝蒂蛀虫C. sinensis产卵的亚致死作用的研究结果表明,在测试的各种杀虫剂中,对荔枝蒂蛀虫的毒性各不相同,毒死蜱的LC50为0.23 mg·kg−1、β-氯氰菊酯的为20.00 mg·kg−1、苯甲依氨菌素(EB)对产卵率,存活率和卵巢有明显的负影响,LC30剂量下荔枝蒂蛀虫C. sinensis的发育和交配率有显著的影响[46]。进一步的研究表明,在EB暴露后24、48和72 h,CsVg和CsVgR的转录水平受到不同程度的损害,这一结果与亚致死浓度EB-下荔枝蒂蛀虫的减少是一致的[46]。一些杀虫剂可以通过破坏昆虫的脂肪体,从而抑制Vg的合成,如印楝素处理可以导致溪岸蚰嫂Labidura riparis脂肪体细胞解体[47],硫丹处理也会破坏剑角蝗Poekilocerus pictus的脂肪体[48],同样,SfVg和SfVgR沉默抑制了白背飞虱S.furcifera的卵巢发育、产卵数和孵化率。噻虫嗪LC10显著抑制了SfVg-like和SfVgR的表达。相反,三唑磷LC25显著促进了白背飞虱S. furcifera中SfVg、SfVg-like和SfVgR的表达,并增加了卵黄蛋白原的含量。因此,杀虫剂可以通过改变SfVg和SfVgR的表达来调节白背飞虱的繁殖,从而影响白背飞虱S.furcifera的种群密度。这些发现有助于加深对杀虫剂对害虫繁殖和复发的影响的分子机制的理解奠定基础,可以说,昆虫的Vg基因,已成为潜在的害虫控制和鉴定的新靶点[49]。
Vg基因的调节在转录水平上直接受激素控制。参与Vg基因转录的激素是保幼激素(JH)、蜕皮类固醇和一些神经肽。总体上根据Vg基因转录的激素调节系统,可以将昆虫分为3类:(i)仅使用JH进行Vg基因转录的昆虫,如鞘翅目和不完全变态昆虫;(ii)同时需要JH和蜕皮类固醇来调节Vg的昆虫,如双翅目昆虫;(iii)需要JH、蜕皮类固醇和其他激素来调节其生殖生物学的昆虫,如鳞翅目昆虫。然而为什么昆虫物种在使用不同的激素来控制其生殖生理方面会发生分歧尚不清楚[25]。本研究获得了Vg和VgRs基因在荔枝蝽不同组织中的时空表达情况,均显示其在卵巢和雌虫脂肪体中的高效高表达的现象,这与其他的昆虫的表达模式类似,所不同的是,T. papi_Vg2和T. papi_Vg3在卵巢中并没有出现显著的高表达趋势,在雌虫脂肪体中,呈现特异的高表达特性。这从另一个角度说明,这两个基因在结构域产生变异之后,功能亦随之发生了变化,这些现象的发现,为更好地理解荔枝蝽T. papillosa的产卵繁殖行为提供了基因层面的理论基础,同时亦可为荔枝蝽防治的靶点筛选提供一些有益的思路。
-
图 2 荔枝蝽3个卵黄原蛋白的氨基酸序列一致性分析
注:红色方框标记为信号肽序列,紫色横线为LPD_N结构域,绿色横向标记为DUF1943结构域,粉色横线为VWD结构域,红色横线标记为low complexity结构域。
Figure 2. Homology of amino acid sequences of 3 T. papillosa vitellogenin genes
Note: Red box contains signal peptide sequence; purple line indicates LPD_N domain; green line indicates DUF1943 domain; pink line indicates VWD domain; and red line indicates low complexity domain.
图 1 荔枝蝽3个卵黄原蛋白及1个卵黄原受体蛋白的结构域
注:3个卵黄原蛋白典型的卵黄原蛋白的结构域[LPD_N(紫色),DUF1943(绿色)和VWD结构域(红色)];Vg2在DUF1943结构域前面,包含一个low complexity(774-785)结构域(粉红色);Vg3在VWD结构域之后,包含一个low complexity(1752-1756)结构域(粉红色);卵黄原受体蛋白包含了8个LDLR,3个EGF,7个LY和1个GRAM结构域。
Figure 1. Schematic diagram of the structural domains of three vitellogenin and one vitellogenin receptor protein in T. papillosa
Note: Three typical vitellogenin domains [LPD_N (purple), DUF1943 (green) and VWD domain (red)]. Vg2 has one low complexity (774-785) domain (pink) before DUF1943 domain, while Vg3 contains a low complexity (1752-1756) domain (pink)after the VWD domain, and vitellogenin receptor protein contains 8 LDLRs, 3 EGFs, and 7 LY and 1 GRAM domain.
图 3 部分昆虫Vg蛋白进化树
注:构建系统发育树所用到的基因信息见表3,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角形标记为荔枝蝽3个Vg基因。
Figure 3. Phylogenetic tree of partial T. papillosa Vg
Note: Genes used to construct phylogenetic tree are shown in Table 3; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and 3 T. papillosa Vg are marked by black triangles.
图 4 部分昆虫VgRs蛋白进化树
注:构建系统发育树所用到的基因信息见表4,利用MEGA X构建NJ树(Bootstrap值1000),黑色三角型标记为荔枝蝽VgRs基因。
Figure 4. Phylogenetic tree of partial T. papillosa VgRs
Note: Genes used to construct phylogenetic tree are shown in Table 4; MEGA X used to construct NJ tree had a Bootstrap value of 1 000; and T. papillosa VgRs is marked by black triangle.
图 5 荔枝蝽卵黄原蛋白基因在不同组织、不同发育时期中的表达分析
注:a、c、e分别为Vg1、Vg2、Vg3基因在不同发育时期表达量分析,不同发育时期以若虫为基础进行比较。b、d、f分别为Vg1、Vg2、Vg3基因在不同组织表达量分析,不同组织以若虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。
Figure 5. Expressions of vitellogenin genes of T. papillosa in tissues at developmental stages
Note: a, c, and e are expression levels of Vg1, Vg2, and Vg3, respectively, at different developmental stages, and the comparison is based on nymph in different development stages. b, d, and f respectively show the expression levels of Vg1 , Vg2 , and Vg3 genes in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different determined by multiple comparison by LSD method at P<0.05.
图 6 荔枝蝽卵黄原蛋白受体基因在不同组织,不同发育时期中的表达分析
注:a为VgR基因在不同发育时期表达量分析,不同发育时期以幼虫为基础进行比较。b为VgR基因在不同组织表达量分析,不同组织是以幼虫触角为基础进行比较。组织部位标注见表1, 18S rRNA基因作为内参基因,图中数据为平均值±标准误,相对表达量差异显著(LSD法多重比对,P<0.05)。
Figure 6. Expressions of vitellogenin receptor gene of T. papillosa in tissues at developmental stages
Note: a is VgR expressions at different developmental stages, and the comparison is based on nymph in different development stages.b is VgR expressions in different tissues, and the different tissues are compared on the basis of nymph antennae. Tissues abbreviations are shown in Table 1; 18S rRNA gene is internal reference gene used; data are mean±standard error; and relative expression is significantly different as determined by multiple comparison by LSD method at P<0.05.
表 1 供试荔枝蝽组织
Table 1 Tissues of T. papillosa under study
组织 Tissue 名称 Name 雌虫 Female insect TP_M 雌虫卵巢 Female ovary TP_MO 雌虫中肠 Female midgut TP_MM 雌虫脂肪体 Female fat body TP_MF 雄虫 Male insect TP_FM 雄虫触角 Male antenna TP_FMA 雄虫精巢 Male testis TP_FMT 雄虫中肠 Male midgut TP_FMM 雄虫脂肪体 Male fat body TP_FMF 雄虫淋巴液 Male lymph TP_FMH 若虫触角 Nymph antennae TP_AA 若虫中肠 Nymph midgut TP_AM 若虫脂肪体 Nymph fat body TP_AF 若虫 Nymph TP_A 表 2 PCR扩增引物序列
Table 2 PCR primer sequences
引物名 Primer name 序列 Sequence Vg1-R-all ATGGCGTGGAGTACAGCCCTTCTC Vg1-F-all TCAGCTTGAAATACAGGCCTCTGG Vg2-R-all CATGTGCTGGTCAAGAACACTT Vg2-F-all TTACAAACTGGAAACACA Vg3-R-all ATGTGGACACAAATTTCACTG Vg3-F-all TTACAAACTGGAAACACATT VgR-R-all AGGCACCAAAGGCTTCCAGTTCG VgR-F-all TTACTCTCATCACTCCCATCACGG 表 3 PCR扩增引物序列
Table 3 qRT-PCR primer sequences
引物名 Primer name 序列 Sequence Vg1-R-RT TTTCGCCGCATCCTACGCCG Vg1-F- RT ACAGGACCTGCCGCCATCCT Vg2-R- RT CTGGGCCAGTTCCGGCTTGG Vg2-F- RT GCAGCCTTGACGAGCGCAGT Vg3-R- RT CGGTGCTGTGAGCTAAGGCGG Vg3-F- RT CGGCCCGGCCCTTGTTTCAA VgR-R- RT TGTTCCAATGCACCAGCGGCA VgR-F- RT GTCGCTTCCGTCAGCGCAGT 表 4 荔枝蝽Vg和VgRs序列分析
Table 4 Sequencing of T. papillosa Vg and VgRs
名称
Name序列长度
Sequence
length/bpORF长度
ORF
length/bp编码氨基酸起始位点
Coded amino
acid start site/bp编码氨基酸长度
Coded amino
acid length/bp信号肽长度
Signal peptide
length/个Sec/SPI pI/Mw T. papi_Vg1 5 764 5 541 118-5 658 1 846 11 0.9868 6.53 / 209748.39 T. papi_Vg2 6 216 5 514 6 200-687 1 837 18 0.9214 6.28/209455.11 T. papi_Vg3 6 278 5 577 6 263-687 1 858 21 0.9721 7.89/208177.72 T. papi_VgRs 3 239 3 207 32-3 238 1 068 29 0.9033 4.96/119486.53 表 5 用于进化树分析的Vg基因序列
Table 5 Vg sequences for phylogenetic tree analysis
序号
Serial number缩写
Abbreviations物种名称
Species name分类地位
Classification status学名
Latin name基因ID
Genebank NO.序列长度
Sequence length/bp1 A.aegy_UGALA_Vg 埃及伊蚊 双翅目,蚊科 Aedes aegypti AAU02548 6 504 2 A.luco_Vg1 绿盲蝽 半翅目,盲蝽科 Apolygus lucorum JQ867181 6 122 3 A.luco_Vg2 绿盲蝽 半翅目,盲蝽科 Apolygus lucorum KC136271 6 097 4 A.mell_Vg 意大利蜜蜂 膜翅目,蜜蜂科 Apis mellifera NM_001011578 5 441 5 A.rosa_Vg 黄翅菜叶蜂 膜翅目,叶蜂科 Athalia rosae AB007850 5 783 6 B.germ_Vg 德国小蠊 蜚蠊目,蜚蠊科 Blattella germanica AJ005115 5 749 7 B.Hypo_Vg 小峰熊蜂 膜翅目,蜜蜂科 Bombus hypocrita GQ340749 5 478 8 B.mori_Vg 家蚕 鳞翅目,蚕蛾科 Bombyx mori NM_001043844 5 734 9 B.taba_Q_Vg Q型烟粉虱 半翅目,粉虱科 Bemisia tabaci biotype Q GU332722 6 552 10 B.taba_B_Vg B型烟粉虱 半翅目,粉虱科 Bemisia tabaci biotype B GU332720 6 474 11 C.livi_Vg 黑肩绿盲蝽 半翅目,盲蝽科 Cyrtorhinus lividipennis KJ652904 5 912 12 C.medi_Vg 稻纵卷叶螟 鳞翅目,螟蛾科 Cnaphalocrocis medinalis JN408698 5 779 13 C.sept_Vg 大草蛉 脉翅目,草蛉科 Chrysopa septempunctata JX286617 5 664 14 C.sine_Vg 荔枝蒂蛀虫 鳞翅目,细蛾科 Conopomorpha sinensis MH553377 5 430 15 C.supp_Vg 二化螟 鳞翅目,草螟蛾科 Chilo suppressalis KT724958 5 373 16 D.vari_Vg 变异革蜱 寄螨目,硬蜱科 Dermacentor variabilis AY885250 5 744 17 G.nigr_Vg 油蝉 半翅目,蝉科 Graptopsaltria nigrofuscata AB026848 6 205 18 G.pall_Vg 大眼长蝽 半翅目,长蝽科 Geocoris pallidipennis KP688587 5 667 19 H.armi_Vg 棉铃虫 鳞翅目,夜蛾科 Helicoverpa armigera JX504706 5 271 20 H.axyr_Vg 异色瓢虫 鞘翅目,瓢甲科 Harmonia axyridis KX442718 5 403 21 L.deyr_Vg 大田负蝽 半翅目,土蝽科 Lethocerus deyrollei AB425334 5 865 22 L.disp_Vg 舞毒蛾 鳞翅目,毒蛾科 Lymantria dispar U60186 5 579 23 L.stri_Vg1 灰飞虱 半翅目,飞虱科 Laodelphax striatella KC469580 6 415 24 L.stri_Vg2 灰飞虱 半翅目,飞虱科 Laodelphax striatella KC469581 6 265 25 N. luge_Vg 褐飞虱 半翅目,飞虱科 Nilaparvata lugens AB353856 6 314 26 O.corn_Vg 角额壁蜂 膜翅目,切叶蜂科 Osmia cornifrons KM387561 5 477 27 P.amer_Vg 美洲蟑螂 蜚蠊目,蜚蠊科 Periplaneta americana AB034804 5 854 28 P.nipp_Vg 日本黑瘤姬蜂 膜翅目,姬蜂科 Pimpla nipponica AF026789 5 604 29 R.clav_Vg 豆类点蜂缘蝽 半翅目,缘蝽科 Riptortus clavatus RCU97277 5 736 30 S.exig_Vg 甜菜夜蛾 鳞翅目,夜蛾科 Spodoptera exigua KT599434 5 286 31 S.invi_Vg 红火蚁 膜翅目,蚁科 Solenopsis invicta AF512520 5 638 32 S.litu_Vg 斜纹夜蛾 鳞翅目,夜蛾科 Spodoptera litura EU095334 5 247 33 T.pui_Vg 蒲氏钩蝠蛾 鳞翅目,蝙蝠蛾科 Thitarodes pui MF622538 5 566 34 Z.atra_Vg 大麦虫 鞘翅目,拟步甲科 Zophobas atratus MK890211 5 457 表 6 用于进化树分析的VgRs基因序列
Table 6 VgRs sequences for phylogenetic tree analysis
序号
Serial number缩写
Abbreviations物种名称
Species name分类地位
Classification status学名
Latin name基因ID
Genebank NO.序列长度
Sequence length/bp1 S.invi_VgR 红火蚁 膜翅目,蚁科 Solenopsis invicta NM_001304596.1 5 764 2 B.mori_VgR 家蚕 鳞翅目,蚕蛾科 Bombyx mori NM_001197251.1 5 746 3 A.aegy_VgR 埃及伊蚊 双翅目,蚊科 Aedes aegypti L77800.1 5 544 4 P.amer_VgR 美洲大蠊 蜚蠊目,蜚蠊科 Periplaneta americana AB077047.2 5 722 5 B.germ_VgR 德国小蠊 蜚蠊目,蜚蠊科 Blattella germanica AM050637.1 5 768 6 T.cinn_VgR 棉花红蜘蛛 蜱螨目,叶螨科 Tetranychus cinnabarinus KR090060.1 5 559 7 B.dors_VgR 桔小实蝇 双翅目,实蝇科 Bactrocera dorsalis JX469118.1 6 595 8 D.mela_VgR 黑腹果蝇 双翅目,果蝇科 Drosophila melanogaster U13637.1 6 254 9 S.invi_VgR 红火蚁 膜翅目,蚁科 Solenopsis invicta AY262832.1 5 764 10 L.ento_VgR 嗜虫书虱 啮虫目,虱啮科 Liposcelis entomophila MN398904.1 5 916 11 S.furc_VgR 白背飞虱 半翅目,飞虱科 Sogatella furcifera MN327568.1 5 796 12 B.lant_VgR 兰州熊蜂 膜翅目,蜜蜂科 Bombus lantschouensis MN217253.1 5 519 13 C.cupp_VgR 二化螟 鳞翅目,草螟蛾科 Chilo suppressalis MN227162.1 5 484 14 C.sine_VgR 荔枝蒂蛀虫 鳞翅目,细蛾科 Conopomorpha sinensis KX987145.1 5 424 15 L.stri_VgR 灰飞虱 半翅目,飞虱科 Laodelphax striatella MH347273.1 6 065 16 C.bowr_VgR 大猿叶虫 鞘翅目,叶甲科 Colaphellus bowringi MH104867.1 5 774 17 B.taba_VgR 烟粉虱 半翅目,粉虱科 Bemisia tabaci complex sp. Asia KR818562.2 5 430 18 S.litu_VgR 斜纹夜蛾 鳞翅目,夜蛾科 Spodoptera litura GU983858.1 5 370 19 P.citr_VgR 柑橘全爪螨 蜱螨目,叶螨科 Panonychus citri KC978894.1 5 676 20 H.armi_VgR 棉铃虫 鳞翅目,夜蛾科 Helicoverpa armigera KC181922.2 5 891 21 A.pern_VgR 姬透目天蚕蛾 鳞翅目,天蚕蛾科 Antheraea pernyi JN003583.1 5 847 22 N.luge_VgR 褐飞虱 半翅目,飞虱科 Nilaparvata lugens GU723297.1 6 174 23 C.ital_VgR 意大利蝗 直翅目,蝗科 Calliptamus italicus MK358118.1 5 589 24 S.exig_VgR 甜菜夜蛾 鳞翅目,夜蛾科 Spodoptera exigua KT899978.1 5 445 25 O.furn_VgR 亚洲玉米螟 鳞翅目,螟蛾科 Ostrinia furnacalis MN058042.1 6 289 26 P.xylo_VgR 小菜蛾 鳞翅目,菜蛾科 Plutella xylostella MN044389.1 5 418 27 M.vitr_VgR 豆野螟 鳞翅目,螟蛾科 Maruca vitrata MG799569.1 5 397 28 D.virg_VgR 玉米根萤叶甲 鞘翅目,叶甲科 Diabrotica virgifera KY373243.1 5 612 -
[1] 陈景耀, 柯冲, 陈菁瑛. 荔枝鬼帚病的初步调查及传病试验 [J]. 植物病理学报, 1992(1):26. CHEN J Y, KE C, CHEN J Y. A preliminary study on the incidence and transmission of litchi witches broom [J]. Acta Phytopathologica Sinica, 1992(1): 26.(in Chinese)
[2] 许长藩, 陈景耀, 夏雨华, 等. 荔枝蝽传播龙眼鬼帚病的研究 [J]. 植物病理学报, 1994, 2(2):60−64. XU C F, CHEN J Y, XIA Y H, et al. On transmission of Longyan witches broom by Tessaratoma papillosa(Drury) [J]. Acta Phytopathologica Sinica, 1994, 2(2): 60−64.(in Chinese)
[3] 黎荣欣, 赵冬香, 王玉洁, 等. 荔枝蝽防治研究进展 [J]. 热带作物学报, 2013, 34(1):195−200. LI R X, ZHAO D X, WANG Y J, et al. Research progress of controlling Tessaratoma papillosa(Drury) [J]. Chinese Journal of Tropical Crops, 2013, 34(1): 195−200.(in Chinese)
[4] AMDAM G V, PAGE JR R E, FONDRK M K, et al. Hormone response to bidirectional selection on social behavior [J]. Evolution & Development, 2010, 12(5): 428−436.
[5] 戈林泉, 吴进才. 昆虫卵黄蛋白及其激素调控的研究进展 [J]. 昆虫知识, 2010, 47(2):236−246. GE L Q, WU J C. Research progress in insect vitellin and its hormone regulation [J]. Chinese Bulletin of Entomology, 2010, 47(2): 236−246.(in Chinese)
[6] MATOZZO V, GAGNÉ F, MARIN M G, et al. Vitellogenin as a biomarker of exposure to estrogenic compounds in aquatic invertebrates: A review [J]. Environment International, 2008, 34(4): 531−545. DOI: 10.1016/j.envint.2007.09.008
[7] TUFAIL M, TAKEDA M. Molecular characteristics of insect vitellogenins [J]. Journal of Insect Physiology, 2008, 54(12): 1447−1458. DOI: 10.1016/j.jinsphys.2008.08.007
[8] TUFAIL M, TAKEDA M. Insect vitellogenin/lipophorin receptors: Molecular structures, role in oogenesis, and regulatory mechanisms [J]. Journal of Insect Physiology, 2009, 55(2): 87−103. DOI: 10.1016/j.jinsphys.2009.01.009
[9] TUFAIL M, TAKEDA M. Molecular cloning, characterization and regulation of the cockroach vitellogenin receptor during oogenesis [J]. Insect Molecular Biology, 2005, 14(4): 389−401. DOI: 10.1111/j.1365-2583.2005.00570.x
[10] CIUDAD L, PIULACHS M D, BELLÉS X. Systemic RNAi of the cockroach vitellogenin receptor results in a phenotype similar to that of the Drosophila yolkless mutant [J]. The FEBS Journal, 2006, 273(2): 325−335. DOI: 10.1111/j.1742-4658.2005.05066.x
[11] LIU Q N, ZHU B J, LIU C L, et al. Characterization of vitellogenin receptor (VgR) from the Chinese oak silkworm, Antheraea pernyi [J]. Bulletin of Insectology, 2011, 64(2): 167−174.
[12] QIAN C, FU W W, WEI G Q, et al. Identification and expression analysis of vitellogenin receptor from the wild silkworm, Bombyx mandarina [J]. Archives of Insect Biochemistry and Physiology, 2015, 89(4): 181−192. DOI: 10.1002/arch.21235
[13] WEINSTOCK G M, ROBINSON G E, GIBBS R A, et al. Insights into social insects from the genome of the honeybee Apis mellifera [J]. Nature, 2006, 443(7114): 931−949. DOI: 10.1038/nature05260
[14] CHO K H, RAIKHEL A S. Organization and developmental expression of the mosquito vitellogenin receptor gene [J]. Insect Molecular Biology, 2001, 10(5): 465−474. DOI: 10.1046/j.0962-1075.2001.00285.x
[15] LU K, SHU Y, ZHOU J, et al. Molecular characterization and RNA interference analysis of vitellogenin receptor from Nilaparvata lugens (Stål) [J]. Journal of Insect Physiology, 2015, 73: 20−29. DOI: 10.1016/j.jinsphys.2015.01.007
[16] BROWN M S, GOLDSTEIN J L. A receptor‐mediated pathway for cholesterol homeostasis (Nobel lecture) [J]. Angewandte Chemie International Edition in English, 1986, 25(7): 583−602. DOI: 10.1002/anie.198605833
[17] SAPPINGTON T W, RAIKHEL A S. Molecular characteristics of insect vitellogenins and vitellogenin receptors [J]. Insect Biochemistry and Molecular Biology, 1998, 28(5-6): 277−300. DOI: 10.1016/S0965-1748(97)00110-0
[18] TUFAIL M, TAKEDA M. Vitellogenin of the cockroach, Leucophaea maderae: Nucleotide sequence, structure and analysis of processing in the fat body and oocytes [J]. Insect Biochemistry and Molecular Biology, 2002, 32(11): 1469−1476. DOI: 10.1016/S0965-1748(02)00067-X
[19] HIRAI M, WATANABE D, KIYOTA A, et al. Nucleotide sequence of vitellogenin mRNA in the bean bug, Riptortus clavatus: Analysis of processing in the fat body and ovary [J]. Insect Biochemistry and Molecular Biology, 1998, 28(8): 537−547. DOI: 10.1016/S0965-1748(98)00052-6
[20] RAIKHEL A S, DHADIALLA T S. Accumulation of yolk proteins in insect oocytes [J]. Annual Review of Entomology, 1992, 37: 217−251. DOI: 10.1146/annurev.en.37.010192.001245
[21] SNIGIREVSKAYA E S, RAIKHEL A S. Receptor-mediated endocytosis of yolk proteins in insect oocytes[J]. Progress in vitellogenesis[J]. Reproductive biology of invertebrates, 2005, 12(Part B): 199-228.
[22] ROEHRKASTEN A, FERENZ H J. Role of the lysine and arginine residues of vitellogenin in high affinity binding to vitellogenin receptors in locust oocyte membranes [J]. Biochimica et Biophysica Acta, 1992, 1133(2): 160−166. DOI: 10.1016/0167-4889(92)90064-I
[23] 张维球, 刘秀琼. 荔枝蝽象血淋巴物理性状及“还原能”季节性变化的研究 [J]. 昆虫学报, 1973, 16(1):15−24. ZHANG W Q, LIU X Q. Studies on the seasonal changes of the physical properties and the reducing power of the haemolymph of the lychee stinkbug, Tessaratoma papillsoa drury (Hemiptera: Pentatomidae) [J]. Acta entomologica sinica, 1973, 16(1): 15−24.(in Chinese)
[24] 佘春仁, 潘蓉英, 古德祥, 等. 利用平腹小蜂防治荔枝蝽若干技术问题探讨 [J]. 福建农业大学学报, 1997, 26(4):441−445. SHE C R, PAN R Y, GU D X, et al. Several technological problems of applying Anastatus sp. to control Tessaratoma papillosa [J]. Journal of Fujian Agricultural University, 1997, 26(4): 441−445.(in Chinese)
[25] 佘春仁, 潘蓉英. 荔枝蝽的系统解剖及其在测报上的应用 [J]. 福建农学院学报, 1993(1):59−63. SHE C R, PAN R Y. Systematic dissection for forecasting the pest Tessaratoma papillosa Drury [J]. Journal of Fujian Agricultural college, 1993(1): 59−63.(in Chinese)
[26] LIVAK K J, SCHMITTGEN T D. Analysis of relative gene expression data using real-time quantitative PCR and the 2− ΔΔCT method [J]. Methods, 2001, 25(4): 402−408. DOI: 10.1006/meth.2001.1262
[27] TUFAIL M, NAGABA Y, ELGENDY A M, et al. Regulation of vitellogenin genes in insects [J]. Entomological Science, 2014, 17(3): 269−282. DOI: 10.1016/j.jinsphys.2008.08.007
[28] UPADHYAY S K, SINGH H, DIXIT S, et al. Molecular characterization of vitellogenin and vitellogenin receptor of Bemisia tabaci [J]. PLoS One, 2016, 11(5): e0155306. DOI: 10.1371/journal.pone.0155306
[29] HU K, TIAN P, TANG Y, et al. Molecular characterization of vitellogenin and its receptor in Sogatella furcifera, and their function in oocyte maturation [J]. Frontiers in Physiology, 2019, 10: 1532. DOI: 10.3389/fphys.2019.01532
[30] ROBERTSON J L, PREISLER H K. Pesticide bioassays with arthropods[M]. CRC Press, 1992: 127.
[31] THOMPSON J R, BANASZAK L J. Lipid-protein interactions in lipovitellin [J]. Biochemistry, 2002, 41(30): 9398−9409. DOI: 10.1021/bi025674w
[32] HUSAIN M, RASOOL K G, TUFAIL M, et al. RNAi-mediated silencing of vitellogenin gene curtails oogenesis in the almond moth Cadra cautella [J]. PloS one, 2021, 16(2): e0245928. DOI: 10.1371/journal.pone.0245928
[33] MORANDIN C, HAVUKAINEN H, KULMUNI J, et al. Not only for egg yolk—functional and evolutionary insights from expression, selection, and structural analyses of Formica ant vitellogenins [J]. Molecular Biology and Evolution, 2014, 31(8): 2181−2193. DOI: 10.1093/molbev/msu171
[34] PIULACHS M D, GUIDUGLI K R, BARCHUK A R, et al. The vitellogenin of the honey bee, Apis mellifera: Structural analysis of the cDNA and expression studies [J]. Insect Biochemistry and Molecular Biology, 2003, 33(4): 459−465. DOI: 10.1016/S0965-1748(03)00021-3
[35] CORONA M, LIBBRECHT R, WURM Y, et al. Vitellogenin underwent subfunctionalization to acquire caste and behavioral specific expression in the harvester ant Pogonomyrmex barbatus [J]. PLoS Genetics, 2013, 9(8): e1003730. DOI: 10.1371/journal.pgen.1003730
[36] YANO K, SAKURAI M T, WATABE S, et al. Structure and expression of mRNA for vitellogenin in Bombyx mori [J]. Biochimica et Biophysica Acta, 1994, 1218(1): 1−10. DOI: 10.1016/0167-4781(94)90094-9
[37] MARTÍN D, PIULACHS M D, COMAS D, et al. Isolation and sequence of a partial vitellogenin cDNA from the cockroach, Blattella germanica (L.) (Dictyoptera, Blattellidae), and characterization of the vitellogenin gene expression [J]. Archives of Insect Biochemistry and Physiology, 1998, 38(3): 137−146. DOI: 10.1002/(SICI)1520-6327(1998)38:3<137::AID-ARCH4>3.0.CO;2-P
[38] TUFAIL M, HATAKEYAMA M, TAKEDA M. Molecular evidence for two vitellogenin genes and processing of vitellogenins in the American cockroach, Periplaneta americana [J]. Archives of Insect Biochemistry and Physiology, 2001, 48(2): 72−80. DOI: 10.1002/arch.1059
[39] SHEN Y, CHEN Y Z, LOU Y H, et al. Vitellogenin and vitellogenin-like genes in the brown planthopper [J]. Frontiers in Physiology, 2019, 10: 1181. DOI: 10.3389/fphys.2019.01181
[40] ROMANS P, TU Z, KE Z, et al. Analysis of a vitellogenin gene of the mosquito, Aedes aegypti and comparisons to vitellogenins from other organisms [J]. Insect Biochemistry and Molecular Biology, 1995, 25(8): 939−958. DOI: 10.1016/0965-1748(95)00037-V
[41] SMITH C D, ZIMIN A, HOLT C, et al. Draft genome of the globally widespread and invasive Argentine ant (Linepithema humile) [J]. Proceedings of the National Academy of Sciences, 2011, 108(14): 5673−5678. DOI: 10.1073/pnas.1008617108
[42] COLETTA A, PINNEY J W, SOLÍS D Y W, et al. Low-complexity regions within protein sequences have position-dependent roles [J]. BMC Systems Biology, 2010, 4(1): 1−13. DOI: 10.1186/1752-0509-4-1
[43] LYNCH M, CONERY J S. The evolutionary fate and consequences of duplicate genes [J]. Science, 2000, 290(5494): 1151−1155. DOI: 10.1126/science.290.5494.1151
[44] CONG L, YANG W J, JIANG X Z, et al. The essential role of vitellogenin receptor in ovary development and vitellogenin uptake in Bactrocera dorsalis (hendel) [J]. International Journal of Molecular Sciences, 2015, 16(8): 18368−18383. DOI: 10.3390/ijms160818368
[45] ZHANG W, MA L, XIAO H, et al. Molecular characterization and function analysis of the vitellogenin receptor from the cotton bollworm, Helicoverpa armigera (Hübner) (Lepidoptera, Noctuidae) [J]. PloS ONE, 2016, 11(5): e0155785. DOI: 10.1371/journal.pone.0155785
[46] YAO Q, XU S, DONG Y Z, et al. Characterization of vitellogenin and vitellogenin receptor of Conopomorpha sinensis Bradley and their responses to sublethal concentrations of insecticide [J]. Frontiers in Physiology, 2018, 9: 1250. DOI: 10.3389/fphys.2018.01250
[47] SAYAH F, FAYET C, IDAOMAR M, et al. Effect of azadirachtin on vitellogenesis of Labidura riparia (Insect Dermaptera) [J]. Tissue and Cell, 1996, 28(6): 741−749. DOI: 10.1016/S0040-8166(96)80077-2
[48] AMIR M. Histopathological effect of some toxicants on the female reproductive system of Sarcophaga ruficornis Fabricius (Diptera: Sarcophagidae) [J]. Cibtech Journal of Zoology ISSN, 2014, 3(2): 2319−38831.
[49] ZHOU C, YANG X B, YANG H, et al. Effects of sublethal concentrations of insecticides on the fecundity of Sogatella furcifera (Hemiptera: Delphacidae) via the regulation of vitellogenin and its receptor [J]. Journal of Insect Science, 2020, 20(5): 14. DOI: 10.1093/jisesa/ieaa099
-
期刊类型引用(0)
其他类型引用(4)




 下载:
下载: