Cloning and Bioinformatics of Chalcone Synthase Gene of Moringa oleifera
-
摘要:目的 查尔酮合成酶是黄酮类生物合成途径中的第1个限速酶基因。从辣木中克隆查尔酮合成酶基因MoCHS1,并对其进行生物信息学分析,为进一步研究其生物学功能提供基础数据。方法 根据NCBI数据库中的辣木基因组信息设计引物,以辣木叶片cDNA和基因组DNA为模板,PCR扩增获得MoCHS1基因序列。利用生物信息学方法分析其序列特征,使用DNAMAN9.0和MEGA10.0软件进行多重比对和构建系统进化树。结果 MoCHS1 ORF序列长度为1 185 bp,编码394个氨基酸,基因组序列长1 387 bp,含有2个外显子和1个内含子。生物信息学分析表明,MoCHS1为稳定的亲水蛋白,以α-螺旋(45.43%)和不规则卷曲(31.98%)为主。MoCHS1含有查尔酮合成酶家族的保守序列和酶活性位点的关键氨基酸残基,包括7个环化袋氨基酸残基、3个辅酶A活性结合位点、半胱氨酸(Cys)-组氨酸(His)-天冬氨酸(Asn)三联体催化位点和查尔酮合成酶基因家族的2个高度保守的特征序列(RLMMYQQGCFAGGTVLR和GVLFGFGPGL),与其他物种的CHS 序列一致性较高。系统进化分析显示,MoCHS1与番木瓜聚在一类,说明其亲缘关系最近。结论 成功分离了一个辣木查尔酮合成酶基因MoCHS1基因序列,该基因推测编码的氨基酸序列具有CHS家族蛋白的典型保守结构特征。研究结果有助于进一步研究辣木查尔酮合成酶基因的调控及基因家族进化机制和类黄酮合成调控机理。Abstract:Objective The open reading frame and gDNA of the gene associated with the chalcone synthase (CHS), the first key enzyme in the flavonoid biosynthetic pathway in Moringa oleifera, were cloned for a bioinformatic analysis.Method Primers were designed according to the M. oleifera genome in NCBI database. The leaf cDNA and genomic DNA were used as templates to amplify the MoCHS1 with PCR for a subsequent bioinformatic analysis. DNAMAN 9.0 and MEGA 10.0 were used for the multiple sequence alignment and phylogenetic tree construction.Result The ORF of MoCHS1
was 1 185 bp encoded 394 amino acids. The genomic DNA spanned 1 387 bp containing 2 exons and 1 intron. MoCHS1 was a stable hydrophilic protein with a structure of 45.43% α helix and 31.98% random coil. The gene possessed conserved sequence as well as enzymatic site residues of the CHS gene superfamily, which included 7 amino acid residues of the cyclization pocket, the Cys-His-Asn catalytic triad sites, and the family signatures of CHSs (‘RLMMYQQGCFAGGTVLR’ and ‘GVLFGFGPGL’) sharing a high similarity with the CHS proteins of other species. The phylogenetic tree of MoCHS1 closely related to and in the same clade with the CHS of Carica papaya. Conclusion MoCHS1was successfully isolated from M. oleifera sharing a typical conserved structure of the CHS gene family. The results provided crucial information for further study on the genes related to the flavonoid metabolic pathway as well as the expression regulation and evolution of the CHS gene family in M. oleifera. -
Keywords:
- Moringa oleifera /
- flavonoid /
- chalcone synthase /
- bioinformatic analysis
-
0. 引言
【研究意义】辣木(Moringa oleifera Lam.)也称鼓槌树,属于十字花目辣木科辣木属,为多年生热带落叶乔木,广泛种植于亚洲、非洲和中美洲的热带、亚热带地区,在我国云南、广西、广东、台湾、福建等地均有种植[1-4]。辣木富含黄酮类化合物(flavonoids)、植物蛋白、维生素A、维生素C、叶酸、泛酸、钙、铁、锌、硒、钾等多种营养素,具有“超级营养库”之称[2]。研究表明,类黄酮化合物是辣木叶中的主要组分之一,平均含量在3%~6%[1,4]。药理学研究表明,辣叶黄酮类提取物在II型糖尿病的预防和治疗中可降低葡萄糖耐受、血糖及血脂含量[1];王玲玲等[3]研究表明辣木叶总黄酮提取物能提高运动耐力,延缓疲劳发生。2012年我国卫生部批准将辣木叶作为新资源食品,可用于功能食品开发[3]。因此,开展辣木植物中黄酮类化合物的生物合成途径中的关键酶基因的克隆、功能鉴定及其调控机制的研究,有助于提高辣木的品质及其资源的开发利用。【前人研究进展】目前,有关黄酮类化合物的生物合成途径的步骤已基本清楚[5,6]。查尔酮合成酶(chalcone synthase,CHS,EC2.3.1.74)为III 型聚酮体合成酶(polyketide synthase,PKS)家族的一员,是启动黄酮类化合物次生代谢生物合成的第1个关键限速酶,负责催化3分子丙二酰-CoA和1分子对香豆酰-CoA缩合形成查尔酮[7-13],随后进一步产生各类的黄酮类化合物(如芦丁,花青素等)。CHS广泛存在于植物中,目前,已从烟草[8]、大豆[9]、藤茶[5]等众多植物中克隆和鉴定了CHS基因。【本研究切入点】目前,虽然对辣木基因组序列进行了测序,但对于辣木查尔酮合成酶的克隆及注释有待进一步深入研究。【拟解决的关键问题】本研究拟基于NCBI数据库中辣木基因组信息结合其他植物的查尔酮合成酶基因核苷酸序列设计PCR引物,通过PCR技术分别分离1条辣木CHS基因(命名为MoCHS1
)的完整开放读码框序列(open reading frame, ORF)和基因组DNA(genomic DNA),并对其进行生物信息学分析,为进一步解析辣木类黄酮物质的生物合成与调控机制及CHS基因家族进化提供科学依据。 1. 材料与方法
1.1 试验材料
辣木叶片采取福建农林大学田间植物园。
1.2 总RNA的提取及cDNA第一链的合成
采用Omega公司Plant RNA Kit提取辣木叶片总RNA,操作步骤按照说明书进行,经琼脂糖电泳及核酸蛋白检测仪检测符合反转录要求的RNA 样品溶液,置于−80 ℃冰箱保存备用。利用湖南艾科瑞生物工程有限公司Evo M-MLV RT试剂盒进行辣木cDNA第一链的合成。
1.3 引物设计与合成
根据NCBI数据库中辣木基因组信息结合其他植物CHS基因信息,利用 DNAMAN 9.0 软件在起始密码子及终止密码附近设计引物一对,引物由福州尚亚生物技术有限公司合成,引物序列:MoCHSF:5′-GTCATCAATGGCGGCATCAGTG-3′;MoCHSR:5′-ACCACTCACTCCCTACCCTTGAT-3′。
1.4 辣木CHS1基因的克隆
利用1.3设计的PCR引物进行辣木CHS基因的克隆。PCR反应体系如下:MoCHSF和MoCHSR(约100 ng·μL−1)各1 μL,10×Buffer 2 μL,Taq DNA polymerase(5 U·μL−1)0.2 μL,dNTPs(10 mmol·L−1)0.5 μL,正反向引物各1 μL,ddH2O 14.3 μL。PCR反应条件:94 ℃预变性5 min 后,分别于94 ℃变性30 s、62 ℃退火30 s和72 ℃延伸90 s,共进行30 个循环,最后在72 ℃延伸10 min。PCR产物保存于4 ℃备用。PCR 产物在经1%琼脂糖凝胶电泳后,用凝胶成像仪拍照,并切下目的条带。利用OMEGA公司的 Gel Extraction Kit回收纯化目的DNA 片段,纯化后的DNA 连接到pESAY-T1 克隆载体(TransGen Biotech),转化大肠杆菌感受态DH5α菌株,筛选并经PCR鉴定的阳性菌落送福州尚亚生物技术有限公司测序。
1.5 辣木CHS1生物信息学分析
利用Blast软件(http://www.ncbi.nlm.nih.gov/Blast)进行在线核苷酸和氨基酸序列分析;利用Protparam(http://web.expasy.org/protparam/)进行在线氨基酸序列相对分子质量、等电点、不稳定系数等理化性质进行分析;利用PSORTPrediction(https://wolfpsort.hgc.jp/)进行蛋白亚细胞定位分析;利用SignalP-5.0 Server(http://www.cbs.dtu.dk/services/SignalP/)进行氨基酸信号肽预测;采用SOPMA(https://npsa-prabi.ibcp.fr/cgi-bin/npsa_automat.pl/page=npsa_sopma.html)预测蛋白二级结构;利用DNAMAN 9.0进行查尔酮合成酶基因编码氨基酸序列多重比对分析;采用MEGA 10.0软件构建CHS蛋白的系统发育树。
2. 结果与分析
2.1 MoCHS1
基因的克隆与结构分析 分别以辣木的cDNA和基因组DNA为模板,利用特异引物CHSF 和CHSR 扩增,分别获得约1 200 bp和1 500 bp的特异条带(图1-A),经过胶回收、克隆测序及Blast比对分析发现,该DNA片段与GenBank 核酸数据库中登录的番木瓜(Carica papaya)、石榴(Punica granatum)、芸香(Ruta graveolens)、山葡萄(Vitis amurensis)等植物的查尔酮合成酶的编码序列相似性较高,推导的氨基酸序列也与数据库中已知的CHS蛋白氨基酸序列的相似性也较高,由此可以初步推测分离所得DNA序列为辣木查尔酮合成酶的基因序列,并命名该基因为MoCHS1
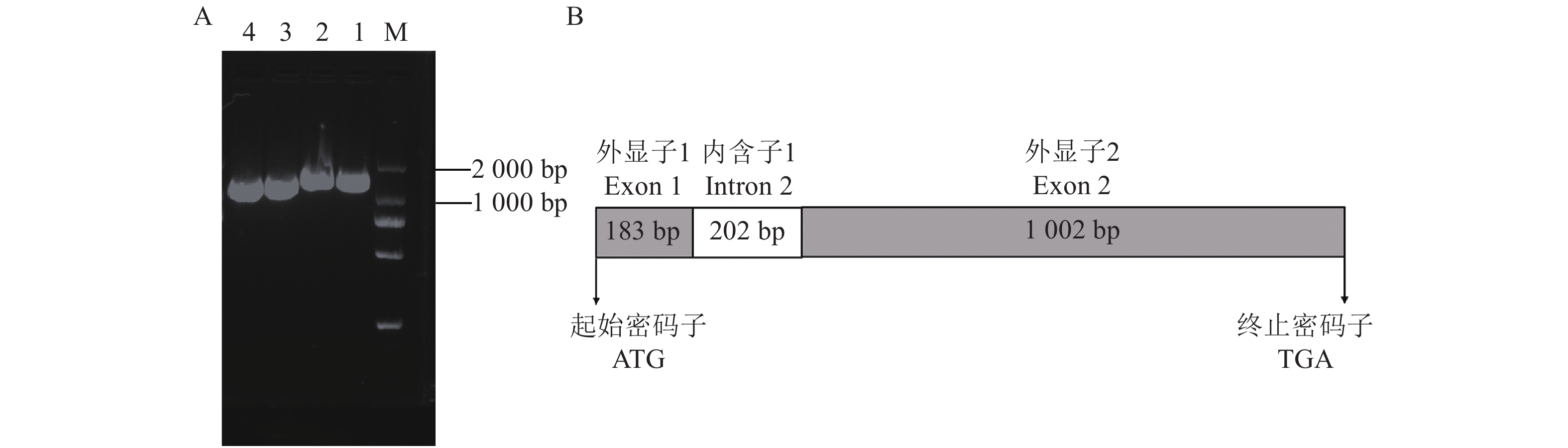
。序列分析表明,以cDNA为模板扩增得到的MoCHS1 ORF序列长度为1 185 bp,编码394个氨基酸(图2),以辣木基因组DNA为模板扩增得到的gDNA序列长度为1 387 bp,两者对比发现,MoCHS1基因中间具有一个内含子(202 bp)序列,外显子1为183 bp,外显子2为1 002 bp(图1-B)。 ![]() 图 1 辣木MoCHS1基因的克隆与结构分析注:A: MoCHS1的PCR扩增产物,M:DL2 000;1,2:以基因组DNA 为模板的扩增产物;3,4:以cDNA为模板扩增产物。B:MoCHS1基因的结构模式图Figure 1. Cloning and structure of MoCHS1
图 1 辣木MoCHS1基因的克隆与结构分析注:A: MoCHS1的PCR扩增产物,M:DL2 000;1,2:以基因组DNA 为模板的扩增产物;3,4:以cDNA为模板扩增产物。B:MoCHS1基因的结构模式图Figure 1. Cloning and structure of MoCHS1of M. oleifera Note: A: PCR amplification product of MoCHS1; M: DL2000; 1 and 2: PCR amplification product of cDNA; 3 and 4: PCR amplification product of genomic DNA; B: structure of MoCHS1.2.2 MoCHS1蛋白质理化性质分析
采用ProParam在线分析工具,对MoCHS1氨基酸序列的理化性质进行预测,结果显示MoCHS1的相对分子量为43.07 KD,等电点(pI)为5.84,分子式为:C1914H3071N515O573S19,不稳定指数为36.04<40,脂肪族指数为93.83,总亲水性平均值(GRAVY)为−0.067<0,推测该蛋白为稳定亲水蛋白。在MoCHS1编码的氨基酸中,含量最高的是亮氨酸和丙氨酸,分别占10.4%和9.1%,半胱氨酸和色氨酸所占比例最小,分别占1.8%和1.0%;其中带负电荷氨基酸残基(Asp + Glu)总数50个,占氨基酸总数的12.7%,而带正电荷氨基酸残基总数为44个,占氨基酸总数为11.2%,推测该蛋白带负电荷。
2.3 MoCHS蛋白质结构分析
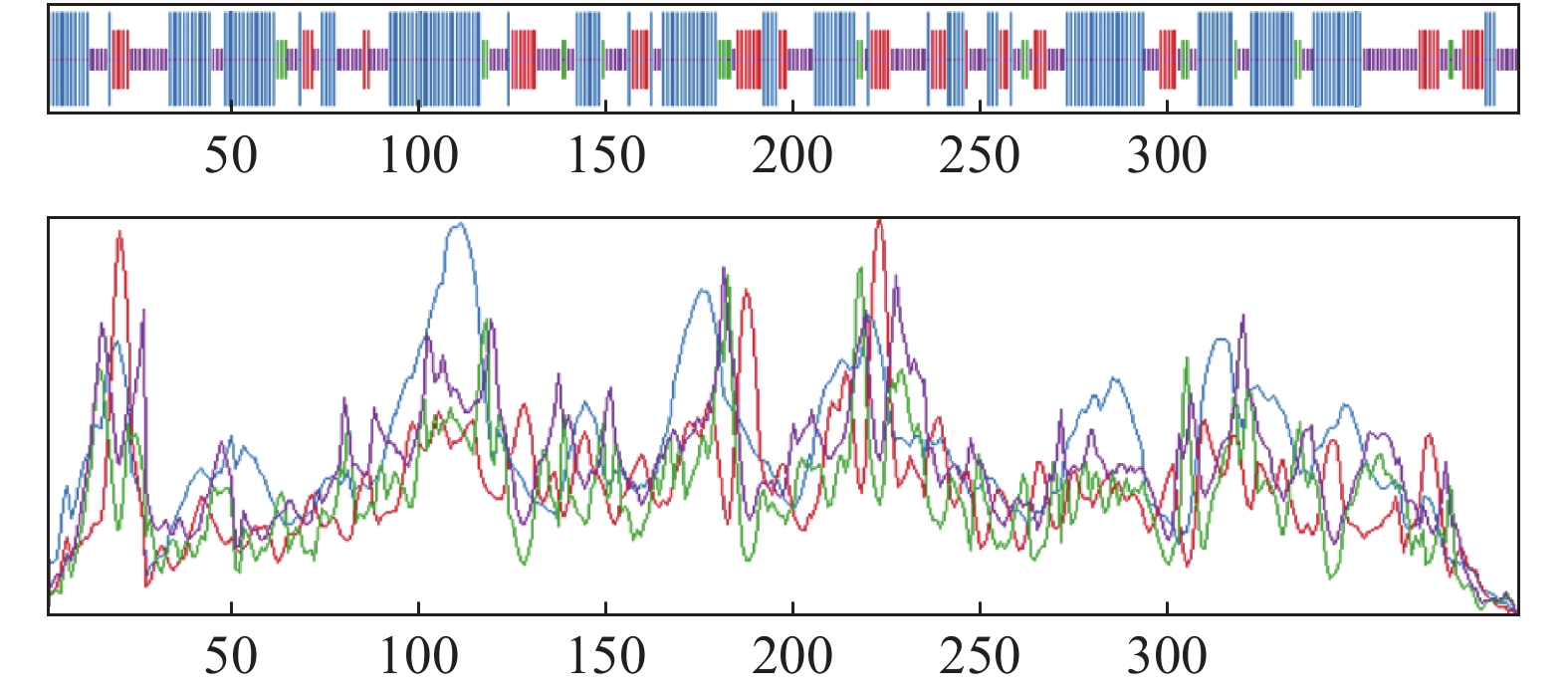
采用SignalP 5.0在线分析表明,辣木MoCHS1蛋白没信号肽;Wolf-psort分析MoCHS蛋白的亚细胞定位显示,在细胞质、叶绿体及液泡中均有分布,而以在细胞质中分布为主。使用SOPMA工具进行分析二级结构分析表明MoCHS1蛋白以α-螺旋(45.43%)和不规则卷曲(31.98%)为主,其次有延伸链(16.75%)、β-转角(5.84%)(图3)。采用Swiss-model对MoCHS1蛋白的三级结构进行预测(图4),结果与其二级结构预测相一致。
2.4 MoCHS的系统进化分析
利用DNAMAN9.0对推测的辣木MoCHS1的氨基酸序列与大豆(GmCHS,)、番木瓜(CpCHS)、拟南芥、烟草、葡萄、黄芩等植物CHS基因氨基酸序列进行多序列比对。结果(图4)表明辣木MoCHS1与大豆、番木瓜、拟南芥、烟草、葡萄、黄芩的相似度分别为85%、88%、84.9%、85.9%、87.5%、81.3%。MoCHS1和其他植物中的CHS蛋白一样,含有查尔酮合成酶基因家族高度保守的氨基酸残基,包括7个环化袋氨基酸残基、3个辅酶A活性结合位点、半胱氨酸(Cys)-组氨酸(His)-天冬氨酸(Asn)三联体催化活性位点和CHS基因家族的2个高度保守氨基酸特征序列(RLMMYQQGCFAGGTVLR和GVLFGFGPGL)(图5)。这些结果进一步说明本研究所克隆的基因序列为辣木查尔酮合成酶基因序列。
![]() 图 5 辣木MoCHS1氨基酸序列与其他物种CHS氨基酸序列的多序列比对分析注:星号标出的三个氨基酸残基为辅酶A活性结合位点;箭头所示为环化袋残基位点;四方体所示三联体催化位点;下划线所示为查尔酮合成酶基因家族特征序列。Figure 5. Multiple alignment on amino acid sequences of CHS of M. oleifera and other speciesNote: Asterisks: active CoA-binding sites (Lys, Arg, and Lys); arrows: 7 amino acid residues of cyclization pocket including Thr, Met, Phe, Ile, Gly, Phe, and Pro sites; squares: catalytic triad sites of Cys, His, and Asn, and family signatures of CHSs (‘RLMMYQQGCFAGGTVLR’ and ‘GVLFGFGPGL’) are underlined.
图 5 辣木MoCHS1氨基酸序列与其他物种CHS氨基酸序列的多序列比对分析注:星号标出的三个氨基酸残基为辅酶A活性结合位点;箭头所示为环化袋残基位点;四方体所示三联体催化位点;下划线所示为查尔酮合成酶基因家族特征序列。Figure 5. Multiple alignment on amino acid sequences of CHS of M. oleifera and other speciesNote: Asterisks: active CoA-binding sites (Lys, Arg, and Lys); arrows: 7 amino acid residues of cyclization pocket including Thr, Met, Phe, Ile, Gly, Phe, and Pro sites; squares: catalytic triad sites of Cys, His, and Asn, and family signatures of CHSs (‘RLMMYQQGCFAGGTVLR’ and ‘GVLFGFGPGL’) are underlined.运用MEGA10.0软件构建辣木MoCHS1与大豆、拟南芥、烟草等29种植物CHS编码氨基酸序列的系统进化树。结果表明,MoCHS1与来源于番木瓜的CHS基因聚在一类,说明其亲缘关系最近,与来源于破布叶、麻风树等植物CHS基因的进化关系也较近,而与来源于玉米、水稻、小麦等单子叶植物的CHS基因进化关系较远(图6)。
3. 讨论与结论
查尔酮合成酶(CHS)属于高等植物中高度保守的III 型聚酮体合成酶(polyketide synthase, PKS),是植物黄酮类化合物合成途径的第1个关键酶,参与重要中间产物查尔酮的形成[5,13,14]。前人研究表明,大部分植物的CHS基因家族均含有1个内含子[8-10]。本研究根据NCBI中辣木基因组测序结果设计引物,首次分别从cDNA和基因组DNA中分离获得MoCHS1
。序列分析表明,以cDNA为模板扩增得到的MoCHS1 ORF序列长度为1 185 bp,编码394个氨基酸,以基因组DNA为模板扩增得到的gDNA序列长度为1 387 bp,两者对比发现,MoCHS1具有1个内含子,结构特征与基因大小与多数物种CHS的大小基本一致。MoCHS1蛋白亚细胞定位结果显示该蛋白主要分布在细胞质中。蛋白质的二级结构主要有α-螺旋、β-转角、β-折叠及不规则卷曲,其中α-螺旋是蛋白质中最常见的二级结构元件,不规则卷曲也是明确而稳定的结构[15]。不同植物中的CHS基因在数量、结构和功能上均存在差异[15],MoCHS1蛋白的二级结构主要以α-螺旋(45.43%)和不规则卷曲(31.98%)为主,β-转角(5.84%)最少。MoCHS1蛋白的三级结构以α-螺旋和不规则卷曲为主,与二级结构预测结果基本一致。推导的氨基酸序列分析表明,MoCHS1含有所有查尔酮合成酶基因家族中高度保守的特征氨基酸序列“GVLFGFGPGL”及活性氨基酸残基位点,如辅酶A活性结合位点、Cys-His-Asn三联体催化位点和环化袋等[16-18]。这些结构特征表明本研究克隆的基因序列具备CHSs家族的共有特性,为辣木CHS的序列[5,11,13,16,17]。Blast在线分析也表明,辣木MoCHS推测的氨基酸序列与其他植物中的CHSs相似性较高,其中与来源于番木瓜、麻风树等药用植物的CHSs的相似性均在85%以上,表明该基因与NCBI数据库中查尔酮合成酶相关基因亲缘关系越近。此外,3D结构模型及系统进化分析均证实MoCHS1与其他植物相一致。以上研究结果表明本研究中MoCHS1属于典型的查尔酮合成酶家族基因。[11-14,19] 本研究首次克隆了辣木CHS1 基因的全长ORF和gDNA序列,将有助于进一步阐明辣木类黄酮人化合物的合成及基调控机制提供科学依据,以期为利用生物技术手段改变植物类黄酮化合物含量,为进一步开发和利用辣木植物资源奠定理论基础。
-
图 1 辣木MoCHS1基因的克隆与结构分析
注:A: MoCHS1的PCR扩增产物,M:DL2 000;1,2:以基因组DNA 为模板的扩增产物;3,4:以cDNA为模板扩增产物。B:MoCHS1基因的结构模式图
Figure 1. Cloning and structure of MoCHS1
of M. oleifera Note: A: PCR amplification product of MoCHS1; M: DL2000; 1 and 2: PCR amplification product of cDNA; 3 and 4: PCR amplification product of genomic DNA; B: structure of MoCHS1.
图 5 辣木MoCHS1氨基酸序列与其他物种CHS氨基酸序列的多序列比对分析
注:星号标出的三个氨基酸残基为辅酶A活性结合位点;箭头所示为环化袋残基位点;四方体所示三联体催化位点;下划线所示为查尔酮合成酶基因家族特征序列。
Figure 5. Multiple alignment on amino acid sequences of CHS of M. oleifera and other species
Note: Asterisks: active CoA-binding sites (Lys, Arg, and Lys); arrows: 7 amino acid residues of cyclization pocket including Thr, Met, Phe, Ile, Gly, Phe, and Pro sites; squares: catalytic triad sites of Cys, His, and Asn, and family signatures of CHSs (‘RLMMYQQGCFAGGTVLR’ and ‘GVLFGFGPGL’) are underlined.
-
[1] CHEN G L, XU Y B, WU J L, et al. Hypoglycemic and hypolipidemic effects of Moringa oleifera leaves and their functional chemical constituents [J]. Food Chemistry, 2020, 333: 127478. DOI: 10.1016/j.foodchem.2020.127478
[2] 周滢, 梁敏丽, 解雅倩, 等. 辣木籽总黄酮提取工艺优化 [J]. 广东化工, 2020(20):18−20. DOI: 10.3969/j.issn.1007-1865.2020.20.010 ZHOU Y, LIANG M L, XIE Y Q, et al. To Optimize the Extraction Technology of Total Flavonoids from Moringa Oleifera Seed [J]. Guangdong Chemical Industry, 2020(20): 18−20.(in Chinese) DOI: 10.3969/j.issn.1007-1865.2020.20.010
[3] 王玲玲, 边祥雨, 高蔚娜, 等. 辣木叶总黄酮提取物抗疲劳功效的研究 [J]. 营养学报, 2020, 42(1):68−77. DOI: 10.3969/j.issn.0512-7955.2020.01.014 WANG L L, BIAN X Y, GAO W N, et al. Anti-fatigue effect of total flavonoids extract from Moringa oleifera leaves [J]. Acta Nutrimenta Sinica, 2020, 42(1): 68−77.(in Chinese) DOI: 10.3969/j.issn.0512-7955.2020.01.014
[4] PASHA S N, SHAFI K M, JOSHI A G, et al. The transcriptome enables the identification of candidate genes behind medicinal value of Drumstick tree (Moringa oleifera) [J]. Genomics, 2020, 112(1): 621−628. DOI: 10.1016/j.ygeno.2019.04.014
[5] 许明, 林世强, 倪冬昕, 等. 藤茶查尔酮合成酶基因AgCHS1的克隆及功能鉴定 [J]. 中国农业科学, 2020, 53(24):5091−5103. DOI: 10.3864/j.issn.0578-1752.2020.24.012 XU M, LIN S Q, NI D X, et al. Cloning and function characterization of chalcone synthase gene AgCHS1 in Ampelopsis grossedentata [J]. Scientia Agricultura Sinica, 2020, 53(24): 5091−5103.(in Chinese) DOI: 10.3864/j.issn.0578-1752.2020.24.012
[6] TOHGE T, DE SOUZA L P, FERNIE A R. Current understanding of the pathways of flavonoid biosynthesis in model and crop plants [J]. Journal of Experimental Botany, 2017, 68(15): 4013−4028. DOI: 10.1093/jxb/erx177
[7] 张声祥, 施圆圆, 王晨凯, 等. 异叶天南星查尔酮合成酶和异构酶基因的克隆及蛋白的结构性质分析 [J]. 中国中药杂志, 2019, 44(9):1799−1807. ZHANG S X, SHI Y Y, WANG C K, et al. Cloning and characterization of Chalcone synthase and Chalcone isomerase genes in Arisaema heterophyllum [J]. China Journal of Chinese Materia Medica, 2019, 44(9): 1799−1807.(in Chinese)
[8] CHEN S, PAN X H, LI Y T, et al. Identification and characterization of Chalcone synthase gene family members in Nicotiana tabacum [J]. Journal of Plant Growth Regulation, 2017, 36(2): 374−384. DOI: 10.1007/s00344-016-9646-6
[9] ANGURAJ V A K, KRYSIAK K, TIAN G, et al. Genome-wide identification and localization of chalcone synthase family in soybean (Glycine max [L]Merr) [J]. BMC Plant Biology., 2018, 18(1): 325. DOI: 10.1186/s12870-018-1569-x
[10] KODURI P K H, GORDON G S, BARKER E I, et al. Genome-wide analysis of the Chalcone synthase superfamily genes of Physcomitrella patens [J]. Plant Molecular Biology, 2010, 72(3): 247−263. DOI: 10.1007/s11103-009-9565-z
[11] ABE I, MORITA H. Structure and function of the chalcone synthase superfamily of plant type III polyketide synthases [J]. Natrual Procuct Reports, 2010, 27(6): 809−838. DOI: 10.1039/b909988n
[12] WANG C H, ZHI S, LIU C Y, et al. Isolation and characterization of a novel Chalcone synthase gene family from mulberry [J]. Plant Physiology and Biochemistry, 2017, 115: 107−118. DOI: 10.1016/j.plaphy.2017.03.014
[13] LIOU G, CHIANG Y C, WANG Y, et al. Mechanistic basis for the evolution of Chalcone synthase catalytic cysteine reactivity in land plants [J]. The Journal of Biological Chemistry, 2018, 293(48): 18601−18612. DOI: 10.1074/jbc.RA118.005695
[14] 康亚兰, 裴瑾, 刘薇, 等. 红花查尔酮合成酶基因的克隆、生物信息学分析及表达 [J]. 中草药, 2014, 45(16):2385−2389. DOI: 10.7501/j.issn.0253-2670.2014.16.020 KANG Y L, PEI J, LIU W, et al. Cloning, bioinformatic analysis, and expression of Chalcone synthase gene in Carthamus tinctorius [J]. Chinese Traditional and Herbal Drugs, 2014, 45(16): 2385−2389.(in Chinese) DOI: 10.7501/j.issn.0253-2670.2014.16.020
[15] 关淑文, 王毅, 郝佳波, 等. 竹叶花椒查尔酮合成酶基因克隆与表达 [J]. 分子植物育种, 2020, 18(16):5300−5305. GUAN S W, WANG Y, HAO J B, et al. Cloning and expression of Chalcone synthase gene from Zanthoxylum armatum [J]. Molecular Plant Breeding, 2020, 18(16): 5300−5305.(in Chinese)
[16] 孙朝霞, 侯思宇, 郭彬, 等. 苦荞查尔酮合成酶基因序列特征及分子进化分析 [J]. 分子植物育种, 2014, 12(4):772−779. SUN Z X, HOU S Y, GUO B, et al. Characterize of sequences and molecular evolution analysis of Chalcone synthase in Fagopyrum tartaricum [J]. Molecular Plant Breeding, 2014, 12(4): 772−779.(in Chinese)
[17] YAHYAA M, ALI S, DAVIDOVICH-RIKANATI R, et al. Characterization of three chalcone synthase-like genes from apple (Malus × domestica Borkh.) [J]. Phytochemistry., 2017, 140: 125−133. DOI: 10.1016/j.phytochem.2017.04.022
[18] HAN Y Y, ZHAO W W, WANG Z C, et al. Molecular evolution and sequence divergence of plant Chalcone synthase and Chalcone synthase-Like genes [J]. Genetica, 2014, 142(3): 215−225. DOI: 10.1007/s10709-014-9768-3
[19] SANJARI S, SHOBBAR Z S, EBRAHIMI M, et al. Chalcone synthase genes from milk thistle (Silybum marianum): Isolation and expression analysis [J]. Journal of Genetics, 2015, 94(4): 611−617. DOI: 10.1007/s12041-015-0560-7
-
期刊类型引用(1)
1. 孙卓楠,付振鑫,孙玉荣,刘旭,张宝俊. 谷子CHs家族全基因组鉴定及表达分析. 山西农业科学. 2022(03): 281-288 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载: