Physiology of Adonis amurensis as Affected by Drought
-
摘要:目的 研究侧金盏花植株在干旱及复水条件下的生理特性,为其引种栽培及应用提供理论依据。方法 采用盆栽控水方式,研究不同程度干旱胁迫对其生理特性的影响。结果 随胁迫程度加重,侧金盏花生物量、株高、叶片相对含水量、叶绿素(Chl)总量、可溶性蛋白含量降低,可溶性糖、丙二醛(MDA)含量和叶片相对电导率增加,脯氨酸(Pro)含量、过氧化物酶(POD)和超氧化物歧化酶(SOD)活性先上升后下降;净光合速率(Pn
)、气孔导度(Gs)、蒸腾速率(Tr)和胞间二氧化碳浓度(Ci)均下降,最大荧光(Fm)、光系统Ⅱ(PSⅡ)潜在活性、PSⅡ最大光化学量子产量、光化学猝灭系数(qp)、表观光合电子传递速率和PSⅡ实际光化学量子产量降低,初始荧光和非光化学猝灭逐渐增大;干旱前期(0~8 d)进行复水,土壤相对含水量不低于29.9%,各生理指标基本恢复至对照,干旱中期(8~12 d)复水后,各指标恢复速度较慢,干旱后期(12~16 d)复水后,各生理指标与对照相比差异显著。 结论 侧金盏花维持正常生长所能承受的持续干旱最长时间是8 d,其土壤相对含水量下限为29.9%;持续干旱8 d后,对侧金盏花造成不可逆伤害,因此对侧金盏花进行补水最晚不超过干旱发生的8 d。Abstract:Objective Physiological characteristics of Adonis amurensis in response to varying degrees of drought stress and subsequent rewatering were studied prior to the introduction for commercial cultivation and applications of the cultivar.Method Potting with controlled watering was applied to study the effects of varied drought stress and subsequent rewatering on the physiological characteristics of A. amurensis.Result The depleting water supply to the A. amurensis plants decreased the biomass, plant height, relative moisture content in leaf, total chlorophyll, and soluble protein, increased the contents of soluble sugar and malondialdehyde as well as the relative electrical conductivity of the leaves, and rose but followed by a decline on the contents of proline, peroxidase, and superoxide dismutase activities of the plants. Meanwhile, the indicators such as Pn, Gs, Tr, and Ci decreased, Fm, Fv/Fo, Fv/Fm, qP, ETR, and ФPSⅡgradually decreased, and Fo and NPQ gradually increased. Upon rewatering the soil to a moisture content no less than 29.9% in the early stage of drought treatment (0-8 d), the physiological indices fully returned to the control levels. However, the recovery slowed down when the rewatering took place in the mid stage (8-12 d), and the indices shifted significantly from control if the rewatering was implemented during 12-16 d after the draught stress began. Conclusion A. amurensis plants seemed to be capable of withstanding continuous water depletion up to 8 d and maintaining normal growth with a minimum 29.9% of soil relative moisture content. After the threshold points, prolonged drought stress with less than the minimum water requirement in the soil would irreversibly damage the plant physiology.Therefore, water supplement for A. amurensis should not exceed 8 days under drought condition.-
Keywords:
- Adonis amurensis /
- drought stress /
- physiological characteristics
-
0. 引言
【研究意义】侧金盏花(Adonis amurensis)是毛茛科侧金盏花属多年生草本植物,分布于我国东北地区,侧金盏花耐寒性强,在冰雪未融化之际便可开放,可作为一种良好早春花卉,其花姿优雅、花色艳丽、花期较长,是园林绿化、美化的良好材料。我国北方多为干旱、半干旱地区,且大部分地区水分供应不足,严重影响了城市园林植物的观赏特性、园林应用价值及正常养护,为此研究植物在干旱逆境中的生态适应性及其评价机制,对干旱地区植被恢复及改善城市生态环境具有重要意义。【前人研究进展】关于植物干旱胁迫研究亦相继展开,例如干旱胁迫会使植株叶片出现气孔闭合、光合作用减弱等反应,从而引发植物体在渗透调节、酶保护体系等方面的变化,使植物体内平衡的自由基稳态遭到破坏[1]。目前关于侧金盏花的研究主要集中在传粉特性[2]、基因获取[3]及药用研究[4]等方面。【本研究切入点】对侧金盏花生态适应性及园林应用方面研究较少,仅有少量的生理生化指标探究,目前缺少对侧金盏花系统的研究,其生理特性以及光合研究特性尚不明晰。【拟解决的关键问题】为此本研究通过盆栽控水试验,研究不同水分条件对侧金盏花形态、生理及光合特性的影响,旨在探讨侧金盏花的耐旱性,为今后侧金盏花的水分管理及栽培利用等方面提供理论依据。
1. 材料与方法
1.1 试验材料
试验材料为长白山野生侧金盏花植株,将引种后的侧金盏花植株移栽到塑料花盆中,每盆2株,花盆规格为盆高28 cm,上口径26 cm,下口径24 cm,栽培基质为园土∶草炭∶沙子为3∶2∶1的混合基质。每盆土质量为(1.8±0.2) kg,置于温室内生长,期间进行正常肥水管理。
1.2 试验方法
试验期间温室昼夜均温分别为23℃、12 ℃,平均相对湿度为37%。待叶片全部展开,选取长势一致、生长良好的植株进行干旱胁迫处理。试验设干旱(试验处理前充足灌水3 d使土壤水分饱和,使其自然干旱,停水0、4、8、12、16 d)、复水(干旱胁迫4、8、12、16 d后对植株进行复水)2个处理,以正常水分管理(70%±5%)为对照(CK)。分别在干旱处理0、4、8、12、16 d和复水处理4 d后进行观测,每个处理50盆,3次重复,相关指标测定均为3次重复。
1.3 测定项目
土壤相对含水量[5];株高、地上和地下部分干重、鲜重;复水后存活率[6](存活植株数量/总植株数量×100%);叶片相对含水量[7]。
生理指标:丙二醛(MDA)含量[5]、相对电导率[8]、脯氨酸(Pro)含量[9]、可溶性糖含量、可溶性蛋白含量、过氧化物酶(POD)活性[5]、超氧化物歧化酶(SOD)活性、叶绿素(Chl)总量[10]。
光合参数:选取晴朗无风的天气,使用CIRAS-2光合仪测定,测定指标为净光合速率(Pn)、蒸腾速率(Tr)、胞间二氧化碳浓度(Ci)、气孔导度(Gs)等光合参数;使用FmS2型脉冲调制式叶绿素荧光仪,测定侧金盏花叶片光适应下的最小荧光(Fo′)、最大荧光(Fm′)、稳态荧光(F′)和可变荧光(Fv′),再进行充分暗适应30 min以上,测定其暗适应下的初始荧光(Fo)、最大荧光(Fm)、可变荧光(Fv),并计算光系统Ⅱ(PSⅡ)最大光化学量子产量(Fv/Fm)、PSⅡ潜在活性(Fv/Fo)、PSⅡ实际光化学量子产量(ΦPSⅡ)、光化学猝灭系数(qP)、非光化学猝灭(NPQ)和表观光合电子传递速率(ETR)[11-13]等荧光参数。
1.4 统计方法
测定相关指标后,使用Excel 2010对数据进行整理,采用IBM SPSS 20.0进行数据统计分析。
2. 结果与分析
2.1 干旱胁迫下土壤相对含水量的动态变化
由表1可知,随胁迫时间的增加,土壤相对含水量逐渐下降,且干旱各处理差异显著(P<0.05),胁迫8 d后,土壤相对含水量均下降至30%以下,到16 d时仅为20.4%;复水后,干旱各处理均恢复到对照,但由于控水可能导致土壤结构改变,因此与对照略有差异。
表 1 侧金盏花不同水分状况土壤相对含水量的变化Table 1. Variation on relative moisture content of A. amurensis-growing soil under varied watering conditions胁迫时间
Stress time/d土壤相对含水量
Soil relative water content/%对照 CK 干旱 Drought 复水 Rewatering 0 71.60±2.34 a 71.85±1.16 a − 4 72.40±3.84 a 41.55±0.43 b 70.20±3.65 ab 8 71.57±1.43 a 29.90±1.35 c 72.67±2.52 a 12 69.93±1.37 a 23.88±2.14 d 67.37±1.26 b 16 68.83±5.08 a 20.40±2.58 e 72.10±0.85 a 注:表中数据为平均值±标准差,同列不同小写字母表明不同胁迫时间同一指标差异显著(P<0.05)。表2-3、5-13同。
Note: The data in the table are mean ± standard deviation, different lowercase letters in the same column indicate significant differences in the same index at different stress times (P<0.05). Same for Table 2-3 and Table 5-13.2.2 干旱胁迫及复水对侧金盏花生长的影响
由表2可知,侧金盏花地上及地下部分生物量随干旱胁迫程度的加大而明显下降,干旱4 d时,其地上及地下部分生物量下降较少,当干旱8、12和16 d,与干旱0 d相比,侧金盏花地上及地下部分鲜质量下降33.05%、37.32%、46.9%和21.8%、41.56%、44.18%,地上及地下干质量下降41.53%、47.43%、52.35%和31.3%、50.94%、60.72%,干旱12、16 d地上鲜质量差异显著(P <0.05),干旱8、12 d地下鲜质量具有显著差异(P <0.05)。
表 2 干旱胁迫下侧金盏花生物量的变化Table 2. Variation on biomass of A. amurensis grown under drought stress胁迫时间
Stresstime/d鲜质量 Fresh mass/g 干质量 Dry mass/g 地上部
Above ground根系
Root地上部
Above ground根系
Root0 2.3633±0.1025 a 9.3620±0.2114 a 0.4527±0.0029 a 3.4303±0.2112 a 4 1.8313±0.1517 b 7.5250±0.4040 b 0.4110±0.0035 a 2.5650±0.1758 b 8 1.5823±0.0609 c 7.3213±0.1550 b 0.2647±0.0040 b 2.3567±0.1503 b 12 1.4813±0.1183 c 5.4713±0.3208 c 0.2380±0.0030 b 1.4683±0.0336 c 16 1.2550±0.0960 d 5.2263±0.0970 c 0.2157±0.0095 b 1.3473±0.0481 c 由表3可知,当侧金盏花遭受干旱时,随土壤相对含水量的减少,其平均株高呈下降趋势。干旱0~8 d,株高降幅较明显,各处理差异达显著水平(P <0.05),恢复供水后,干旱4 d的株高有所增加,但仍显著低于对照(P <0.05),干旱8、12、16 d复水前后变化不显著(P >0.05)。
表 3 侧金盏花不同水分状况株高的变化Table 3. Variation on plant height of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d株高 plant height/cm 对照 CK 干旱 Drought 复水 Rewatering 0 9.17±0.76 e 9.37±0.65 a − 4 10.40±0.40 d 7.93±0.12 b 8.27±0.21 a 8 12.33±0.31 c 7.10±0.10 c 7.40±0.26 b 12 13.60±0.10 b 6.57±0.12 c 6.80±0.20 c 16 14.57±0.35 a 5.57±0.49 d 5.90±0.10 d 2.3 干旱胁迫及复水对侧金盏花形态及复水后存活率的影响
由表4可知,将侧金盏花进行不同程度胁迫处理,其地上部分形态变化主要表现为叶片下垂,边缘卷曲、皱缩和干枯。干旱4 d,叶片表现出轻微萎蔫现象,复水后,其外观形态恢复正常,成活率为100%;胁迫8 d,叶片皱缩并出现萎蔫下垂现象,复水后,外观基本恢复正常,仅茎尖处有少量枯黄萎蔫,复水后,成活率为100%;胁迫至12 d,叶片出现严重皱缩,萎蔫下垂,地上部分出现干枯现象,此时进行复水,部分植株可恢复生命力,成活率为50.67%;干旱16 d,大多数植株死亡,复水后成活率仅为6.35%。
表 4 侧金盏花不同干旱胁迫时间复水后存活率Table 4. Survival rate of Adonis amurensis after rehydration under different drought stress times胁迫时间
Stress time/d存活率
Survival rate/%胁迫时间
Stress time/d存活率
Survival rate/%0 100 12 50.67 4 100 16 6.35 8 100 2.4 干旱胁迫及复水对侧金盏花叶片相对含水量的影响
由表5可知,随干旱程度加深,侧金盏花叶片相对含水量逐渐下降,胁迫第16 d时达到最小值44.62%,比对照显著下降49.62%(P<0.05),干旱8、12 d,与对照相比,叶片相对含水量降低24.86%、42.73%,均显著低于对照和复水处理(P<0.05);复水后,叶片相对含水量均有不同程度的恢复。
表 5 侧金盏花不同水分状况叶片相对含水量的变化Table 5. Variation on leaf relative moisture content of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d叶片相对含水量 Leaf relative water content/% 对照 CK 干旱 Drought 复水 Rewatering 0 89.39±5.07a 86.28±3.61a − 4 86.37±4.61a 75.66±1.08b 79.58±3.51a 8 86.56±3.74a 65.04±4.50c 77.46±1.46a 12 90.35±5.45a 51.74±1.93d 63.76±0.92b 16 88.57±4.21a 44.62±2.87e 47.43±2.50c 2.5 干旱胁迫及复水对侧金盏花生理指标的影响
2.5.1 干旱胁迫及复水对侧金盏花叶绿素总量的影响
由表6可知,随干旱胁迫持续进行,侧金盏花叶片叶绿素总量呈下降趋势,胁迫8~16 d,各处理差异显著(P<0.05)。胁迫4 d,叶绿素总量比对照下降10.07%,显著低于对照(P<0.05);干旱8 d,较对照显著降低14.27%(P<0.05),干旱12、16 d,比对照分别降低25.85%、34.68%;干旱8、12、16 d复水后,叶绿素总量有所上升,比复水前分别上升8.7%、4.81%、4.3%。
表 6 侧金盏花不同水分状况叶绿素总量的变化Table 6. Variation on chlorophyll in leaves of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d叶绿素总含量 Chl content/(mg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 2.8348±0.0881 ab 2.7621±0.2360 a − 4 2.9203±0.1850 a 2.6263±0.1286 a 2.6423±0.0763 a 8 2.7347±0.1171 ab 2.3444±0.0331 b 2.5483±0.1659 a 12 2.6529±0.0455 b 1.9670±0.0992 c 2.0616±0.1215 b 16 2.6182±0.1058 b 1.7103±0.0827 d 1.7838±0.1070 c 2.5.2 干旱胁迫及复水对侧金盏花渗透调节物质含量的影响
不同水分处理下,侧金盏花Pro含量不同,由表7可知,干旱处理下,Pro含量呈先升后降趋势,各处理差异显著(P<0.05),干旱至12 d,Pro含量达最大值,干旱8、12、16 d分别比对照增加2.24、2.41、2.27倍,显著高于对照与复水处理(P<0.05);复水后,Pro含量有所下降,干旱4 d复水后其含量恢复至对照,干旱8、12、16 d复水后比干旱处理分别下降16.07%、19.22%、31.15%,表明侧金盏花细胞膜透性得到一定恢复,方差分析表明,干旱8、12、16 d复水后各处理差异显著(P<0.05)。
表 7 侧金盏花不同水分状况脯氨酸含量的变化Table 7. Variation of proline content in A. amurensis grown under varied watering conditions胁迫时间
Stress time/d脯氨酸含量 Proline content/(μg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 5.34±0.15 ab 4.34±0.13 e − 4 5.06±0.15 b 5.91±0.15 d 5.47±0.20 d 8 5.23±0.03 ab 16.93±0.99 c 14.21±0.34 b 12 5.79±0.26 a 19.72±0.11 a 15.93±0.95 a 16 5.64±0.70 ab 18.46±0.98 b 12.71±1.00 c 由表8可知,侧金盏花随干旱时间的增加,可溶性糖含量逐渐增大,干旱处理前12 d,各处理差异显著(P<0.05),干旱8、12、16 d比对照分别增加87.60%、100.48%、103.09%;复水后,可溶性糖含量下降,干旱4 d复水后略高于对照,表明质膜受伤害程度减少,胁迫12、16 d复水后,与干旱组相比,可溶性糖含量分别下降8.09%、8.19%。
表 8 侧金盏花不同水分状况可溶性糖含量的变化Table 8. Variation on soluble sugar content in A. amurensis grown under varied watering conditions胁迫时间
Stress time/d可溶性糖含量 Soluble sugar content/% 对照 CK 干旱 Drought 复水 Rewatering 0 3.69±0.15 b 3.81±0.12 d − 4 4.02±0.13 ab 5.44±0.16 c 4.65±0.14 c 8 3.87±0.17 ab 7.26±0.19 b 5.53±0.27 b 12 4.13±0.33 a 8.28±0.22 a 7.61±0.30 a 16 4.21±0.24 a 8.55±0.14 a 7.85±0.43 a 从表9可知,侧金盏花在干旱处理下,可溶性蛋白含量呈下降趋势。干旱16 d,可溶性蛋白含量最低,比对照下降78.15%,复水后其含量恢复至对照的37.86%,说明干旱使蛋白质合成受阻,植物受损严重,而复水使可溶性蛋白含量得到一定恢复。胁迫4 d复水后其可溶性蛋白含量与对照无显著差异(P >0.05),方差分析表明,胁迫12、16 d各处理差异显著(P <0.05)。
表 9 侧金盏花不同水分状况可溶性蛋白含量的变化Table 9. Variation on soluble protein content in A. amurensis grown under varied watering conditions胁迫时间
Stress time/d可溶性蛋白含量 Soluble protein content/(mg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 33.38±2.14 a 34.04±1.90 a − 4 26.49±1.31 c 24.30±1.28 b 28.33±1.94 a 8 27.76±0.56 bc 14.65±1.22 c 19.37±2.06 b 12 29.55±2.18 b 13.42±0.49 c 17.78±1.70 b 16 30.53±0.35 b 6.67±0.82 d 11.56±0.97 c 2.5.3 干旱胁迫及复水对侧金盏花MDA含量、叶片相对电导率的影响
由表10可知,随干旱程度增加,侧金盏花MDA含量逐渐升高,且各处理差异显著(P<0.05)。胁迫至16 d达到最大值,比对照增加2.59倍,显著高于对照与复水处理(P<0.05),复水过程中,MDA含量有所降低,干旱8 、12 d复水后差异显著(P<0.05),胁迫8 、12 、16 d复水后,MDA含量较干旱组分别下降12.31%、31.35%、36.62%,仍显著高于对照(P<0.05),干旱16 d复水后MDA含量为对照的2.28倍,表明干旱胁迫程度严重时,复水虽使MDA含量有所下降,但仍处于较高水平。
表 10 侧金盏花不同水分状况丙二醛含量的变化Table 10. Variation on malondialdehyde content in A. amurensis grown under varied watering conditions胁迫时间
Stress time/d丙二醛含量 Malondialdehyde content/(μmol·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 1.44±0.11 ab 1.60±0.10 e − 4 1.28±0.17 bc 2.27±0.12 d 1.68±0.14 c 8 1.23±0.10 c 3.33±0.25 c 2.92±0.27 b 12 1.22±0.07 c 4.53±0.18 b 3.11±0.07 b 16 1.55±0.06 a 5.57±0.31 a 3.53±0.18 a 由表11可知,在干旱胁迫下,侧金盏花叶片相对电导率逐渐增加,各处理差异达显著水平(P<0.05),与对照相比,干旱第8 、12 、16 d分别上升51.03%、102.04%和180.78%,均显著高于对照(P<0.05),第16 d时达到最大值;复水后,膜透性均有所恢复,干旱4 、8 d复水后叶片相对电导率略高于对照,干旱16 d复水后是对照的2.09倍,显著高于对照(P<0.05)。
表 11 侧金盏花不同水分状况相对电导率的变化Table 11. Variation on relative electric conductivity of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d相对电导率 Relative conductivity/% 对照 CK 干旱 Drought 复水 Rewatering 0 17.47±1.27 b 17.30±0.76 e − 4 18.17±1.26 b 22.33±0.59 d 21.30±0.61 d 8 19.40±0.78 ab 29.30±1.11 c 28.27±1.42 c 12 20.13±1.21 a 40.67±1.53 b 35.17±0.76 b 16 19.67±1.56 b 55.23±1.20 a 41.10±1.02 a 2.5.4 干旱胁迫及复水对侧金盏花抗氧化保护酶的影响
由表12所示,干旱处理下,POD活性高于对照和复水处理,呈先升后降趋势,各处理差异显著(P<0.05),侧金盏花植株受迫4~8 d时,POD活性上升,胁迫8 d时,比对照显著提高2.3倍,(P<0.05),胁迫12 ~16 d,其活性下降,比对照分别上升121.57%、56.42%,显著高于对照与复水处理(P<0.05);复水后,POD活性降低,各处理差异显著(P<0.05),干旱4 d复水后其活性与对照相比无显著差异(P>0.05),胁迫8、12、16 d复水后,POD活性较复水前分别下降23.60%、25.85%和13.57%,仍显著高于对照(P<0.05)。
表 12 侧金盏花不同水分状况过氧化物酶活性的变化Table 12. Variation on peroxidase activity of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d过氧化物酶活性 POD activity/(U·g−1min−1) 对照 CK 干旱 Drought 复水 Rewatering 0 226.74±11.68 a 214.72±16.15 e − 4 236.08±10.49 a 258.73±16.68 d 253.45±6.08 d 8 234.72±9.14 a 773.43±30.40 a 590.88±26.36 a 12 246.77±6.15 a 546.76±22.93 b 405.45±28.57 b 16 238.74±18.82 a 373.43±23.33 c 322.74±18.05 c 由表13可知,随胁迫程度加大,侧金盏花SOD活性呈先升后降趋势,胁迫0~4 d SOD活性上升趋势不明显,说明前期侧金盏花可通过调节SOD活性来平衡活性氧代谢、保护膜结构,对外界不良环境进行抵御,胁迫12 d达到最大值,比对照显著增加58.31%(P<0.05);复水后SOD活性下降,干旱4 d复水后略高于对照,胁迫12、16 d复水后其活性较复水前下降23.75%、15.11%。
表 13 侧金盏花不同水分状况超氧化物歧化酶活性的变化Table 13. Variation on superoxide dismutase activity of A. amurensis grown under varied watering conditions胁迫时间
Stress time/d超氧化物歧化酶活性 SOD activity/(U·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 315.98±10.21 c 322.23±19.77 d − 4 310.21±9.54 b 360.50±10.00 c 358.78±7.57 b 8 314.66±9.72 b 410.12±8.22 a 370.87±8.37 b 12 322.73±10.35 a 510.92±6.14 b 389.59±5.80 a 16 329.50±5.00 a 435.35±4.45 c 369.56±7.71 b 2.6 干旱胁迫及复水对侧金盏花叶片光合参数的影响
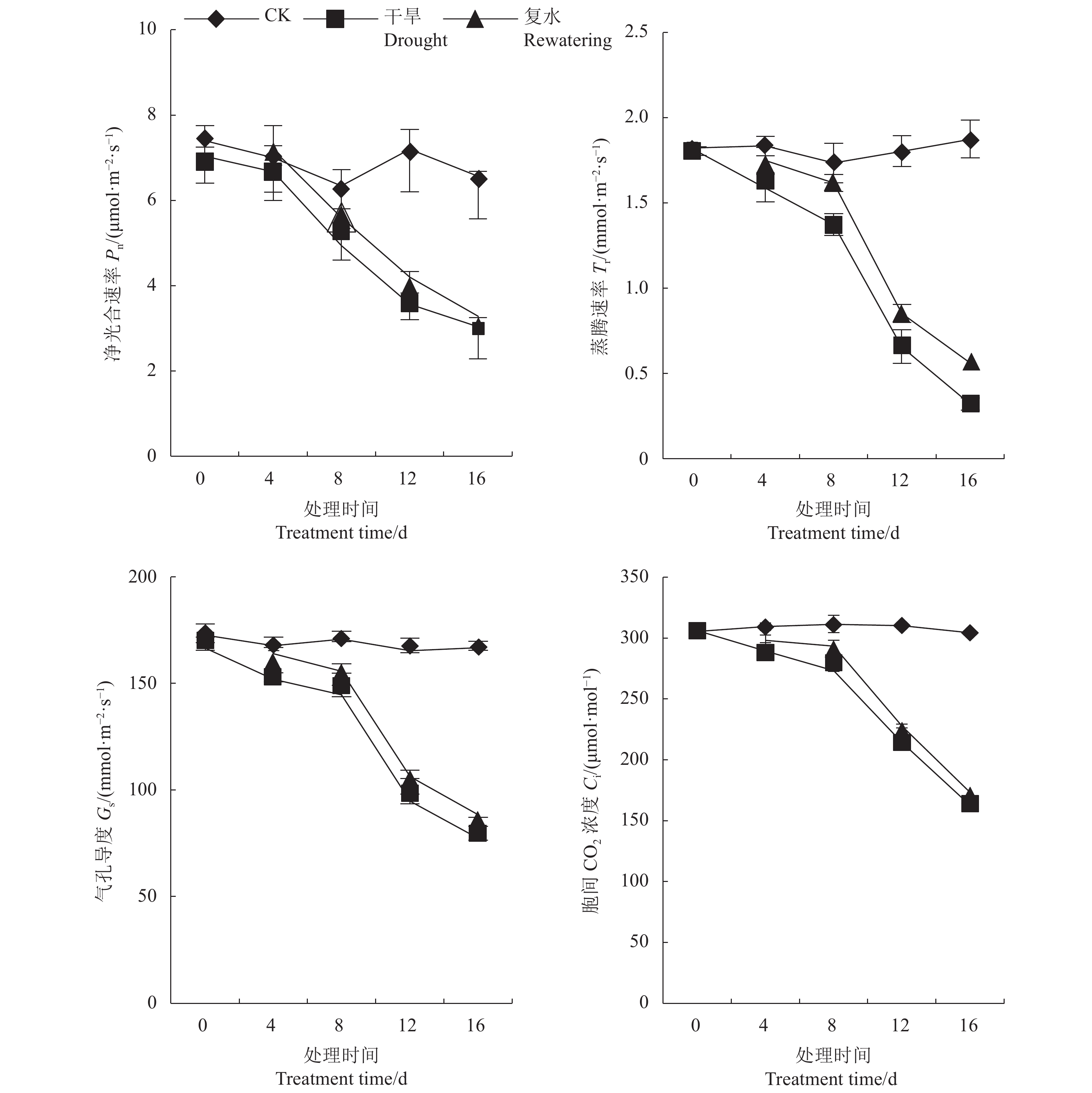
由图1可知,侧金盏花叶片Pn、Tr、Gs、Ci随着干旱胁迫时间的延长逐渐降低。胁迫8、12、16 d,与对照相比,Pn分别下降22.11%、50.46%、53.81%,干旱12、16 d复水后,Pn较干旱处理分别上升17.76%、8.24%;胁迫8、12和16 d,Tr较对照分别下降20.77%、63.58%、82.92%,复水后Tr有所恢复;干旱8、12和16 d时,Gs较对照分别下降15.23%、42.74%、53.6%,复水后,Gs较复水前分别上升7.6%、12.32%、14.22%,说明复水可使植物得到一定的缓解;胁迫8、12 d,Ci较对照下降12.21%、30.89%,较复水前分别上升7.32%、6.15%。
2.7 干旱胁迫及复水对侧金盏花叶片荧光参数的影响
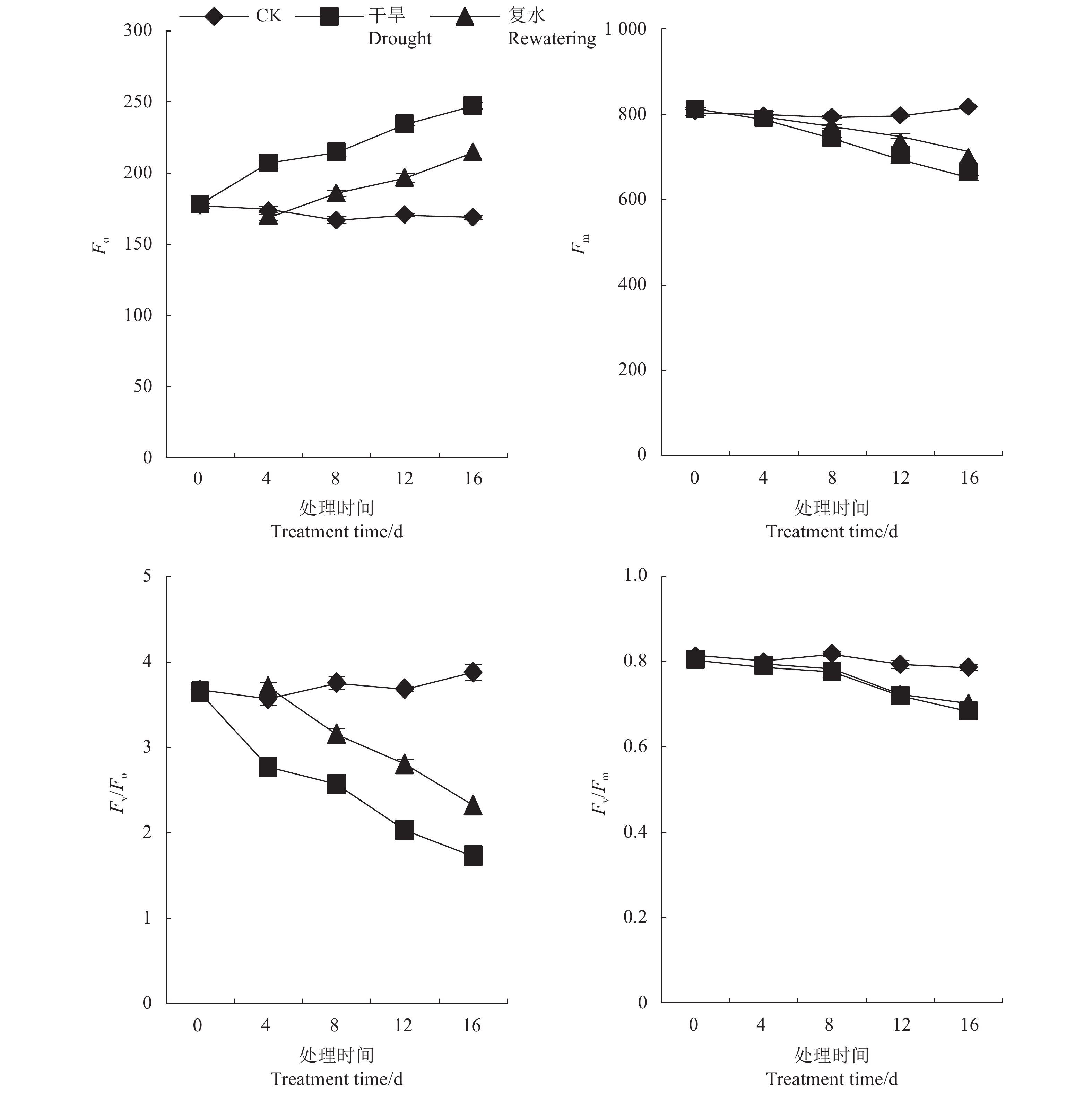
从图2可知,干旱处理下,侧金盏花叶片Fo上升,Fm下降。胁迫8、12、16 d,Fo较对照上升28.67%、37.47%、46.44%;胁迫8、12、16 d,Fm比对照分别下降6.35%、12.93%、20.2%。Fv/Fo、Fv/Fm随胁迫程度加深均表现出下降趋势。干旱8、12 d,Fv/Fo比对照下降31.57%、44.97%,胁迫16 d,较对照下降57.56%,复水后,其值有所上升;胁迫4 d,与对照相比,Fv/Fm下降不明显,胁迫8~16 d,较对照分别下降5.1%、9.37%、13.03%,复水过程中,其值有所上升,干旱4 d复水后Fv/Fm恢复至对照。
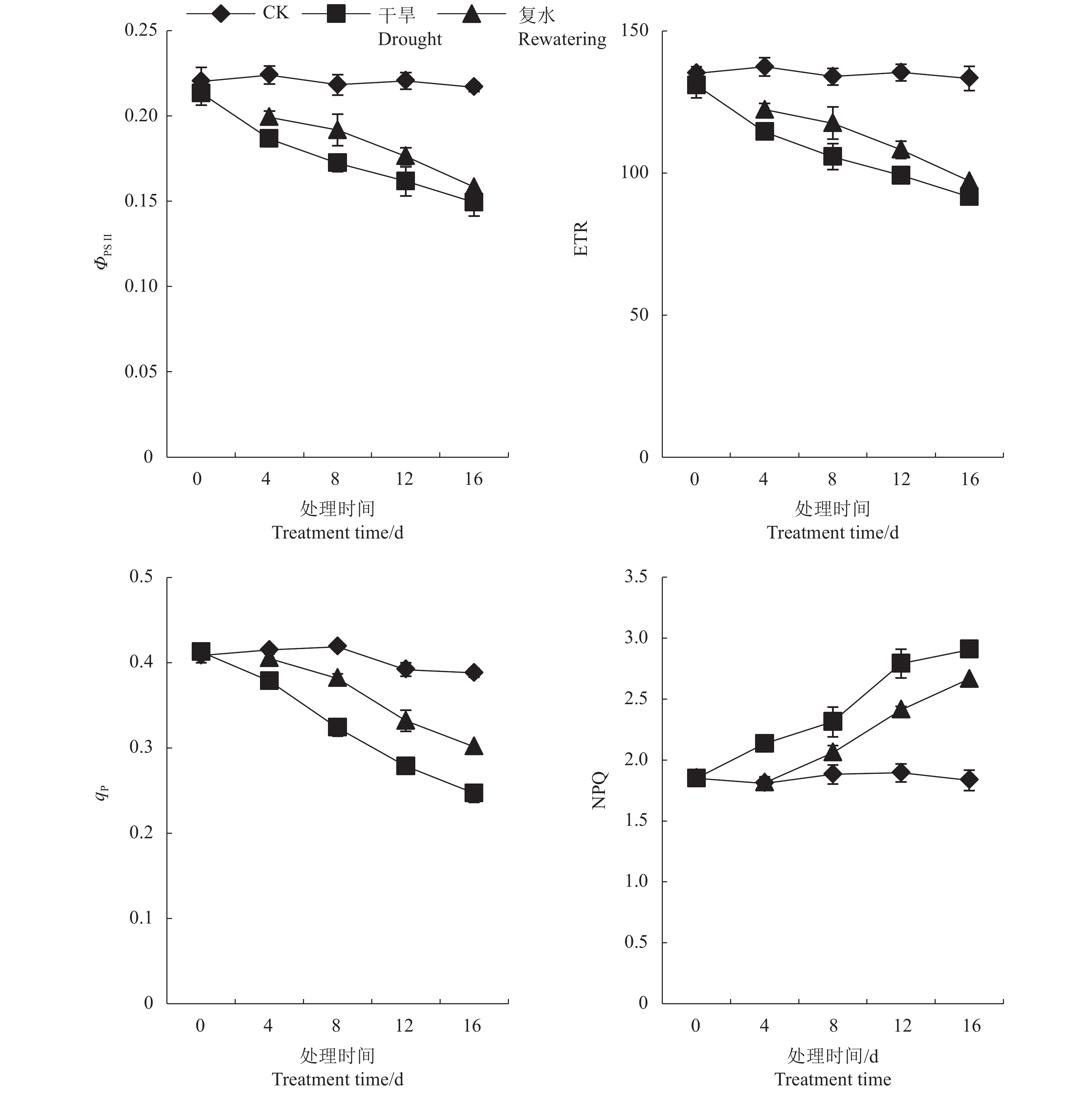
图3表明,干旱胁迫下,各处理ΦPSⅡ、ETR下降。干旱12、16 d,ΦPSⅡ比对照分别下降26.73%、31.2%,均显著低于对照(P<0.05),复水后,其值均增加;胁迫16 d时,ETR值最小,比对照下降31.29%,复水后,其值上升,较复水前升高6.03%。胁迫过程中,qP呈下降趋势,NPQ逐渐上升,干旱4~8 d,qP比对照降低8.76%、22.7%,胁迫12~16 d,qP值下降较快,比对照显著下降28.93%、36.38%(P<0.05);干旱至16 d,NPQ值最大,比对照显著上升58.44%(P<0.05)。复水后,qP、NPQ均有所恢复。
3. 讨论与结论
干旱胁迫下,侧金盏花的正常生命活动受到抑制。徐苏男等[14]认为,干旱使植物生长缓慢,其干物质量减少,本研究与之结果一致;相关研究表明,复水后成活率和叶片相对含水量是衡量植物脱水耐受性的有效指标[15-16],叶片相对含水量呈下降趋势;叶绿素是光能吸收的主要物质,直接影响植物光合作用[17]。本研究中,叶绿素总量不断降低,可能与植物自身生物学特性等因素有关[18]。
前人研究表明[19-21],渗透调节物质的积累是植物适应干旱胁迫的机制之一,干旱处理下,Pro和可溶性糖含量持续升高,可溶性蛋白含量先上升后下降,本研究与之略有差异,胁迫12 ~16 d时,脯氨酸含量下降,可能是因植物受害严重,导致机能紊乱;可溶性糖含量在干旱16 d达到最大值,表明植物叶片受害程度严重,复水后,其含量下降不明显,说明即使胁迫解除,短期内也未能恢复;可溶性蛋白含量在干旱期间持续下降,复水后有所回升,表明此时植物合成可溶性蛋白的能力增加。由此可知,不同植物在干旱胁迫下其渗透调节物质变化有所不同。
MDA和叶片相对电导率可体现干旱胁迫程度,是植物鉴定耐旱性的重要生理指标[22-23]。本研究中,干旱程度越重,MDA含量和叶片相对电导率越高,说明胁迫时间越长,侧金盏花质膜透性变大,细胞膜功能减弱,这与前人[24-25]研究结果一致。POD、SOD是植物体内的重要保护酶,可缓解脂质过氧化物积累而引起的细胞伤害[26]。本试验中,POD活性在第8 d达到峰值,胁迫0~12 d,SOD活性不断上升,表明此时植物通过增强保护酶活性来清除活性氧自由基,从而维持细胞膜的稳定性和完整性,这与崔颖等[27]研究结果相似。
植物在干旱处理下,叶片Pn、Gs、Ci和Tr在不同时期呈现不同变化。Farguhar[28]认为Pn、Gs和Ci变化一致时,Pn变化是由Gs引起,反之Pn的变化是由叶肉细胞活性决定的。本试验中,侧金盏花叶片Pn与Gs、Ci均下降,变化规律相同,胁迫12~16 d Pn恢复不明显,推测可能是植物受到严重胁迫后对光系统的伤害程度较大,这与张林春等[29]研究结果相似。此外,植物通过减小气孔开度使Tr降低,这也是植物一种抗旱机制[30]。本试验中,Tr逐渐下降,类似的研究结果也出现在葡萄等植物上[31]。
叶绿素荧光可检测植株在逆境条件下光合作用的真实行为。Fo是PSII反应中心完全开放状态时的荧光强度[32]。本研究中,侧金盏花叶片Fo增加量与受损程度成正比,表明PSII反应中心遭到破坏。前人研究表明[33],Fm、Fv/Fo、Fv/Fm是植物抗旱性主要指标,本研究中,均呈下降趋势,引起其降低的原因是叶片PSⅡ质子醌库(PQ库)容量变小,这与康红梅等[34]研究结果一致;随干旱胁迫加剧,qP、NPQ呈相反趋势,复水后,qP升高,NPQ下降,表明光合电子传递得以恢复,植物通过调整NPQ使其对自身光合结构起保护作用,这与Fernandez等[35]在苹果幼树的研究结果相似。ETR的高低在一定程度上反映了PSⅡ反应中心的电子捕获效率的高低[36],本试验中,ETR和ФPSⅡ变化与qP一致,均逐渐减小,ФPSⅡ、qP和ETR显著下降说明干旱减弱QA的氧化能力及PSII的电子传递能力,导致碳同化降低,光合系统受损。
综上可知,当土壤相对含水量低于29.9%,各项指标变化显著,侧金盏花生长受到明显抑制;干旱不超过8 d时进行复水,各指标恢复效果明显,干旱8 d后复水,各指标较对照相比有显著差异。综合分析得出侧金盏花可承受持续8 d(土壤相对含水量为29.9%)的干旱胁迫,因此,侧金盏花在养护管理时,在持续时间低于8 d,土壤相对含水量不低于29.9%时的短期土壤失水时,应及时复水救苗,持续干旱8 d后,土壤相对含水量低于29.9%时,对侧金盏花造成不可逆的伤害。
-
表 1 侧金盏花不同水分状况土壤相对含水量的变化
Table 1 Variation on relative moisture content of A. amurensis-growing soil under varied watering conditions
胁迫时间
Stress time/d土壤相对含水量
Soil relative water content/%对照 CK 干旱 Drought 复水 Rewatering 0 71.60±2.34 a 71.85±1.16 a − 4 72.40±3.84 a 41.55±0.43 b 70.20±3.65 ab 8 71.57±1.43 a 29.90±1.35 c 72.67±2.52 a 12 69.93±1.37 a 23.88±2.14 d 67.37±1.26 b 16 68.83±5.08 a 20.40±2.58 e 72.10±0.85 a 注:表中数据为平均值±标准差,同列不同小写字母表明不同胁迫时间同一指标差异显著(P<0.05)。表2-3、5-13同。
Note: The data in the table are mean ± standard deviation, different lowercase letters in the same column indicate significant differences in the same index at different stress times (P<0.05). Same for Table 2-3 and Table 5-13.表 2 干旱胁迫下侧金盏花生物量的变化
Table 2 Variation on biomass of A. amurensis grown under drought stress
胁迫时间
Stresstime/d鲜质量 Fresh mass/g 干质量 Dry mass/g 地上部
Above ground根系
Root地上部
Above ground根系
Root0 2.3633±0.1025 a 9.3620±0.2114 a 0.4527±0.0029 a 3.4303±0.2112 a 4 1.8313±0.1517 b 7.5250±0.4040 b 0.4110±0.0035 a 2.5650±0.1758 b 8 1.5823±0.0609 c 7.3213±0.1550 b 0.2647±0.0040 b 2.3567±0.1503 b 12 1.4813±0.1183 c 5.4713±0.3208 c 0.2380±0.0030 b 1.4683±0.0336 c 16 1.2550±0.0960 d 5.2263±0.0970 c 0.2157±0.0095 b 1.3473±0.0481 c 表 3 侧金盏花不同水分状况株高的变化
Table 3 Variation on plant height of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d株高 plant height/cm 对照 CK 干旱 Drought 复水 Rewatering 0 9.17±0.76 e 9.37±0.65 a − 4 10.40±0.40 d 7.93±0.12 b 8.27±0.21 a 8 12.33±0.31 c 7.10±0.10 c 7.40±0.26 b 12 13.60±0.10 b 6.57±0.12 c 6.80±0.20 c 16 14.57±0.35 a 5.57±0.49 d 5.90±0.10 d 表 4 侧金盏花不同干旱胁迫时间复水后存活率
Table 4 Survival rate of Adonis amurensis after rehydration under different drought stress times
胁迫时间
Stress time/d存活率
Survival rate/%胁迫时间
Stress time/d存活率
Survival rate/%0 100 12 50.67 4 100 16 6.35 8 100 表 5 侧金盏花不同水分状况叶片相对含水量的变化
Table 5 Variation on leaf relative moisture content of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d叶片相对含水量 Leaf relative water content/% 对照 CK 干旱 Drought 复水 Rewatering 0 89.39±5.07a 86.28±3.61a − 4 86.37±4.61a 75.66±1.08b 79.58±3.51a 8 86.56±3.74a 65.04±4.50c 77.46±1.46a 12 90.35±5.45a 51.74±1.93d 63.76±0.92b 16 88.57±4.21a 44.62±2.87e 47.43±2.50c 表 6 侧金盏花不同水分状况叶绿素总量的变化
Table 6 Variation on chlorophyll in leaves of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d叶绿素总含量 Chl content/(mg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 2.8348±0.0881 ab 2.7621±0.2360 a − 4 2.9203±0.1850 a 2.6263±0.1286 a 2.6423±0.0763 a 8 2.7347±0.1171 ab 2.3444±0.0331 b 2.5483±0.1659 a 12 2.6529±0.0455 b 1.9670±0.0992 c 2.0616±0.1215 b 16 2.6182±0.1058 b 1.7103±0.0827 d 1.7838±0.1070 c 表 7 侧金盏花不同水分状况脯氨酸含量的变化
Table 7 Variation of proline content in A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d脯氨酸含量 Proline content/(μg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 5.34±0.15 ab 4.34±0.13 e − 4 5.06±0.15 b 5.91±0.15 d 5.47±0.20 d 8 5.23±0.03 ab 16.93±0.99 c 14.21±0.34 b 12 5.79±0.26 a 19.72±0.11 a 15.93±0.95 a 16 5.64±0.70 ab 18.46±0.98 b 12.71±1.00 c 表 8 侧金盏花不同水分状况可溶性糖含量的变化
Table 8 Variation on soluble sugar content in A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d可溶性糖含量 Soluble sugar content/% 对照 CK 干旱 Drought 复水 Rewatering 0 3.69±0.15 b 3.81±0.12 d − 4 4.02±0.13 ab 5.44±0.16 c 4.65±0.14 c 8 3.87±0.17 ab 7.26±0.19 b 5.53±0.27 b 12 4.13±0.33 a 8.28±0.22 a 7.61±0.30 a 16 4.21±0.24 a 8.55±0.14 a 7.85±0.43 a 表 9 侧金盏花不同水分状况可溶性蛋白含量的变化
Table 9 Variation on soluble protein content in A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d可溶性蛋白含量 Soluble protein content/(mg·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 33.38±2.14 a 34.04±1.90 a − 4 26.49±1.31 c 24.30±1.28 b 28.33±1.94 a 8 27.76±0.56 bc 14.65±1.22 c 19.37±2.06 b 12 29.55±2.18 b 13.42±0.49 c 17.78±1.70 b 16 30.53±0.35 b 6.67±0.82 d 11.56±0.97 c 表 10 侧金盏花不同水分状况丙二醛含量的变化
Table 10 Variation on malondialdehyde content in A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d丙二醛含量 Malondialdehyde content/(μmol·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 1.44±0.11 ab 1.60±0.10 e − 4 1.28±0.17 bc 2.27±0.12 d 1.68±0.14 c 8 1.23±0.10 c 3.33±0.25 c 2.92±0.27 b 12 1.22±0.07 c 4.53±0.18 b 3.11±0.07 b 16 1.55±0.06 a 5.57±0.31 a 3.53±0.18 a 表 11 侧金盏花不同水分状况相对电导率的变化
Table 11 Variation on relative electric conductivity of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d相对电导率 Relative conductivity/% 对照 CK 干旱 Drought 复水 Rewatering 0 17.47±1.27 b 17.30±0.76 e − 4 18.17±1.26 b 22.33±0.59 d 21.30±0.61 d 8 19.40±0.78 ab 29.30±1.11 c 28.27±1.42 c 12 20.13±1.21 a 40.67±1.53 b 35.17±0.76 b 16 19.67±1.56 b 55.23±1.20 a 41.10±1.02 a 表 12 侧金盏花不同水分状况过氧化物酶活性的变化
Table 12 Variation on peroxidase activity of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d过氧化物酶活性 POD activity/(U·g−1min−1) 对照 CK 干旱 Drought 复水 Rewatering 0 226.74±11.68 a 214.72±16.15 e − 4 236.08±10.49 a 258.73±16.68 d 253.45±6.08 d 8 234.72±9.14 a 773.43±30.40 a 590.88±26.36 a 12 246.77±6.15 a 546.76±22.93 b 405.45±28.57 b 16 238.74±18.82 a 373.43±23.33 c 322.74±18.05 c 表 13 侧金盏花不同水分状况超氧化物歧化酶活性的变化
Table 13 Variation on superoxide dismutase activity of A. amurensis grown under varied watering conditions
胁迫时间
Stress time/d超氧化物歧化酶活性 SOD activity/(U·g−1) 对照 CK 干旱 Drought 复水 Rewatering 0 315.98±10.21 c 322.23±19.77 d − 4 310.21±9.54 b 360.50±10.00 c 358.78±7.57 b 8 314.66±9.72 b 410.12±8.22 a 370.87±8.37 b 12 322.73±10.35 a 510.92±6.14 b 389.59±5.80 a 16 329.50±5.00 a 435.35±4.45 c 369.56±7.71 b -
[1] SALEHI S P, IZADPANAH M, FALAH H L, et al. Comparison of the effects of drought stress on pigments, peroxidase, osmotic adjustment and antioxidant enzymes in different accessions of anthemistinctoria and tripleurospermumservanes of natural resources gene bank of iran [J]. En Journals, 2015: 126−139.
[2] 何淼, 陈士惠, 马翠青, 等. 野生及引种侧金盏花的开花物候与传粉特性 [J]. 草业科学, 2014, 31(3):431−437. DOI: 10.11829/j.issn.1001-0629.2013-0209 HE M, CHEN S H, MA C Q, et al. Flowering phenology and pollination charateristic of Adonis amurensis [J]. Pratacultural Science, 2014, 31(3): 431−437.(in Chinese) DOI: 10.11829/j.issn.1001-0629.2013-0209
[3] 宁波. RACE法获取顶冰花CBF1基因及其抗冻性质研究[D]. 长春: 吉林大学, 2008. NING B. Research of Adonis CBF1by SMART RACE and Realtime PCR[D]. ChangChun: Jilin University, 2008.
[4] 王乐忠, 刘鸣远. 东北侧金盏花属的研究 [J]. 植物研究, 1988, 8(2):49−53. WANG Y Z, LIU M Y. Studies on the genus Adonis in northeast China [J]. Bulletin of Botanical Research, 1988, 8(2): 49−53.(in Chinese)
[5] 张治安, 陈展宇. 植物生理学实验技术[M]. 长春: 吉林大学出版社, 2008. [6] 王骞春, 陆爱君, 冯健, 等. 干旱胁迫对日本落叶松生理指标的影响 [J]. 东北林业大学学报, 2016, 44(8):13−17, 40. DOI: 10.3969/j.issn.1000-5382.2016.08.003 WANG Q C, LU A J, FENG J, et al. Effects of drought stress on physiological indices of Japanese larch [J]. Journal of Northeast Forestry University, 2016, 44(8): 13−17, 40.(in Chinese) DOI: 10.3969/j.issn.1000-5382.2016.08.003
[7] LI H. Principles and techniques of plant physiological and biochemical experiments[M]. Beijing: Higher Education Press, 2003: 191-205.
[8] HAO Z. Plant physiological experiments[M]. Harbin: Harbin Institute of Technology Press, 2004.
[9] BATES L S, WALDREN R D, TEARE I D. Rapid determination of free proline for drought studies [J]. Plant Soil, 1973, 39: 205−207. DOI: 10.1007/BF00018060
[10] GAO J. Instruction for plant physiology experiments[M]. Beijing: Higher Education Press, 2006: 211-214.
[11] BILGER W, BJÖRKMAN O. Role of the xanthophyll cycle in photoprotection elucidated by measurements of light-induced absorbance changes, fluorescence and photosynthesis in leaves of Hedera canariensis [J]. Photosynthesis Research, 1990, 25(3): 173−185. DOI: 10.1007/BF00033159
[12] 黄有总, 张国平. 叶绿素荧光测定技术在麦类作物耐盐性鉴定中的应用 [J]. 麦类作物学报, 2004, 24(3):114−116. DOI: 10.3969/j.issn.1009-1041.2004.03.029 HUANG Y Z, ZHANG G P. Application of measuring chlorophyll fluorescence in identification of salinity tolerance in triticeae crops [J]. Journal of Triticeae Crops, 2004, 24(3): 114−116.(in Chinese) DOI: 10.3969/j.issn.1009-1041.2004.03.029
[13] 谢志玉, 张文辉. 干旱和复水对文冠果生长及生理生态特性的影响 [J]. 应用生态学报, 2018, 29(6):1759−1767. XIE Z Y, ZHANG W H. Effects of drought and rewatering on growth and photosynthetic physioecological characteristics of Xanthoceras sorbifolia [J]. Chinese Journal of Applied Ecology, 2018, 29(6): 1759−1767.(in Chinese)
[14] 徐苏男. 水分胁迫及复水对结缕草生长生理和光合荧光特性的影响[D]. 沈阳: 辽宁大学, 2012. XUE S N. Effects of water stress and rewatering on physiological and photosynthetic chlorophyll fluorescence characteristics of Zoysiajaponica[D]. Shenyang: Liaoning University, 2012.
[15] 雷蕾. 黄连花开花生物学和抗旱、抗盐碱研究[D]. 哈尔滨: 东北林业大学, 2017. LEI L. The study on flowering biology and drought and salt resistance of Lysimachiadavurica[D]. Harbin: Northeast Forestry University, 2017.
[16] ANJUM S A, XIE X Y, WANG L C, et al. Morphological, physiological and biochemical responses of plants to drought stress [J]. Afr. J. Agric. Res, 2011, 6(9): 2026−2032.
[17] 毛伟, 李玉霖, 赵学勇, 等. 3种藜科植物叶特性因子对土壤养分、水分及种群密度的响应 [J]. 中国沙漠, 2009, 29(3):468−473. MAO W, LI Y L, ZHAO X Y, et al. Respondence of leaf traits of three Chenopodiaceae plants to soil nutrients, water content and plant density [J]. Journal of Desert Research, 2009, 29(3): 468−473.(in Chinese)
[18] 李芳兰, 包维楷, 吴宁. 白刺花幼苗对不同强度干旱胁迫的形态与生理响应 [J]. 生态学报, 2009, 29(10):5406−5416. DOI: 10.3321/j.issn:1000-0933.2009.10.027 LI F L, BAO W K, WU N. Morphological and physiological responses of current Sophora davidii seedlings to drought stress [J]. Acta Ecologica Sinica, 2009, 29(10): 5406−5416.(in Chinese) DOI: 10.3321/j.issn:1000-0933.2009.10.027
[19] WU S W, HU C X, TAN Q L, et al. Effects of molybdenum on water utilization, antioxidative defense system and osmotic-adjustment ability in winter wheat (Triticum aestivum) under drought stress [J]. Plant Physiology and Biochemistry, 2014, 83: 365−374. DOI: 10.1016/j.plaphy.2014.08.022
[20] GAO S S, et al. Effects of drought stress on growth, physiology and secondary metabolites of Two Adonis species in Northeast China [J]. Scientia Horticulturae, 2020: 259.
[21] 季杨, 张新全, 彭燕, 等. 干旱胁迫对鸭茅根、叶保护酶活性、渗透物质含量及膜质过氧化作用的影响 [J]. 草业学报, 2014, 23(3):144−151. DOI: 10.11686/cyxb20140316 JI Y, ZHANG X Q, PENG Y, et al. Effects of drought stress on lipid peroxidation, osmotic adjustment and activities of protective enzymes in the roots and leaves of orchardgrass [J]. Acta Prataculturae Sinica, 2014, 23(3): 144−151.(in Chinese) DOI: 10.11686/cyxb20140316
[22] 王洪瑞, 敖红. 干旱胁迫对红皮云杉和嫩江云杉渗透调节及抗氧化系统的影响 [J]. 东北林业大学学报, 2020, 48(8):16−21, 32. DOI: 10.3969/j.issn.1000-5382.2020.08.004 WANG H R, AO H. Response of osmotic regulation and antioxidant system to drought stress in Korean spruce and Nenjiang spruce [J]. Journal of Northeast Forestry University, 2020, 48(8): 16−21, 32.(in Chinese) DOI: 10.3969/j.issn.1000-5382.2020.08.004
[23] 周静, 汪天, 崔键, 等. 红壤水分条件对柑橘叶片质膜透性以及活性氧代谢和保护酶活性的影响 [J]. 土壤, 2009, 41(2):236−242. DOI: 10.3321/j.issn:0253-9829.2009.02.015 ZHOU J, WANG T, CUI J, et al. Effects of red soil moisture on content of reactive oxygen species and activities of protective enzymes of Citrus (Citrus unshiu Marc.)leaves [J]. Soils, 2009, 41(2): 236−242.(in Chinese) DOI: 10.3321/j.issn:0253-9829.2009.02.015
[24] 李文鹤. 干旱胁迫对野菊生理特性的影响[D]. 哈尔滨: 东北林业大学, 2011. LI W H. Effects on physiological characteristics of Dendrathema indicum L. under drought stress[D]. Harbin: Northeast Forestry University, 2011.
[25] 李博. 水分胁迫对大花飞燕草种子萌发及幼苗生理特性的影响[D]. 哈尔滨: 东北林业大学, 2011. LI B. Effects on seed germination and physiological reaction of Delphinium grandiflorum seedlings under water stress[D]. Harbin: Northeast Forestry University, 2011.
[26] PENG M, KUC J. Peroxidase generated hydrogen peroxide as asource of antifungal activity in vitro and on tobacco leaf disks [J]. Physiology and Biochemistry, 1992, 82: 696−699.
[27] 崔颖, 李芊夏, 刘彬, 等. 干旱胁迫对地果幼苗形态与生理特性的影响 [J]. 西北林学院学报, 2020, 35(6):82−88, 227. DOI: 10.3969/j.issn.1001-7461.2020.06.11 CUI Y, LI Q X, LIU B, et al. Effects of drought stress on morphology and physiological characteristics of Ficus tikoua seedlings [J]. Journal of Northwest Forestry University, 2020, 35(6): 82−88, 227.(in Chinese) DOI: 10.3969/j.issn.1001-7461.2020.06.11
[28] FARQUHAR G D, EHLERINGER J R, HUBICK K T. Carbon isotope discrimination and photosynthesis [J]. Annual Review of Plant Physiology and Plant Molecular Biology, 1989, 40: 503−537. DOI: 10.1146/annurev.pp.40.060189.002443
[29] 张林春, 郝扬, 张仁和, 等. 干旱及复水对不同抗旱性玉米光合特性的影响 [J]. 西北农业学报, 2010, 19(5):76−80. DOI: 10.3969/j.issn.1004-1389.2010.05.017 ZHANG L C, HAO Y, ZHANG R H, et al. Response of drought and rewatering to leaf photosynthetic characteristics in different maize varieties [J]. Acta Agriculturae Boreali-Occidentalis Sinica, 2010, 19(5): 76−80.(in Chinese) DOI: 10.3969/j.issn.1004-1389.2010.05.017
[30] STEDUTO P, KATERJI N, PUERTOS M H, et al. Water use efficiency of sweet sorghum under water stress conditions: gas exchange investigations at leaf and canopy scales [J]. Field Crops Research, 1997, 54(2): 221−234.
[31] 李敏敏, 袁军伟, 韩斌, 等. 干旱和复水对两种葡萄砧木叶片光合和叶绿素荧光特性的影响 [J]. 干旱地区农业研究, 2019, 37(1):221−226. DOI: 10.7606/j.issn.1000-7601.2019.01.31 LI M M, YUAN J W, HAN B, et al. Effect of drought and rewatering on the photosynthesis and chlorophyll fluorescence of two grape rootstock leaves [J]. Agricultural Research in the Arid Areas, 2019, 37(1): 221−226.(in Chinese) DOI: 10.7606/j.issn.1000-7601.2019.01.31
[32] LI X, FENG W, ZENG X C. Advances in chlorophyll fluorescence analysis and its uses [J]. Acta Botanica Boreali Occidentalia Sinica, 2006, 26(10): 2186−2196.
[33] MATHOBO R, MARAIS D, STEYN J M. The effect of drought stress on yield, leaf gaseous exchange and chlorophyll fluorescence of dry beans(Phaseolus vulgaris) [J]. Agricultural Water Management, 2017, 18: 118−125.
[34] 康红梅, 刘琛彬, 薄伟, 等. 干旱胁迫对4种地被植物水分生理和叶绿素荧光参数的影响 [J]. 山西农业科学, 2020, 48(11):1767−1771. DOI: 10.3969/j.issn.1002-2481.2020.11.15 KANG H M, LIU C B, BO W, et al. Effect of drought stress on the leaf water physiology and chlorophyll fluorescence of four ground cover plants [J]. Journal of Shanxi Agricultural Sciences, 2020, 48(11): 1767−1771.(in Chinese) DOI: 10.3969/j.issn.1002-2481.2020.11.15
[35] FERNANDEZ R T, PERRY R L, FLORE J A. Drought response of young apple trees on three rootstocks. II. Gas exchange, chlorophyll fluorescence, water relations, and leaf abscisic acid [J]. Journal of the American Society for Horticultural Science, 1997, 122: 841−848. DOI: 10.21273/JASHS.122.6.841
[36] SUN J K, ZHANG W H, LU Z H, et al. Chlorophyll fluorescence characteristics of Elaeagnusangustifolia L. and Grewia biloba G. Don var. parviflora(Bge.)Hand. Mazz. Seedlings under drought stress [J]. Bulletin of Botanical Research, 2009, 29(2): 216−223.
-
期刊类型引用(7)
1. 戚金存,刘大泉,刘泓,金鑫,陈明婉,吕猛,杨福孙,李昌珍. 干旱胁迫及复水对槟榔幼苗形态和生理特性的影响. 江苏农业学报. 2024(04): 615-624 .  百度学术
百度学术
2. 何淼,张紫馥,臧帅彤,尹雪,孟儒,孙颖. 辽吉侧金盏花的开花特性和繁育系统. 东北林业大学学报. 2023(03): 54-59 .  百度学术
百度学术
3. 赵英,赵凯丽,朱宇林,仇明月,任琪,吴敏. 干旱胁迫与复水对喀斯特地区红背山麻杆生长及生理特性的影响. 西北农林科技大学学报(自然科学版). 2023(08): 59-68 .  百度学术
百度学术
4. 刘志强,王建立,赵景云,仇永康. 花期干旱对大豆生理及光合特性的影响. 热带农业科学. 2022(01): 17-21 .  百度学术
百度学术
5. 陈玮婷,夏朝水,陈昌铭,廖巧玲,曹奕鸯,陈仕朋,郭芸玮. 印度梨形孢对非洲菊幼苗生长及抗旱性的影响. 西北农林科技大学学报(自然科学版). 2022(09): 53-61 .  百度学术
百度学术
6. 马建蓉,朱玉雪,朱永娟,梅艳桃,马国花,郭晓农. 干旱胁迫对藜麦幼苗生长及生理的影响. 大麦与谷类科学. 2022(04): 14-20+26 .  百度学术
百度学术
7. 丁久玲,孟海涛,郑凯. 10个空气凤梨品种对干旱胁迫的生理响应及抗旱性评价. 浙江农业科学. 2022(11): 2677-2683 .  百度学术
百度学术
其他类型引用(7)




 下载:
下载: