Responses of Rhizosphere Bacterial Community to Straw-mulching and Conditioner-addition in Acid Soil of Maize Field
-
摘要:目的 以福建省黄泥田土壤为研究对象,探讨不施化肥(CK)、单一施化肥(T1)、化肥配施秸秆还田(T2)、化肥配施土壤调理剂(T3)等4组处理玉米根际土壤细菌群落组成、多样性和结构的变化。方法 利用 Illumina Miseq测序平台对4组处理土壤样品进行测序,基于第二代高通量技术分析4种处理(CK、T1、T2、T3)的玉米根际土壤细菌的16S rRNA基因在V3~V4区域的多样性指数、丰富度以及群落组成和结构。结果 4个处理的玉米根际土壤细菌优势门(相对丰度>10%)为变形菌门(Proteobacteria)、绿弯菌门(Chloroflexi)、放线菌门(Actinobacteria)。T1处理细菌的丰富度指数(ACE指数和Chao1指数)较CK均有所降低,分别降低17.65%和17.88%;T3处理的细菌丰富度指数(ACE指数和Chao1指数)高于CK处理,分别提高14.52%和14.00%。分层聚类图显示细菌属水平上,CK、T1和T2处理的土壤样品细菌群落结构相似性较高,T3与其他3个处理细菌群落结构差异较大。结论 化肥配施土壤调理剂对土壤细菌群落结构影响大于单一施化肥和化肥配施秸秆还田处理,单一施化肥降低了根际土壤细菌的丰富度,化肥配施土壤调理剂可以显著提高玉米根际土壤细菌群落的丰富度,施用土壤调理剂提高酸性土壤pH对玉米根际细菌群落影响最大。Abstract:Objective Composition and diversity of rhizosphere bacterial community in response to straw-mulching and soil conditioning on land of maize field were studied.Methods Soil at the maize growing fields was treated with either no chemical fertilizer (CK), a single chemical fertilizer (T1), straw-mulching and chemical fertilization (T2), or a soil conditioner plus chemical fertilization (T3). The second-generation technology of Illumina Miseq high-throughput sequencing was used based on the bacterial 16S rRNA genes in V3-V4 region to determine the changes of diversity, richness, composition, and structure of bacterial community in the rhizosphere soil under treatment.Results The dominant bacteria, which showed their relative abundance greater than 10%, in the rhizosphere bacterial community were 4,183 genera of Proteobacteria, Chloroflexi, and Actinobacteria. The ACE and Chao 1 richness indices of the community under T1 were 17.65% and 17.88%, respectively, lower, while those under T3, 14.52% and 14%, respectively, higher than those under CK. At genera level, the stratified cluster diagram of community structure under T3 differed from those under CK, T1, and T2.Conclusion T3 significantly affected the structure of the bacteria community and more so than did the other treatments. Among all treatments, T1 lowered, while T3 enhanced, the richness of the community over CK. And the added soil conditioner raised the pH of the acidic soil rendering the greatest effect on the rhizosphere bacterial community in maize field.
-
0. 引言
【研究意义】土壤微生物主要包括细菌、放线菌、真菌等[1],既是土壤有机质分解与转化的参与者,也是生态系统碳、氮、硫、磷等元素循环的推动者[2]。土壤细菌占土壤微生物总量的70%~90%,对环境变化敏感,可作为评价土壤健康和质量的重要指标,在土壤养分循环和肥力变化中起着重要作用[3-5]。【前人研究进展】近年来,第二代高通量测序技术在土壤微生物等领域得到广泛应用[6],可以对不同环境下微生物群落的物种组成和相对丰度等进行细致、准确的分析,极大地促进了基因组学研究的进展,为土壤微生物学的深入研究做出了巨大贡献[7]。相较于传统的测序法,高通量测序技术主要运用芯片技术一次可以测定几十万甚至几百万的序列,通过统计测序 DNA的次数实现对 DNA 丰度的准确计算,可以显著降低测序成本。【本研究切入点】由于土壤中会发生许多重要的化学和生化反应,从而导致土壤酸碱度的变化。土壤酸碱度直接影响养分元素存在形式及其生物有效性,土壤为微生物提供其生存及生长所需养分等[8],由此可见土壤环境一旦变化会直接影响微生物的优势菌群和群落结构。不同作物吸收营养物质和微量元素对土壤 pH值的需求不同,土壤 pH值也会影响种植作物对养分的吸收利用和生长[9]。【拟解决的关键问题】黄泥田是中国南方稻区典型的低产田[10],主要分布在山地丘陵,pH值平均值4.5,属于酸性土壤。土壤酸化会提高铝、锰的释放数量,导致土壤贫瘠[11],影响玉米种植产量。合理进行土壤改良,提高黄泥田作物产量,以及土壤改良后土壤微生物群落如何作出响应这方面较少研究。本研究在 Illumina Miseq平台使用高通量测序技术分析不同施肥管理模式下,玉米根际土壤样品中细菌16S rDNA,探讨单一施化肥、化肥与土壤调理剂以及化肥配施秸秆还田施肥措施对土壤细菌多样性、类群组成及结构的影响,以期揭示酸性黄泥田土壤细菌群落结构变化,为改良南方酸性土壤提高生物肥力提供理论依据。
1. 材料与方法
1.1 试验地概况
研究地点位于福建省建瓯市映山龙种业有限公司种植基地,东经118°48′30″,北纬 27°09′26″,海拔116 m,属中亚热带海洋性季风气候,全市年均气温 18.8 ℃,年降雨量约1 700 mm。试验区土壤类型为黄泥田,质地为黏土,耕层土壤pH值4.5,有机质22.40 g·kg−1,全氮 124.00 g·kg−1,碱解氮105.40 mg·kg−1,速效磷146.60 mg·kg−1,速效钾135.00 mg·kg−1,玉米品种为‘泰鲜甜1号’。
1.2 试验设计
试验设置4个处理:不施化肥(CK)、单一施化肥(T1)、化肥配施秸秆还田(T2) 和化肥配施土壤调理剂 (T3),每个处理3次田间重复。2019年3月20日进行试验,小区面积为602 m2。玉米播种行距0.60 m,密度3.6万株·hm−2。T2处理玉米秸秆还田方式为整杆埋入,还田量约为4 800 kg·hm−2。T3处理土壤调理剂原料为白云石粉与牡蛎壳粉各50%混匀,pH 10.5,施用量约为6 kg·hm−2。各处理玉米全生育期施纯N 264 kg·hm−2,播种时一次性施入基肥,旋耕,基施复合肥600 kg·hm−2,氮肥为尿素,复合肥m(N)∶m(P205)∶m(K2O)为 15∶15∶15。4月21日追施纯N 50 kg·hm−2,小喇叭口期配合降雨施纯N 70 kg·hm−2,大喇叭口期配合降雨施纯N 54 kg·hm−2。
于玉米收获期(6月25日)在近玉米株根部10 cm 处打土钻,采集玉米根际土壤(直径3 cm,深度15 cm),每个处理小区多点取样,充分混匀后取样3 次重复,土壤样品各分为2份,约50 g放入实验室−80 ℃保存,供高通量测序分析,进行土壤基本理化性质分析约500 g,参照鲍士旦[12]的方法。
1.3 土壤DNA提取和高通量测序
使用Omega Soil microbial DNA extraction kit提取土壤样品总 DNA,用 NanoDrop2000 测定DNA 的浓度和纯度。以总DNA为模板用引物338F 和806R 对 V3~V4 可变区进行 PCR 扩增。20 μL的扩增体系:10 ng DNA为模板,0.4 μL FastPfu 聚合酶,0.8 μL 引物,2 μL 2.5 mmol·L−1 dNTPs,4 μL 5×FastPfu 缓冲液。扩增反应条件:预变性95 ℃ 3 min;变性95 ℃ 30 s,退火55 ℃ 30 s和延伸72 ℃ 30 s,共27个循环;最后是延伸72 ℃ 10 min。3次重复混合纯化PCR 产物,纯化产物利用Miseq PE300 平台进行测序,由上海美吉生物公司完成。
1.4 数据分析
去除OTU 单序列和嵌合体,在相似度97%水平上利用UPARSE 软件(version 7.1 http://drive5.com/uparse/)进行聚类,有效序列信息物种分类注释使用RDP classifier 软件进行,70%阈值比对Silva数据库(SSU123)。
在97%分类水平上对4组土壤处理进行α多样性相关分析,包括chao1、shannon、coverage、ace、simpson多样性指数。
2. 结果与分析
2.1 测序结果
样本测序列数据结果在NCBI上的登录号为PRJNA678629。由表1可见,对12个土壤样品细菌16s rDNA V3~V4区测序过滤后,获得有效序列数在46 145~56 660,OTUs数在1 476~2 057,在97%相似水平下聚类统计得到各个土壤样品OTU中的丰度信息。T3处理OTUs数最多,较CK处理增加14.98%,T2处理较CK处理减少0.55%,较T1处理增加了20.53%。
表 1 4种施肥措施下根际土壤细菌的序列读数及OTUs数Table 1. Sequences and OTUs of rhizosphere bacterial community under treatments处理 Treatment 序列读数 Reads OTUs数 OTUs CK 50675±1401 b 1789±34 ab T1 46145±2253 b 1476±57 b T2 47686±1571 b 1779±145 ab T3 56660±2119 a 2057±220 a 注:① CK:不施化肥秸秆不还田;T1:常规施肥秸秆不还田;T2:常规施肥秸秆还田;T3:常规施肥加土壤调理剂。② 同列数据后不同小写字母表示差异达显著水平(P<0.05),下同。
Note: ① CK: Basic soil; T1: Conventional fertilization; T2: Humic acid organic-inorganic mixed fertilizer ; T3: Humic acid biological organic fertilizer;-N 20% Humic acid biological organic fertilizer. ② Data with different lowercase letters on same row denote significant difference between treatments (P<0.05), same for the following.2.2 不同施肥处理对玉米根际土壤细菌群落组成和丰度影响
Chao1指数和ACE指数代表细菌群落结构变化,丰富度随数值升高而增高[13];Shannon指数反映各土壤样品多样性,多样性程度随数值升高而增高;Simpson指数反映细菌类群的优势度[14]。表2所示,物种覆盖率为0.9875~0.9909,T1处理的ACE指数和Chao1指数较CK均有所降低,分别为17.65%和17.88%,T3处理的ACE指数和Chao1指数较T1处理均有显著提高,分别为39.06%和38.83%,说明施用土壤调理剂可以改善土壤细菌群落的丰富程度。
表 2 4种施肥措施下根际土壤细菌的多样性指数Table 2. Bacterial diversity of rhizosphere soil under treatments处理
TreatmentACE指数
ACE indexChao1 指数
Chao1 indexSimpson指数
Simpson indexShannon指数
Shannon index覆盖率指数
Good’s coverageCK 2170±28 ab 2164±28 ab 0.0072±0.0014 a 5.96±0.02 a 0.9889±0.0003 a T1 1787±73 b 1777±69 b 0.0124±0.0004 a 5.53±0.07 a 0.9909±0.0004 ab T2 2175±150 ab 2181±144 ab 0.0063±0.0006 a 5.94±0.13 a 0.9888±0.0005 ab T3 2485±257 a 2467±260 a 0.0115±0.006 a 6.04±0.29 a 0.9875±0.0013 b 2.3 不同处理土壤细菌类群分析
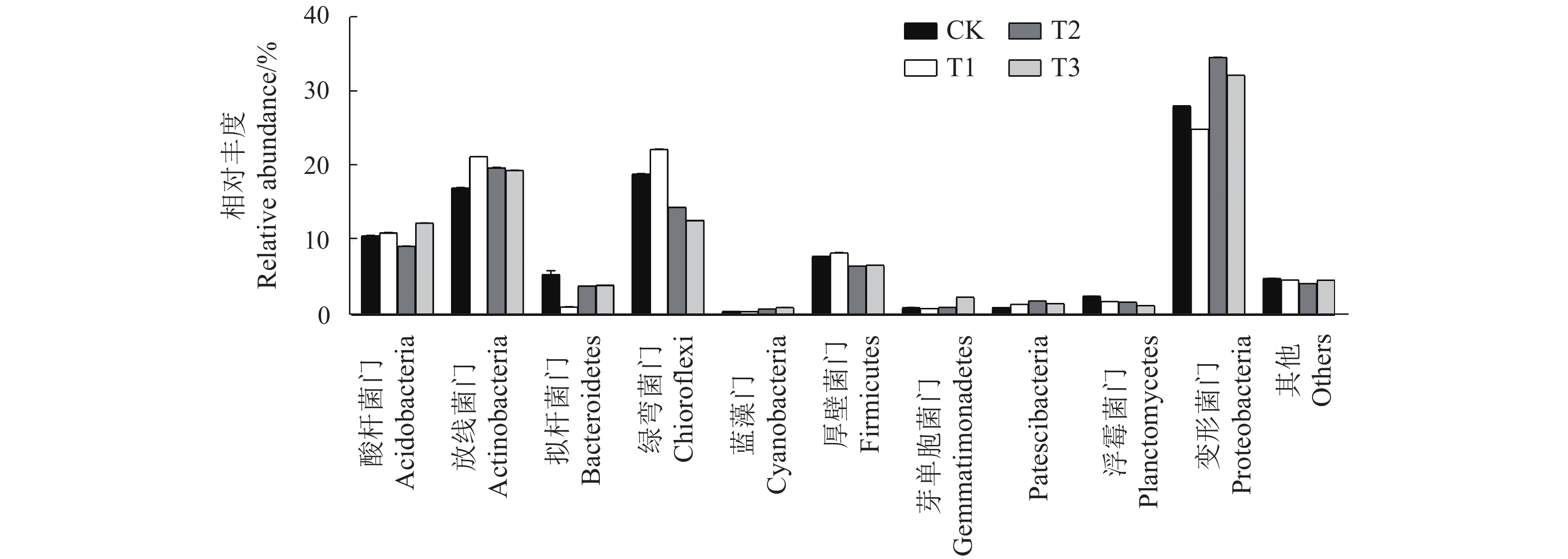
对所有土壤样品OTUs对应的生物分类学信息进行统计,由图1可以看出,变形菌门(Proteobacteria)、放线菌门(Actinobacteria)、酸杆菌门(Acidobacteria)、绿弯菌门(Chloroflexi)、拟杆菌门(Bacteroidetes)、芽单胞菌门(Gemmatimonadetes)、浮霉菌门 (Planctomycetes)、蓝藻门(Cyanobacteria)、厚壁菌门(Firmicutes)、Patescibacteria相对丰度较大,相对丰度之和在4组处理中均占到总量93%以上。
CK、T1和T3处理中的优势细菌门均为酸杆菌门、放线菌门、绿弯菌门、变形菌门,与CK相比,单一施化肥处理放线菌门和绿弯菌门相对丰度分别增加4.08%和3.24%,变形菌门相对丰度降低3.08%;与T1相比,配施调理剂(T3)变形菌门和酸杆菌门相对丰度分别增加7.14%和1.29%,放线菌门和绿弯菌门相对丰度分别降低1.77%和9.41%。T2处理优势细菌门为放线菌门、绿弯菌门、变形菌门,与T1相比,配施秸秆还田(T2)变形菌门的相对丰度增加了9.46%,放线菌门和绿弯菌门的相对丰度分别降低了1.44%和7.64%。
由图2可知,在细菌纲分类水平上,α-变形菌纲(Alphaproteobacteria)、放线菌纲(Actinobacteria)、δ-变形菌纲(Deltaproteobacteria)、γ-变形菌纲(Gamm aproteobacteria)、芽单胞菌纲 (Gemmatimonadetes)、酸杆菌纲(Acidobacteria)、拟杆菌纲(Bacteroidia)、厌氧绳菌纲(Anaerolineae)、绿弯菌纲(Chloroflexia)、纤线杆菌纲(Ktedonbacteria)、芽孢杆菌纲(Bacilli)、产氧光细菌纲(Oxyphotobacteria)等相对丰度较大,其相对丰度之和均占到各处理土壤细菌总量的80%以上。
CK和T1处理细菌优势纲分别为酸杆菌纲、α-变形菌纲、放线菌纲、纤线杆菌纲、γ-变形菌纲,T2处理细菌优势纲为放线菌纲、酸杆菌纲、γ-变形菌纲、α-变形菌纲,化肥配施土壤调理剂放线菌纲、γ-变形菌纲、α-变形菌纲为优势纲。单一施肥的土壤细菌中γ-变形菌纲、酸杆菌纲、纤线杆菌纲的相对丰度较CK分别增加了39.43%、2.55%、15.48%,α-变形菌纲和放线菌纲相对丰度分别降低了29.27%和2.86%。与单一施肥处理相比,化肥配施秸秆还田处理增加了α-变形菌纲和酸杆菌纲的相对丰度,增加60.35%和5.85%,降低了γ-变形菌纲和放线菌纲的相对丰度,降低22.07%和6.5%;化肥配施土壤调理剂处理增加了α-变形菌纲的相对丰度,增加13.28%,γ-变形菌纲、放线菌纲、酸杆菌纲相对丰度分别降低了29.05%、37.06%、49.16%。
对相对丰度排名前50的细菌属进行双向二维聚类,展示多样品间OTUs情况(图3),可以直观通过颜色的梯度及相似程度清楚地获知样本间细菌丰度变化,颜色逐渐加深代表细菌属相对丰度逐渐升高。图3中12个土壤样品分成两大类,CK、T1和T2处理土壤样品细菌群落结构较相似聚为一类,T3单独为一类。由此可知在细菌属水平上,施入土壤调理剂对土壤细菌群落结构影响大于秸秆还田与常规施肥处理。鞘氨醇单胞菌属、芽单胞菌属在T3处理相对丰度最大,丛生放线菌属相对丰度最小。
通过对门水平下土壤细菌种群分布和环境因子的冗余分析,从图4-A可以看出速效钾、总钾和 pH的射线较长,说明对土壤样品中细菌的影响较大,呈显著相关性。图4-B基于属水平下土壤细菌种群分布和环境因子的冗余分析,pH、总磷、总钾和速效钾的射线较长,与土壤细菌呈显著相关性。
3. 讨论
本研究旨在探讨秸秆还田和土壤调理剂的施用对酸性土壤中细菌种群多样性的影响,目前关于这方面的报道还较少。大部分植物适应中性或微酸性土壤生长,土壤 pH值太低会引发植物病虫害,也会增强土壤中有毒金属元素的活性。本试验所用的土壤调理剂原料主要是白云石粉和牡蛎壳粉,有研究表明白云石粉和牡蛎壳粉在对改良酸性土壤方面有明显效果[15],并且对玉米生物学性状影响方面,也表现出明显的增加效果,可以明显提高玉米地上部生物量、株高、根重与根长,且随土壤调理剂施用量的增加而增加[16]。本研究中,化肥配施土壤调理剂处理的细菌群落丰富度较单一施化肥处理显著提高,这可能是因为土壤调理剂的施入改善了土壤酸性环境,影响了一部分对土壤酸度极其敏感的微生物。合理的秸秆还田也可以在一定范围内改善土壤pH,促使其向中性土壤或是适合所种植作物生长的酸碱度变化,秸秆在土壤微生物的降解下可以释放出大量的有机质,增加细菌多样性[17]。
有研究表明,施用白云石粉可以显著降低土壤中交换性铝含量,并且土壤中有效磷和速效钾含量会随着白云石粉用量的增加而增加[15];秸秆中含有丰富的钾资源[18-19],秸秆还田对于土壤速效钾含量的提高具有显著作用[20],一定范围内土壤速效钾含量的提高会随秸秆还田量的增加而增大[21]。本研究中速效钾、总钾和土壤pH对门水平下土壤细菌种群分布影响较大,呈显著相关性;pH、总磷、总钾和速效钾对属水平下土壤细菌种群分布影响较大,呈显著相关性,可能是由于化肥配施土壤调理剂和秸秆还田提高了土壤养分的有效性,改变了土壤细菌群落生存环境,从而影响土壤细菌类群的相对丰富度。
CK、T1和T3处理中的优势细菌门为酸杆菌门、放线菌门、绿弯菌门、变形菌门,T2处理优势细菌门为放线菌门、绿弯菌门、变形菌门,与前人研究结果一致[22-23];优势细菌纲有α-变形菌纲、γ-变形菌纲、酸杆菌纲、放线菌纲、纤线杆菌纲。4个处理中的变形菌门相对丰度均为最大,化肥配施秸秆还田和土壤调理剂均提高了变形菌门的相对丰度,变形菌门是细菌域中最大的一门,被广泛用于氮肥的促进利用[24]。有相关研究表明,土壤酸杆菌的相对丰度与土壤 pH 值呈负相关关系[25],也有研究表明因受土壤其他环境因子影响,酸杆菌的相对丰度与土壤 pH 相关性不显著[26]。本研究中,化肥配施土壤调理剂处理的酸杆菌门相对丰度较单一施化肥处理略有减少,可能是由于施用土壤调理剂增加了土壤中交换性铝含量,酸杆菌细菌中不同亚群对土壤环境因子的适应性存在差异有关。放线菌门可以降解土壤中的各种不溶性有机物质,对有机物的矿化有着重要作用,从而参与自然界氮素循环[27]。单一施化肥处理放线菌门相对丰度大幅提高,可能与全氮的含量与利用有关,化肥配施秸秆还田处理较单一施化肥处理放线菌门的相对丰度略有减少,可能与秸秆还田时间有关,长期施用对放线菌门丰富度的影响会更明显。鞘氨醇单胞菌属对芳香化合物有极为广泛的代谢能力,芽单孢菌属与磷代谢相关,在化肥配施土壤调理剂处理中相对丰度最大。
4. 结论
化肥配施土壤调理剂可以显著提高土壤细菌群落丰富性。化肥配施土壤调理剂对土壤细菌群落结构影响大于单一施化肥和化肥配施秸秆还田处理,单一施化肥降低了土壤细菌丰富度。施用土壤调理剂提高酸性土壤 pH对玉米根际细菌群落影响最大。黄泥田酸性土壤细菌群落结构对秸秆还田和土壤调理剂的响应机制还需要进一步深入研究。
-
表 1 4种施肥措施下根际土壤细菌的序列读数及OTUs数
Table 1 Sequences and OTUs of rhizosphere bacterial community under treatments
处理 Treatment 序列读数 Reads OTUs数 OTUs CK 50675±1401 b 1789±34 ab T1 46145±2253 b 1476±57 b T2 47686±1571 b 1779±145 ab T3 56660±2119 a 2057±220 a 注:① CK:不施化肥秸秆不还田;T1:常规施肥秸秆不还田;T2:常规施肥秸秆还田;T3:常规施肥加土壤调理剂。② 同列数据后不同小写字母表示差异达显著水平(P<0.05),下同。
Note: ① CK: Basic soil; T1: Conventional fertilization; T2: Humic acid organic-inorganic mixed fertilizer ; T3: Humic acid biological organic fertilizer;-N 20% Humic acid biological organic fertilizer. ② Data with different lowercase letters on same row denote significant difference between treatments (P<0.05), same for the following.表 2 4种施肥措施下根际土壤细菌的多样性指数
Table 2 Bacterial diversity of rhizosphere soil under treatments
处理
TreatmentACE指数
ACE indexChao1 指数
Chao1 indexSimpson指数
Simpson indexShannon指数
Shannon index覆盖率指数
Good’s coverageCK 2170±28 ab 2164±28 ab 0.0072±0.0014 a 5.96±0.02 a 0.9889±0.0003 a T1 1787±73 b 1777±69 b 0.0124±0.0004 a 5.53±0.07 a 0.9909±0.0004 ab T2 2175±150 ab 2181±144 ab 0.0063±0.0006 a 5.94±0.13 a 0.9888±0.0005 ab T3 2485±257 a 2467±260 a 0.0115±0.006 a 6.04±0.29 a 0.9875±0.0013 b -
[1] 林先贵, 胡君利. 土壤微生物多样性的科学内涵及其生态服务功能 [J]. 土壤学报, 2008, 45(5):892−900. LIN X G, HU J L. Scientific connotation and ecological service function of soil microbial diversity [J]. Acta Pedologica Sinica, 2008, 45(5): 892−900.(in Chinese)
[2] 曹志平. 土壤生态学[M]. 北京: 化学工业出版社, 2007. [3] 齐虹凌, 贺国强, 李恒全, 等. 轮作与连作对烤烟不同生育期根际土壤细菌群落结构的影响 [J]. 中国烟草学报, 2015, 21(5):42−48. QI H L, HE G Q, LI H Q, et al. Effects of rotational and continuous cropping on bacterial community structures in rhizospheric soil at different growth stages of flue-cured tobacco [J]. Acta Tabacaria Sinica, 2015, 21(5): 42−48.(in Chinese)
[4] CARSWELL A M, HILL P W, JONES D L, et al. Short-term biotic removal of dissolved organic nitrogen (DON) compounds from soil solution and subsequent mineralisation in contrasting grassland soils [J]. Soil Biology and Biochemistry, 2016, 96: 82−85. DOI: 10.1016/j.soilbio.2016.01.017
[5] MANOHARAN L, KUSHWAHA S K, AHRÉN D, et al. Agricultural land use determines functional genetic diversity of soil microbial communities [J]. Soil Biology and Biochemistry, 2017, 115: 423−432. DOI: 10.1016/j.soilbio.2017.09.011
[6] 樊晓刚, 金轲, 李兆君, 等. 不同施肥和耕作制度下土壤微生物多样性研究进展 [J]. 植物营养与肥料学报, 2010, 16(3):744−751. FAN X G, JIN K, LI Z J, et al. Soil microbial diversity under different fertilization and tillage practices: A review [J]. Plant Nutrition and Fertilizer Science, 2010, 16(3): 744−751.(in Chinese)
[7] 李玉新, 赵忠, 陈金泉, 等. 沙棘林土壤微生物多样性研究 [J]. 西北农林科技大学学报(自然科学版), 2010, 38(8):67−74, 82. LI Y X, ZHAO Z, CHEN J Q, et al. Study on soil microbial diversity of seabuckthorn forest [J]. Journal of Northwest a& f University (Natural Science Edition), 2010, 38(8): 67−74, 82.(in Chinese)
[8] 刘玮琦, 茆振川, 杨宇红, 等. 应用16S rRNA基因文库技术分析土壤细菌群落的多样性 [J]. 微生物学报, 2008, 48(10):1344−1350. LIU W Q, MAO Z C, YANG Y H, et al. Analysis of soil bacterial diversity by Using the 16S rRNA gene Library [J]. Acta Microbiologica Sinica, 2008, 48(10): 1344−1350.(in Chinese)
[9] 朱兆良, 文启孝. 中国土壤氮素[M]. 南京: 江苏科学技术出版社, 1992. [10] 荣勤雷, 梁国庆, 周卫, 等. 不同有机肥对黄泥田土壤培肥效果及土壤酶活性的影响 [J]. 植物营养与肥料学报, 2014, 20(5):1168−1177. RONG Q L, LIANG G Q, ZHOU W, et al. Effects of different organic fertilization on fertility and enzyme activities of yellow clayey soil [J]. Plant Nutrition and Fertilizer Science, 2014, 20(5): 1168−1177.(in Chinese)
[11] 王飞, 林诚, 李清华, 等. 长期不同施肥方式对南方黄泥田水稻产量及基础地力贡献率的影响 [J]. 福建农业学报, 2010, 25(5):631−635. WANG F, LIN C, LI Q H, et al. Effects of long-term fertilization on rice yield and contribution rate of basic soil productivity on the yellow paddy of Southern China [J]. Fujian Journal of Agricultural Sciences, 2010, 25(5): 631−635.(in Chinese)
[12] 鲍士旦. 土壤农化分析[M]. 3版. 北京: 中国农业出版社, 2000. [13] WANG Y, SHENG H F, HE Y, et al. Comparison of the levels of bacterial diversity in freshwater, intertidal wetland, and marine sediments by using millions of illumina tags [J]. Applied and Environmental Microbiology, 2012, 78(23): 8264−8271. DOI: 10.1128/AEM.01821-12
[14] 葛英亮, 于水利, 时文歆, 等. 应用Illumina MiSeq高通量测序技术解析O3−BAC饮用水处理过程细菌多样性变化 [J]. 食品科学, 2016, 37(16):223−228. GE Y L, YU S L, SHI W X, et al. Analysis of bacterial diversity in O3−BAC drinking water treatment process by using illumina MiSeq high throughput sequencing technology [J]. Food Science, 2016, 37(16): 223−228.(in Chinese)
[15] 王爱英, 赵啸林, 孙玲丽, 等. 沼渣土壤调理剂对胶东地区酸性土壤改良效果研究 [J]. 中国沼气, 2019, 37(4):98−102. WANG A Y, ZHAO X L, SUN L L, et al. Effect of soil conditioner of biogas slurry on acid soil improvement in Jiaodong area [J]. China Biogas, 2019, 37(4): 98−102.(in Chinese)
[16] 李昂. 四种土壤调理剂对酸性土壤铝毒害改良效果研究[D]. 北京: 中国农业科学院, 2014. LI A. Remediate effects on aluminum toxicity by using four soil conditioners in acid soils[D]. Beijing: Chinese Academy of Agricultural Sciences, 2014. (in Chinese).
[17] KALBITZ K, KAISER K. Contribution of dissolved organic matter to carbon storage in forest mineral soils [J]. Journal of Plant Nutrition and Soil Science, 2010, 171(1): 52−60.
[18] 戴志刚, 鲁剑巍, 李小坤, 等. 不同作物还田秸秆的养分释放特征试验 [J]. 农业工程学报, 2010, 26(6):272−276. DAI Z G, LU J W, LI X K, et al. Nutrient release characteristic of different crop straws manure [J]. Transactions of the Chinese Society of Agricultural Engineering, 2010, 26(6): 272−276.(in Chinese)
[19] 郑丹. 不同条件下作物秸秆养分释放规律的研究[D]. 哈尔滨: 东北农业大学, 2012. ZHENG D. The nutrient releasing regularity of crop stalks under different conditions[D]. Harbin: Northeast Agricultural University, 2012. (in Chinese).
[20] 王志勇, 白由路, 杨俐苹, 等. 低土壤肥力下施钾和秸秆还田对作物产量及土壤钾素平衡的影响 [J]. 植物营养与肥料学报, 2012, 18(4):900−906. WANG Z Y, BAI Y L, YANG L P, et al. Effects of application of potassium fertilizer and straw returning on crop yields and soil potassium balance in low-yielding fields [J]. Plant Nutrition and Fertilizer Science, 2012, 18(4): 900−906.(in Chinese)
[21] IQBAL M, UL-HASSAN A, VAN ES H M. Influence of Residue Management and Tillage Systems on Carbon Sequestration and Nitrogen, Phosphorus, and Potassium Dynamics of Soil and Plant and Wheat Production in Semi-arid Region [J]. Communications in Soil Science and Plant Analysis, 2011, 42(5): 528−547. DOI: 10.1080/00103624.2011.546929
[22] 王怡, 常彬河, 刘月, 等. 基于MiSeq测序分析酸性农作物土壤细菌群落结构与多样性 [J]. 环境科学研究, 2019, 32(9):1575−1583. WANG Y, CHANG B H, LIU Y, et al. Analysis of bacterial community composition and diversity in acid soil using MiSeq sequencing [J]. Research of Environmental Sciences, 2019, 32(9): 1575−1583.(in Chinese)
[23] 李丹, 靳鲲鹏, 李小霞, 等. 基于高通量测序技术的玉米不同生育时期土壤细菌多样性变化 [J]. 山西农业科学, 2019, 47(9):1569−1572. LI D, JIN K P, LI X X, et al. Variations of soil bacterial diversity at different growth stages in maize based on high-throughput sequencing [J]. Journal of Shanxi Agricultural Sciences, 2019, 47(9): 1569−1572.(in Chinese)
[24] LIU J J, SUI Y Y, YU Z H, et a1. High throughput sequencing analysis of biogeographical distribution of bacterial communities in the black soils of northeast China [J]. Soil Biology and Biochemistry, 2014, 70: 113−122. DOI: 10.1016/j.soilbio.2013.12.014
[25] GRIFFITHS R I, THOMSON B C, JAMES P, et a1. The bacterial biogeography of British soils [J]. Environmental Microbiology, 2011(13): 1642−1654.
[26] NAVARRETE A A, KURAMAE E E, DE HOLLANDER M, et al. Acidobacterial community responses to agricultural management of soybean in Amazon forest soils [J]. FEMS Microbiology Ecology, 2013, 83(3): 607−621. DOI: 10.1111/1574-6941.12018
[27] LAUBER C L, STRICKLAND M S, BRADFORD M A, et a1. The influence of soil properties on the structure of bacterial and fungal communities across land-use types [J]. Soil Biology and Biochemistry, 2008, 40(9): 2407−2415. DOI: 10.1016/j.soilbio.2008.05.021
-
期刊类型引用(2)
1. 魏全全,张萌,芶久兰,顾小凤,柳玲玲. 土壤调理剂用量对连作酒用高粱生长、黄壤养分及微生物的影响. 现代园艺. 2023(12): 4-7+26 .  百度学术
百度学术
2. 刘梦丹,胡思敏,王宗抗. 深汕特别合作区旱地土壤肥力状况调查与分析. 安徽农业科学. 2023(18): 74-77+81 .  百度学术
百度学术
其他类型引用(1)




 下载:
下载: