Cloning and Expression of Pathogenesis-related Protein Gene, BoPR1, in Brassica oleracea var. italica
-
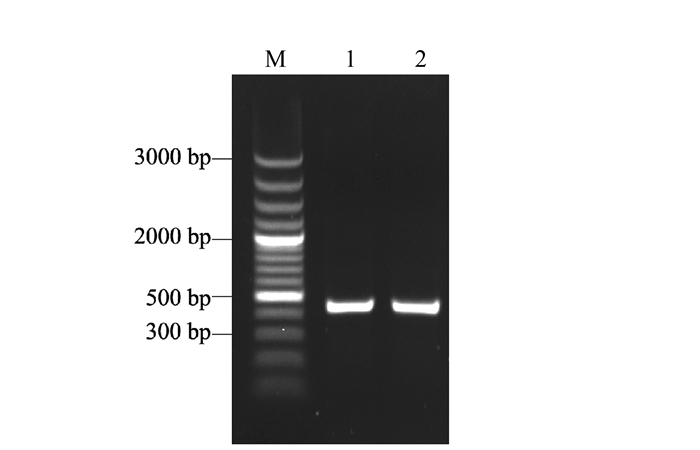
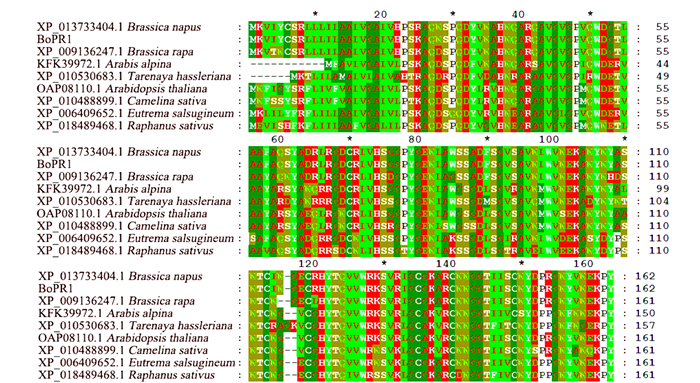
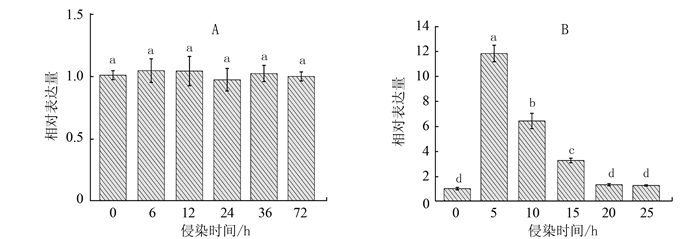
摘要: 病程相关蛋白(Pathogenesis-related protein,PR)是参与植物抗病性的重要物质,在诱导系统抗性过程中起着重要作用。本研究以青花菜为材料,在克隆BoPR1基因的基础上,利用荧光定量PCR技术研究它们在根肿菌和核盘菌侵染下的表达模式。序列分析结果表明,BoPR1基因组全长为489 bp,无内含子,编码162个氨基酸,具1个信号肽和1个SCP结构域。系统发育分析的结果表明,BoPR1与甘蓝型油菜和白菜的PR1遗传距离最小,亲缘关系最近,在进化树上聚为一组;与醉蝶花PR1遗传距离最大,亲缘关系最远。荧光定量PCR结果显示,BoPR1基因的表达受根肿菌诱导,在接种5 d时的表达量最高,为对照的11.84倍;BoPR1基因的表达则不受核盘菌诱导。Abstract: Pathogenesis-related proteins (PRs) are crucial in the induced systemic disease resistance for plants. Using real-time fluorescence quantitative PCR, this study isolated a gene, designated as BoPR1, frombroccoli to examine its expression patterns after inoculated by pathogens, Plasmodiophora brassicae and Sclerotinia sclerotiorum. A sequence analysis indicated that the full genome DNA of BoPR1 was 489 bp in length encoding 162 amino acids and containing no intron. The deduced protein consisted of a signal peptide and a SCP domain. The results from aphylogenetic analysis showed thatBoPR1 had a minimum genetic distance, clustering on a same clade, with the PR1 proteins from Brassica napus and B. rapa, indicating a close relationship among them. On the other hand, it was remotely related to Tarenaya hassleriana, as the genetic distance between the two PR1swas the greatest among the tested samples. Theq RT-PCR results suggested that the expression of BoPR1 was induced by P. brassicae, with the highest level observed 5 d after inoculationwhich was 11.84-fold of control. But, BoPR1 expression was not affected by S. sclerotiorum. Theobtained isolation and expression information on BoPR1 would be useful for futureresearch on thedisease resistance mechanism as well as the molecular breeding programs on B. oleracea.
-
Keywords:
- Brassica oleracea var. italica /
- BoPR1 /
- gene cloning /
- expression analysis
-
0. 引言
【研究意义】贫困问题一直以来都是发展中国家经济和社会发展过程中重点关注问题之一。十九大报告指出,2017-2020年是全面建成小康社会的决胜期,到2020年实现全面脱贫是全面建设小康社会的根本要求。农业产业扶贫作为一项重要扶贫举措在全国各地大面积推广。然而,从农业产业扶贫的效果来看具有较大差异,在一部分地区农业产业扶贫取得显著成果,有效促进贫困户的脱贫,但是另一部分地区则出现农业产业扶贫项目无法有效推进的问题。是什么原因导致了农业产业项目不同的实施效果?在什么条件下农业产业扶贫才能实现有效减贫,在什么条件下不太适合农业产业扶贫?因此,研究农业产业扶贫的门槛条件,对精准扶贫、有效利用扶贫资金有重要的现实指导意义。【前人研究进展】产业扶贫作为一种新型的扶贫措施,不同于以往的“输血”措施,盘活了当地资源,赋予贫农可持续发展的能力,因而广受欢迎。有学者研究表明,农业产业扶贫通过打造优势产业,培育内生发展能力,有效推动减贫的进程[1]。当资本超过一定的门槛值以后,才能摆脱贫困,进入资本积累促进减贫的阶段,依赖稳定持续的经济增长获得增长带来的减贫效应。即当资本超过某一门槛值时,经济增长的横向“扩散效应”和纵向的“涓滴效应”才能显现出来[2]。20世纪50年代出现了贫困固化的三大理论[3],分别是纳克斯的贫困恶性循环理论[4]、纳尔逊的低水平均衡陷阱理论[5]和缪尔达尔的循环积累因果关系理论[6]。这3个理论均认为是物质或人力资本的匮乏导致了贫困固化的产生。只有物质或人力资本越过一定的门槛值以后,经济理论才能发挥作用,即存在门槛效应[7]。随着20世纪60年代新古典主义的兴起,部分发展经济学家认为制度问题是导致贫困的主要原因。制度的不完善,会使得拥有相同经济资源的地区采取不同的发展路径,从而分化稳定在高水平或低水平均衡状态。发展要素如物质资本、人力资本、公共资本等的严重匮乏,会形成自我强化,使得贫困地区陷入贫困循环状态。当这些重要的发展要素超过一定的门槛值,进一步投资才会推动经济进入良性积累的循环过程,促进经济的稳步增长[8]。关于农业产业发展的益贫性,已经有许多学者做出大量的研究。农业产业扶贫是指将贫困农户的生产活动纳入到社会农业产业的大循环中[9],以市场为导向,以当地资源为依托,发展当地特色产业的扶贫模式[10]。农业产业扶贫可以通过集聚化和品牌化两条道路实现减贫。这两条路径的基本思路一个是通过集聚的规模效应实现成本优势,从而实现农业产业高产值;另一个是通过打造高端优质产业,实现差异化优势,增加农业产业的附加值。邰秀军等[11]以山西的县域数据论证了农业产业集聚和品牌化对于农民收入以及农业人均GDP的提升作用。此外,农业综合资源的优化也有助于减贫[12]。农业产业化扶贫可以通过政府和市场两方面的力量共同实现减贫,其中以政府财政作为支撑的农业产业化经营投入可以有效促进贫困的减少[13]。郭雅[14]认为农业产业化经营可以通过帮助农民克服技术短板、健全农业经营组织、加速资本积累、优化产业结构这4个途径实现减贫。显而易见的是,农业具有弱质性。农业弱质性源于难以形成有效的专业化分工组织,与其他产业相比生产率较低[15]。农业对于自然具有强依赖性,生产周期较长,市场调节机制滞后、失灵,农民的抗风险能力较差,而消费者的需求弹性又很小。王丽华[16]分析了地缘性贫困群体的特征及贫困因素,认为农业贫困主要是人力资本投资的不足。沈洋[17]认为山区贫农除了个人劳动能力不足,以及农业技术匮乏之外,农业经营的分散性也成为农户收入难以增长的重要原因。王定祥等[18]研究发现贫困农户的信贷需求较高,但是满足率较低。农民面临的信贷约束也会进一步加深农业的弱质性。罗楚亮[19]分析了农村贫困状况的变动状况,认为经营收入的波动是导致农户贫困的一个重要因素,外出务工等工资性收入增长可以有效促进扶贫。兼业农户的生计资本禀赋要远远优于纯农业户[20]。【本研究切入点】在金融和医疗领域,扶贫的门槛条件已经得到检验。但是在农业领域,前人的研究大多集中在农业产业扶贫的效果上,针对为何农业产业扶贫具有不同的扶贫效果鲜见深入分析。【拟解决的关键问题】从农业产业扶贫的门槛条件入手,基于福建省县域贫困和社会经济统计的面板数据,构建门槛效应模型,检验农业产业扶贫的门槛条件,研究在什么条件下农业产业扶贫才能有较好的扶贫效果,打开农业产业扶贫效果异质性的“黑盒之谜”,为精准扶贫和扶贫资金的有效利用提供政策参考。
1. 研究方法
随着计量经济学的发展,门槛效应在检验方法上有了长足的进步。Hansen[21]提出了运用bootstrap方法检验门槛效应模型(threshold regression)门槛值的显著性,该方法得以广泛应用。在实证分析中,该模型被拓展至金融领域[22]、环境领域[23]等。与以往文献相比,本文的创新点在于将模型拓展至农业生产领域,探究是否当农村居民人均可支配收入越过一定的门槛,农业产业的规模效应或结构优化才能对贫困显现出减贫效应。农业产业对于贫困有正、负两种效应,即农业产业本身的弱质性与农业产业的益贫性共同作用决定了农业产业的减贫效应。当益贫性大于弱质性的时候,农业生产的适度规模将呈现出减贫效应;当益贫性小于弱质性时,农业产业的发展陷入贫困之中,规模扩张无助于减贫,只有调整农业产业结构才能有效突破农业弱质性的制约。之所以会出现不同的效果,根本原因在于贫困地区和富裕地区的社会与经济发展基础水平不同,部分农村居民人均可支配收入较低的地区陷入贫困固化的漩涡,难以发挥出农业产业的益贫性,农业产业的弱质性凸显。
综上所述,门槛模型在实证分析上拓展至金融和环境等各个扶贫领域。农业生产领域因其同时存在益贫性和弱质性,构成了贫困的内在逻辑。据此提出假说:当地区农业基础设施不完善时,农业产业的规模扩张无助于减贫,只有通过农业产业的结构调整才能发挥出减贫效应;当地区跳出贫困循环状态,农业产业的适度规模有利于减缓贫困。本文将从农业规模和结构两个方面着手,以农村居民人均可支配收入作为门槛变量,验证农业产业扶贫的门槛效应。
2. 变量选取与实证分析
2.1 变量的选取
本文选取2016年福建省的县、区级相关数据进行分析,共计84个样本量。贫困人口作为被解释变量,以农业产业规模、农业产业结构为核心解释变量,农村居民人均可支配收入作为门槛变量进行验证。除此之外,基础设施、金融情况、教育水平、医疗条件作为控制变量。贫困人口数据来源于福建省农业农村厅扶贫办,其他数据来源于《福建省统计年鉴2017》。
2.1.1 被解释变量
本文选择贫困人口作为模型的被解释变量。贫困人口可以反映贫困的基本情况,是个绝对数指标。根据中央脱贫计划表,到2020年要实现全面脱贫,福建总体的贫困人口相对较少,2016年贫困发生率仅为0.54%,贫困发生率这个相对指标意义被弱化了,福建贫困的绝对人数是脱贫的关键所在。采用贫困人口作为模型的因变量是合理合适的。贫困人口数据来源于福建省农业农村厅扶贫办。在实施精准扶贫之后,贫困人口的统计口径才可以规范统一。
2.1.2 解释变量
农业产业规模:选择第一产业生产总值作为衡量农业产业规模的核心指标,单位为亿元。农业产业结构:选择非粮作物播种面积占农作物播种总面积的比值作为农业产业结构的衡量指标。这里的农业产业结构,主要指粮食作物和非粮作物的相对结构,该比例可以反映农业产业结构。本文选择农村居民人均可支配收入作为门槛变量。
控制变量包含基础设施、金融情况、教育水平、医疗条件等4个方面。其中,基础设施的主要衡量指标为:农村投递路线总长度(km)和公路通车里程(km)。这两个方面主要代表信息通路和交通通路的基础设施,是当地与外界联结的核心指标。金融情况主要分为金融规模、金融效率和金融结构。金融规模是指金融机构人民币各项存款和贷款余额的总和,以亿元为单位。金融效率用金融机构人民币各项贷款余额占金融机构人民币各项存款余额的比重表示。金融结构是指短期贷款占中长期贷款的比重。教育水平主要指地区的教师数和学生数的比值,即师生比。卫生条件主要以卫生机构数、卫生技术人员数作为衡量指标。
2.2 模型设定与描述性分析
根据以上分析,本文重点考察农业产业规模和结构对于贫困减缓的影响,同时考虑到贫困减缓还受到其他社会经济因素的影响,因此引入基础建设、金融约束、教育水平和医疗条件等因素作为控制变量。本文设定的基本估计方程为:
Ppverty=β0+β1⋅ArgScale⋅(Income>k)+β2⋅ArgStructure⋅(Income>k)+β3⋅Deliverty+β4⋅Road+β5⋅Fscale+β6⋅Fefficiency+β7⋅FStructure+β8⋅TSratio+β9⋅Hospital+β10⋅HManpover+ε (1) 式(1)中,βi (i=1~10)为模型估计系数,k表示贫困的农村居民人均可支配收入门槛值,ε表示随机误差。
表 1给出了所用变量的定义与描述统计。
表 1 变量描述Table 1. Descriptions of statistic variables变量
Variable均值
Mean标准差
Standard error最小值
Minimum最大值
Maximum被解释变量Interpreted variables 贫困人口Poor Population/人 2389.69 2769.63 0 10710.00 农业产业情况Agriculture 农业产业规模Scale of Agriculture/亿元 29.18 22.36 0.13 138.98 农业产业结构Agricultural Industry Structure 0.56 0.16 0.26 1.00 门槛变量Threshold variables 农村居民人均可支配收入Per capita disposable income of rural residents/元 25571.80 17848.36 10516.55 96850.64 基础设施Infrastructure 农村投递路线总长度Total length of rural delivery routes/km 1284.21 1195.25 449.00 7167.00 公路通车里程Highway mileage/km 1301.89 781.02 87.00 4058.00 金融环境Financial environment 金融规模Financial scale/亿元 1.41 0.47 0.21 3.16 金融效率Financial efficiency 0.76 0.28 0.32 1.91 金融结构Financial structure 0.78 0.41 0.21 2.34 教育水平Education level 师生比Teacher student ratio 0.07 0.01 0.05 0.10 医疗条件Medical conditions 卫生机构数Number of health institutions/个 329.26 183.84 106.00 933.00 卫生技术人员数Number of health technicians/人 2629.63 2572.73 407.00 15721.00 注:贫困人口数据来源于福建省农业农村厅扶贫办,其他数据来源于《福建省统计年鉴2017》。
Note:Data on poverty-stricken population are from the Poverty Alleviation Office of Fujian Agricultural Bureau,and others from Fujian Statistical Yearbook 2017.2.3 模型的估计
本文在农村居民人均可支配收入所有取值范围内进行网格搜寻及遍历回归,找出模型残差标准误最小的点。如图 1所示,通过自举法(Bootstrap)重复抽取样本,得到当农村居民人均可支配收入为14 146元时,模型的残差标准误最小。并且,以农村居民人均可支配收入14 146元作为门槛值进行拟合回归。当农村居民人均可支配收入大于门槛值时,估计结果在0.01水平上显著。因此,该门槛值是显著有效的。当农村居民人均可支配收入越过门槛值以后,很有可能可以摆脱贫困,通过农业产业的发展促进贫困的减缓。
3. 结果与分析
由以上分析(表 2)可知,当农村居民人均可支配收入低于门槛值时,农业产业规模越大,贫困人口越多。即当人们陷入贫困时,农业产业规模越大,农业产业的弱质性越强于益贫性,越不利于减贫。处于贫困中的市县推行农业产业的规模化是不现实的。但是,改善农业产业的结构是有利于减贫的。
表 2 农业产业减贫效应的估计结果(因变量:贫困人口)Table 2. Estimated poverty alleviation in agriculture communities (dependent variables: population in poverty)变量
Variable估计值
Coefficients标准误
Standard errort值
t valueP值
P value截距项Intercept 7124.564 4744.811 1.502 0.14052 农业产业规模Scale of agriculture 90.4663 37.4943 2.413 0.02017** 农业产业结构Agricultural iIndustry structure -14842.4 5233.323 -2.836 0.00694*** 农村居民人均可支配收入>14146元
Per capita disposable income of rural residents>14146 Yuan-5247.14 3375.845 -1.554 0.12744 农村投递路线总长度Total Length of rural delivery route/km -0.8889 0.4341 -2.048 0.04673** 公路通车里程Highway mileage/km 0.4768 0.5916 0.806 0.42469 金融规模Financial scale/亿元 -772.067 829.9796 -0.93 0.35745 金融效率Financial efficiency -2252.41 1335.283 -1.687 0.09888* 金融结构Financial structure 1076.541 806.8983 1.334 0.18917 师生比Teacher student ratio 26770.49 36885.96 0.726 0.47192 卫生机构数Number of health institutions/个 3.5539 2.9137 1.22 0.22922 卫生技术人员数Number of health technicians/人 0.2931 0.5985 0.49 0.62682 农业产业规模:农村居民人均可支配收入>14146元
Scale of agriculture: Per capita disposable income of rural residents>14146 Yuan-95.47 40.6836 -2.347 0.02362** 农业产业结构:农村居民人均可支配收入>14146元
Agricultural structure: Per capita disposable income of rural residents>14146 Yuan12337.73 6337.306 1.947 0.0581* F统计值(F statistical value):4.096 R2 :0.5532 注:***、**、*表示估计结果在0.01、0.05、0.1的水平上显著。
Note: ***,** and * indicate estimates of significance at levels of 0.01,0.05,0.1,respectively.当农村居民人均可支配收入高于门槛值时,扩大农业规模才有利于减少贫困,改善农业产业结构仍然具有减贫效应,但是没有基础设施完善的地区效果显著。从模型回归结果看,当农村居民人均可支配收入高于门槛值时,随着农业产业规模的扩大,农业产业的益贫性强于弱质性,减贫效应开始显现。若某个地区已经脱离贫困,就会进入资本积累的良性循环,农业产业的适度规模就会产生规模经济,大幅提高农民的经济收益。
4. 结论与政策建议
综上,本文运用2016年福建省贫困人口数据以及福建统计年鉴相关数据,分析农业产业规模和结构的减贫效应。研究结果表明,福建地区农村贫困门槛值为农村居民人均可支配收入14 146元;当农村居民人均可支配收入低于该门槛值时,贫困地区很难通过农业产业规模的发展以及经济水平的提升减缓贫困,但是改善农业产业结构有利于减缓贫困。当农村居民人均可支配收入超过该门槛值时,农业产业的规模扩张才能对农村减贫发挥出正向效应。
对于尚未跳出贫困陷阱的地区,建议从以下几方面开展扶贫工作:
第一,优化农业产业结构促进减贫。通过发展非粮经济作物,发掘特色优势产业,培育具有地域特色的产业增收项目,增强农村经济活力。通过优化产业布局、调优农业产业结构,不断地提升贫困地区的农业生产的竞争力,提高农产品的质量和效益。
第二,农业基础尚未完善的地区实施兜底式扶贫。极端贫困户陷于贫困的泥沼,迫于生计,思维能力以及道德品行退化,无法摆脱贫困。对于这一批丧失基本生活保障、无劳动能力的贫困户,通过给予低保兜底保障、资金补助、生产资料供给、异地搬迁等“输血式”模式,逐步改善其生产生活条件。
第三,以工代赈,完善农村农业生产基础设施建设。对于尚未完善农业基础设施的县域,以全面完善基础设施建设为核心任务,依靠财政支持、挂钩帮扶、项目对接等形式提升县域整体经济水平,不断完善农村交通网络,升级和维护社会公共设施,完善医疗、教育等社会事业,实施以工代赈,提升贫困农户生计水平。
对于跳出贫困陷阱的地区,可以从以下几方面开展农业产业扶贫工作:
第一,对于跳出贫困陷阱的地区,加快农地流转,促进农业适度规模发展。挖掘优势特色农业产业,促进农业产业集聚,通过规模化提升农业产业竞争力。促进农业生产要素流入农业专业大户、农业技术能人、公司企业等农业经营主体,充分发挥资源最大价值以及企业家精神,做强做大农业。
第二,针对有非农意愿的部分小农户,推广资源资产收益扶贫机制。探索扶贫资金量化折股试点,将各类财政扶贫资金及涉农发展资金注入农业项目,并根据资产量化折股给贫困户,保障贫困户能够按股分红,实现股权收益。探索资源型收益扶贫试点,将土地、生态林地等农业资源入股,增加股权收益,引导村集体和贫困户参与经营管理,健全农业经营主体的收益联动机制。
-
-
[1] 林俊. 青花菜标准化栽培关键技术研究[D]. 杭州: 浙江大学, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10335-2009156642.htm [2] 陈晓峰. 不结球白菜抗真菌病基因的克隆与表达分析[D]. 扬州: 南京农业大学, 2008. http://cdmd.cnki.com.cn/Article/CDMD-10307-2009076976.htm [3] 崔香仙.西兰花主要病害及其综合防治[J].特种经济动植物, 2005, 8(3):42-42. http://www.cqvip.com/QK/92994A/200503/15162748.html [4] 陈海平. 青花菜霜霉病病原和流行因素研究[D]. 杭州: 浙江大学, 2012. http://cdmd.cnki.com.cn/Article/CDMD-10335-1013186946.htm [5] 高婷婷. 大白菜抗霜霉病防御信号途径中相关基因的表达分析[D]. 扬州: 扬州大学, 2013. http://www.wanfangdata.com.cn/details/detail.do?_type=degree&id=y2418919 [6] SEKHWAL M K, LI P, LAM I, et al. Disease resistance gene analogs (RGAs) in plants[J]. International Journal of Molecular Sciences, 2015, 16(8):19248-19290. DOI: 10.3390/ijms160819248
[7] GOVRIN E M, LEVINE A. The hypersensitive response facilitates plant infection by the necrotrophic pathogen Botrytis cinerea[J]. Current Biology, 2000, 10(13):751-757. DOI: 10.1016/S0960-9822(00)00560-1
[8] 刘利华, 林奇英, 谢华安, 等.病程相关蛋白与植物抗病性研究[J].福建农业学报, 1999, 14(3):53-58. http://www.cnki.com.cn/Article/CJFDTOTAL-FJNX199903011.htm [9] 杨瑞瑞, 易小娅, 曾幼玲. PR10的结构、信号转导以及功能的研究进展[J].中国农学通报, 2014, 30(4):251-258. DOI: 10.11924/j.issn.1000-6850.2013-2152 [10] 王勇刚, 曾富华, 吴志华, 等.植物诱导抗病与病程相关蛋白[J].湖南农业大学学报:自然科学版, 2002, 28(2):177-182. http://www.cnki.com.cn/Article/CJFDTOTAL-SJNY199108016.htm [11] 杨德翠, 张玉喜, 郑国生.牡丹病程相关蛋白1基因的克隆及表达分析[J].园艺学报, 2013, 40(8):1583-1590. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=yyxb201308019 [12] 王燕华, 何水林.植物诱导抗病性的分子生物学研究进展[J].应用与环境生物学报, 2004, 10(6):811-815. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=yyyhjswxb200406029 [13] 罗红丽, 秦云霞, 闫志烨, 等.巴西橡胶树病程相关蛋白基因(HbPR1)的克隆及分析[J].热带作物学报, 2011, 32(8):1499-1502. http://www.cnki.com.cn/Article/CJFDTotal-CYKE201506003.htm [14] ZHOU J M, TRIFA Y, SILVA H, et al. NPR1 differentially interacts with members of the TGA/OBF family of transcription factors that bind an element of the PR-1 gene required for induction by salicylic acid[J]. Molecular Plant-microbe Interactions, 2000, 13(2):191-202. DOI: 10.1094/MPMI.2000.13.2.191
[15] 张小丽, 刘玉梅, 方智远, 等.青花菜及近缘种属种质资源抗根肿病鉴定[J].植物遗传资源学报, 2016, 17(6):1106-1115. http://www.cnki.com.cn/Article/CJFDTOTAL-ZNYK200810015.htm [16] DELLAPORTA S L, WOOD J, HICKS J B. A plant DNA minipreparation:version Ⅱ[J]. Plant Molecular Biology Reporter, 1983, 1(4):19-21. DOI: 10.1007/BF02712670
[17] 张凯敏, 王玉成, 杨桂燕, 等.柽柳ThPR1基因的克隆与表达分析[J].南京林业大学学报:自然科学版, 2013, 37(2):45-49. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=njlydxxb201302008 [18] 马立功, 张匀华, 孟庆林, 等.向日葵病程相关蛋白HaPR1基因的克隆与功能[J].作物学报, 2015, 41(12):1819-1827. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zuowxb201512006 [19] 姚红燕, 皇甫伟国, 赵海棠, 等.青花菜几种病害的初步调查[J].宁波农业科技, 2004, (4):2-4. http://cpfd.cnki.com.cn/Article/CPFDTOTAL-IGSS200400001016.htm [20] 王汉荣. 青花菜褐茎病病原鉴定及其防治技术研究[D]. 杭州: 浙江大学, 2010. http://cdmd.cnki.com.cn/article/cdmd-10335-1011060984.htm [21] LOON L C V, REP M, PIETERSE C M J. Significance of inducible defense-related proteins in infected plants[J]. Annual Review of Phytopathology, 2006, 44(1):135-162. DOI: 10.1146/annurev.phyto.44.070505.143425
[22] 侯丽霞, 高超, 车永梅, 等.葡萄病程相关蛋白1基因的克隆和表达分析[J].植物生理学报, 2012, 48(1):57-62. http://www.cnki.com.cn/Article/CJFDTOTAL-ZWSL201201011.htm [23] AGRAWAL G K, NAMSOO J, RAKWAL R. A novel rice (Oryza sativa L.) acidic PR1 gene highly responsive to cut, phytohormones, and protein phosphatase inhibitors[J]. Biochemical & Biophysical Research Communications, 2000, 274(1):157-165. https://www.sigmaaldrich.com/catalog/papers/10903912
[24] 赵淑清, 郭剑波.植物系统获得抗性及信号转导途径[J].中国农业科学, 2003, 36(7):781-787. http://www.wanfangdata.com.cn/details/detail.do?_type=perio&id=zgnykx200307009 [25] ALEXANDER D, GOODMAN R M, GUT-RELLA M, et al. Increased tolerance to two oomycete pathogens in transgenic tobacco expressing pathogenesis-related protein 1a[J]. Proceeding of the National Academy of Science of America, 1993, 90(15):7327-7331. DOI: 10.1073/pnas.90.15.7327
[26] SAROWAR S, KIM Y J, KIM E N, et al. Overexpression of a pepper basic pathogenesis-related protein 1 gene in tobacco plants enhances resistance to heavy metal and pathogen stresses[J]. Plant Cell Reports, 2005, 24(4):216-224. DOI: 10.1007/s00299-005-0928-x
[27] 赵长江, 鲁国东, 杜晓昱, 等.水稻纹枯病发病过程PR1和PBZl的表达动态[J].植物病理学报, 2006, 26(4):317-321. http://mall.cnki.net/magazine/Article/ZWBL200604006.htm -
期刊类型引用(4)
1. 南瑞江,肖俊涛. 基于贫困户感知的脱贫驱动力因素实证分析——以鄂西北集中连片特困区9县1637户的调查数据为基础. 湖北文理学院学报. 2021(11): 73-79 .  百度学术
百度学术
2. 郭萌,王怡. 秦巴山区商洛市核桃产业发展的规模特征及经济效应. 农业工程. 2020(06): 124-128 .  百度学术
百度学术
3. 钱力,彭瑞峰. 大别山连片特困地区经济增长益贫性时空差异分析. 重庆理工大学学报(社会科学). 2020(08): 29-36 .  百度学术
百度学术
4. 刘金领,刘辉. 产业扶贫打破纳克斯贫困恶性循环——基于国家级贫困县N县的调研分析. 农村经济与科技. 2020(17): 137-140 .  百度学术
百度学术
其他类型引用(5)




 下载:
下载: